Clear Sky Science · sv
KCTD1 stabiliserar c-Myc för att uppreglera PD-L1 och dämpa anti-tumörimmunitet vid hepatocellulär cancer
Varför detta betyder något för framtidens cancerbehandling
Många personer med levercancer drar inte nytta av dagens mest lovande immunterapier, som är utformade för att frigöra kroppens egna T-celler mot tumörer. Denna studie undersöker varför en vanlig form av levercancer, hepatocellulär cancer, fortfarande kan gömma sig från immunsvar även under behandling — och identifierar en ny molekylär strömbrytare, kallad KCTD1, som skulle kunna få befintliga immunläkemedel att fungera bättre.
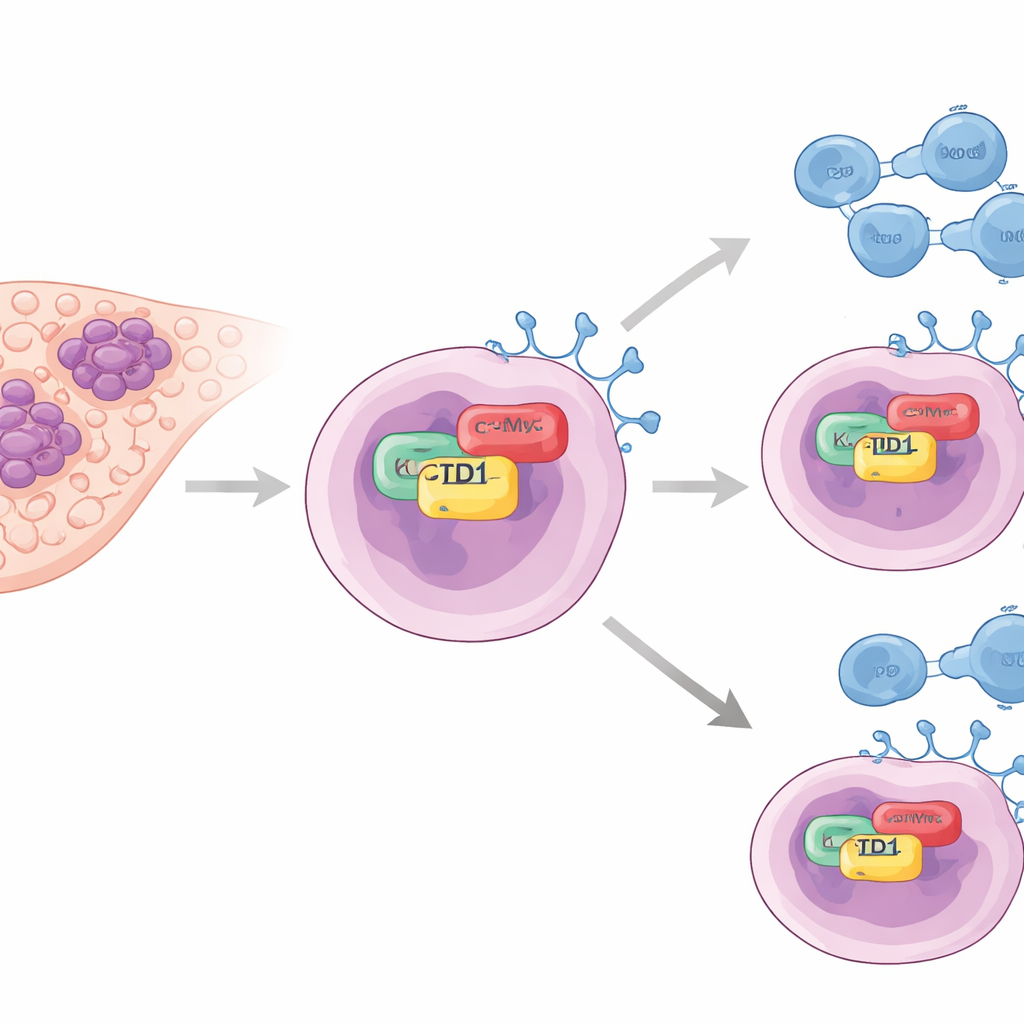
En dold hjälpare till tumörers "avstängningsknappar"
Författarna fokuserade på ett protein som heter KCTD1, tidigare kopplat till levertumörtillväxt men inte väl studerat i samband med immunundvikande. I tumörprover från patienter fann de att nivåerna av KCTD1 var markant högre i canceröst levervävnad än i normal lever. Viktigt är att tumörer rika på KCTD1 också hade höga nivåer av PD-L1, ett ytprotein på cancerceller som binder PD-1 på T-celler och i praktiken säger åt immunsystemet att hålla tillbaka. Patienter med tumörer som hade lägre KCTD1 tenderade att leva längre, vilket tyder på att detta protein är kopplat både till sjukdomens allvar och till styrkan i tumörens immunskydd.
Sambindning av molekylära ledtrådar inne i cancerceller
För att förstå hur KCTD1 ökar PD-L1 vände sig teamet till levercancercellinjer odlade i laboratoriet. När de minskade KCTD1 sjönk PD-L1-proteinnivåerna och den kvarvarande PD-L1 bröts ner snabbare, vilket indikerar att KCTD1 hjälper till att stabilisera PD-L1 snarare än bara att slå på dess gen. Med biokemiska pull-down-experiment och fluorescensmikroskopi visade de att KCTD1 fysiskt binder en annan viktig tumördrivare, onkoproteinet c-Myc, inne i cellkärnan. Denna interaktion sker via specifika kontaktregioner på båda proteinerna och leder till ett mer stabilt c-Myc, vilket i sin tur ökar PD-L1-produktionen. När c-Myc ensam minskades föll PD-L1 även om KCTD1 var rikligt, vilket placerar c-Myc som den avgörande mellanlänken i en KCTD1–c-Myc–PD-L1-kedja.
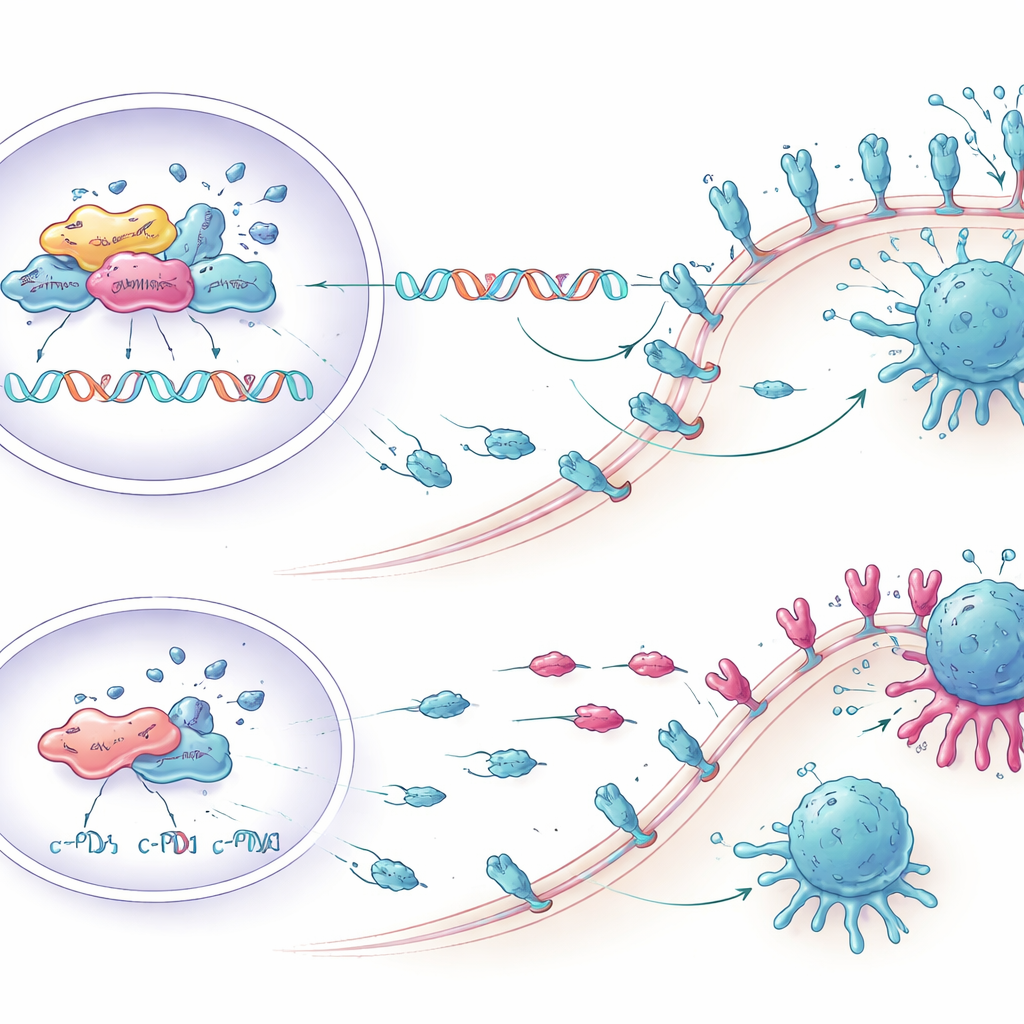
Återväckande av T-celler i laboratoriet
Forskarna frågade sedan om sänkning av KCTD1 faktiskt kunde förstärka immunsvaret. De samexponerade mänskliga levercancerceller med immunceller tagna från blodgivare. Tumörceller som konstruerats för att ha mindre KCTD1, och därmed mindre PD-L1, utlöste starkare svar från CD8-T-celler — immunsystemets huvudmördare av cancerceller. Fler av dessa T-celler producerade inflammatoriska molekyler som TNF-α och interferon-gamma, visade högre markörer för tillväxt och aktivering och uppvisade färre tecken på utmattning. Resultatet blev att fler tumörceller genomgick programmerad celldöd när KCTD1 undertrycktes, vilket visar att de molekylära förändringarna översattes till reella vinster i immundödande.
Test av mekanismen i möss
För att se om samma mönster gäller i levande organismer implanterade teamet muslevercancerceller som saknade KCTD1 direkt i mössens lever. Tumörer med reducerat KCTD1 bildade färre och mindre knutor, visade långsammare celldelning och hade fler cancerceller som genomgick celldöd. Dessa tumörer uttryckte också mindre c-Myc och PD-L1. Avlägsnande av CD8-T-celler från mössen utplånade mycket av denna fördel, vilket indikerar att tumörminskningen i hög grad berodde på T-cellernas aktivitet. Slutligen, när forskarna kombinerade KCTD1-nedreglering med en anti–PD-1-antikropp — ett befintligt läkemedel mot immunkontrollspunkter — hade mössen den minsta tumörbördan och de högsta nivåerna av CD4- och CD8-T-cellsinfiltration i sina tumörer.
Vad detta kan betyda för patienter
Sammantaget visar arbetet att KCTD1 är en central koordinator som stabiliserar c-Myc, ökar PD-L1 på levercancerceller och dämpar CD8-T-cellers angrepp. Att störa denna väg gör tumörer både mer sårbara för immunsystemet och mer mottagliga för PD-1–blockerande läkemedel i möss. För patienter antyder detta att läkemedel riktade mot KCTD1 eller dess kontaktyta med c-Myc i framtiden skulle kunna kombineras med nuvarande immunterapier för att hjälpa fler personer med levercancer att uppnå varaktig immun kontroll över sin sjukdom.
Citering: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
Nyckelord: hepatocellulär cancer, tumörimmunterapi, PD-1 PD-L1-väg, c-Myc-signalering, T-cells anti-tumörimmunitet