Clear Sky Science · sv
Multi-omik avslöjar heterogenitet och funktionella populationer av oligodendrocytprogenitorceller inducerade av humana neurala stamceller
Varför det är viktigt att skydda hjärnans isolering
Hjärnans ledningsnät är beroende av ett fettlager kallat myelin, som sveper runt nervfibrerna som isolering runt elektriska kablar. När myelin skadas, som vid multipel skleros och andra sjukdomar, blir signalerna långsammare eller går förlorade, vilket orsakar problem med rörelse, syn och tänkande. Denna studie undersöker en särskild grupp humana celler som kan bygga upp myelin igen och ställer en praktisk fråga: vilka celler är bäst lämpade för framtida cellterapier för att reparera denna viktiga isolering?
Från startceller i hjärnan till myelinbyggare
Forskarna utgick från humana neurala stamceller—mångsidiga startceller tagna från fostervävnad i hjärnan som redan är inriktade att bli nervsystemets celler. De styrde dessa stamceller i laboratoriet att differentiera till oligodendrocytprogenitorceller, eller hOPC:er, som är direkta föregångare till de myelinbildande cellerna. Under mikroskopet förändrades cellerna från enkla runda former till mer komplexa med flera förgreningar, och de slog på karakteristiska proteiner som markerar steg på vägen mot mogna myelinproducerande celler. Detta gav en pålitlig, relativt säker källa av humana myelinbyggande prekursorer för detaljerad analys.
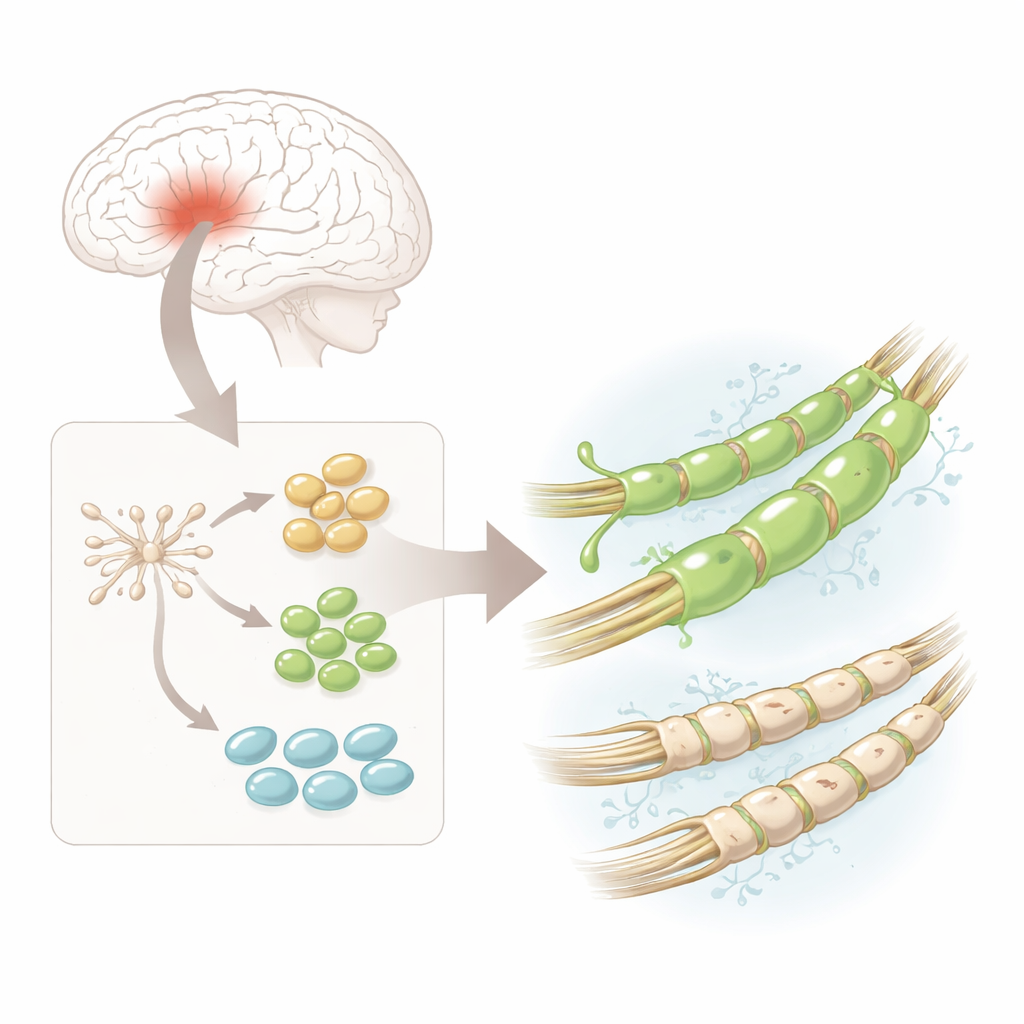
En celltyp, många dolda varianter
Med hjälp av single-cell RNA-sekvensering—en metod som läser av vilka gener som är aktiva i tusentals individuella celler—upptäckte teamet att hOPC:erna inte var identiska. Istället grupperade de sig i tre huvudstadier: tidiga ”pre-progenitorer”, mer engagerade progenitorer och celler som närmade sig full oligodendrocytidentitet. Över alla dessa stadier framträdde en gen särskilt: PDGFRA, som kodar för en cellytereceptor. En mycket känslig avbildningsmetod kallad RNA-Scope bekräftade att PDGFRA:s budskap och protein var mer rikliga än andra nyckelmarkörer i varje stadium, vilket tyder på att denna receptor kan definiera särskilt kapabla myelinbyggande celler.
Att sålla fram de mest kraftfulla reparationscellerna
För att testa denna idé separerade forskarna hOPC:erna i två grupper baserat på om de bar PDGFR-α-receptorn på ytan eller inte. De jämförde därefter PDGFR-α–positiva celler, PDGFR-α–negativa celler och osorterade celler i en serie funktionstester. När de transplanterades i så kallade »shiverer»-möss—som inte kan bilda normal myelin—producerade de PDGFR-α–positiva cellerna tätare, mer kompakt myelin runt nervfibrerna än de andra grupperna. Dessa celler migrerade också längre och delade sig snabbare i laboratorieassay. Med andra ord var PDGFR-α–positiva populationen mest energisk när det gällde att röra sig dit den behövdes, öka i antal och återuppbygga isoleringen.
Signalsystem inuti som driver tillväxt och reparation
Genom att gå djupare jämförde teamet genaktiviteten mellan PDGFR-α–positiva och –negativa celler. De fann att de positiva cellerna slog på nätverk av gener involverade i gliacelltillväxt och myelinbildning, samt flera viktiga signalvägar inuti cellen. Särskilt två vägar stack ut: PI3K–AKT–mTOR, som länge kopplats till celltillväxt och myelinproduktion, och TGF-β-signalering, som påverkar hur unga hjärnceller väljer sina öden. Uppgifterna föreslog att aktivering av PDGFR-α matar in i PI3K–AKT–mTOR, vilket i sin tur stärker TGF-β–relaterade signaler, och tillsammans skjuter cellerna mot att bli effektiva myelinbyggare.
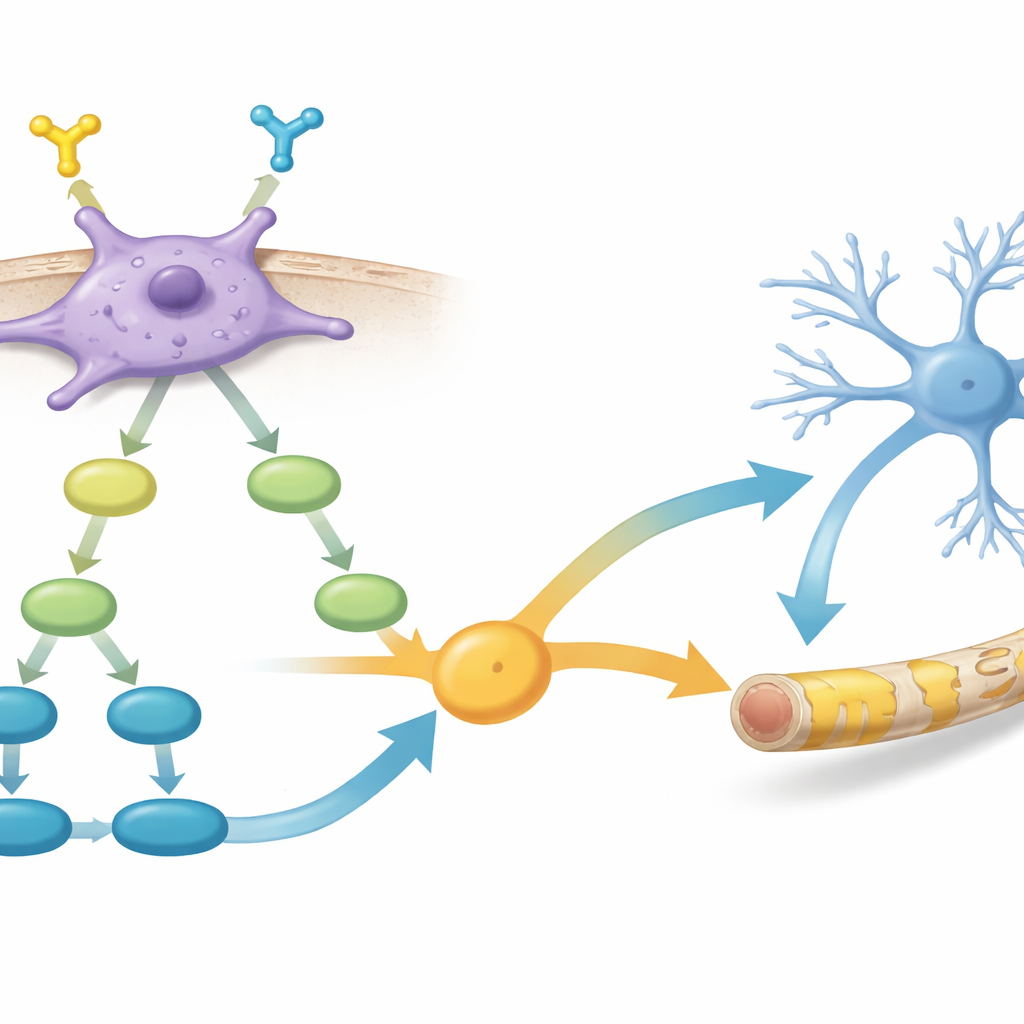
Att förbättra myelinreparation med ett kemiskt hjälpmedel
Forskarna undrade sedan om de kunde förbättra dessa lovande celler ytterligare. De behandlade PDGFR-α–positiva hOPC:er med en liten molekyl som aktiverar TGF-β-vägen och undersökte både genaktivitet och beteende. Efter behandling visade dessa celler högre nivåer av flera myelinrelaterade gener och producerade tjockare, mer fullständiga myelinskidor när de transplanterades i shiverer-möss, jämfört med obehandlade PDGFR-α–positiva celler. Detta stödjer idén att noggrann fininställning av interna signaler i redan välvalda progenitorceller kan förbättra deras förmåga som levande verktyg för myelinreparation.
Vad detta betyder för framtida behandlingar
För icke-specialister är kärnbudskapet att inte alla myelinbyggande prekursorceller är likadana. Genom att kombinera kraftfulla genavläsnings- och avbildningsverktyg identifierar denna studie en framstående undergrupp—PDGFR-α–positiva hOPC:er—that migrerar bättre, delar sig mer och återbygger myelin mer effektivt än sina likar. Den belyser också interna signalvägar som kan kemiskt påverkas för att göra dessa celler ännu mer potenta. Tillsammans lägger dessa insikter en färdplan för att utforma säkrare, mer effektiva cellterapier för att återställa hjärnans isolering vid sjukdomar där myelin gått förlorat.
Citering: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
Nyckelord: myelinreparation, oligodendrocytprogenitorceller, neutrala stamceller, cellterapi, single-cell RNA-sekvensering