Clear Sky Science · sv
Mitochondriell bioenergetik–SASP‑korsprat avgör senolytisk effektivitet vid terapiinducerad senescens
Varför det är så svårt att zappa ”zombieliknande” cancerceller
Många moderna cancerläkemedel dödar inte varje tumörcell direkt. Istället går vissa celler in i ett limbo‑liknande tillstånd som kallas senescens: de slutar dela sig men förblir vid liv, lite som ”zombieceller”. Dessa terapiinducerade senescenta celler kan till en början vara fördelaktiga, men om de dröjer sig kvar kan de driva återfall, resistens och biverkningar. Forskare testar därför senolytiska läkemedel som är utformade för att selektivt döda senescenta celler. Denna artikel ställer en vilseledande enkel fråga: varför dör vissa senescenta cancerceller när de utsätts för senolytika, medan andra envist överlever?
Kraftverk som bär minnet av sitt förflutna
I studiens kärna finns mitokondrierna, cellernas små kraftverk. Författarna undersökte om sättet mitokondrier använder olika bränslen—såsom socker, fett och aminosyror—påverkar hur känsliga senescenta cancerceller är för senolytiska läkemedel som riktar sig mot ett överlevnadsprotein kallat BCL‑xL. Med hjälp av ett höggenomströmningsprov (MitoPlate S‑1) ”fingeravtryckade” de funktionellt mitokondriell aktivitet i flera cancercellinjer före och efter att senescens utlösts av olika behandlingar (DNA‑skadande läkemedel, mitoshämmare, oxidativ stress eller cellcykelhämmare). De fann att terapiinducerad senescens inte skapade ett enda, enhetligt mitokondriellt tillstånd. Istället lämnade varje läkemedel ett distinkt ”bioenergetiskt avtryck” som ändrade hur brett och intensivt mitokondrierna kunde använda olika energikällor. Avgörande var att denna flexibilitet låg ovanpå en förhandsinställd grundnivå: de ursprungliga föräldrarnas mitokondriella konfiguration satte en övre gräns—”taket”—för hur starkt ett senare senolytiskt svar kunde bli.
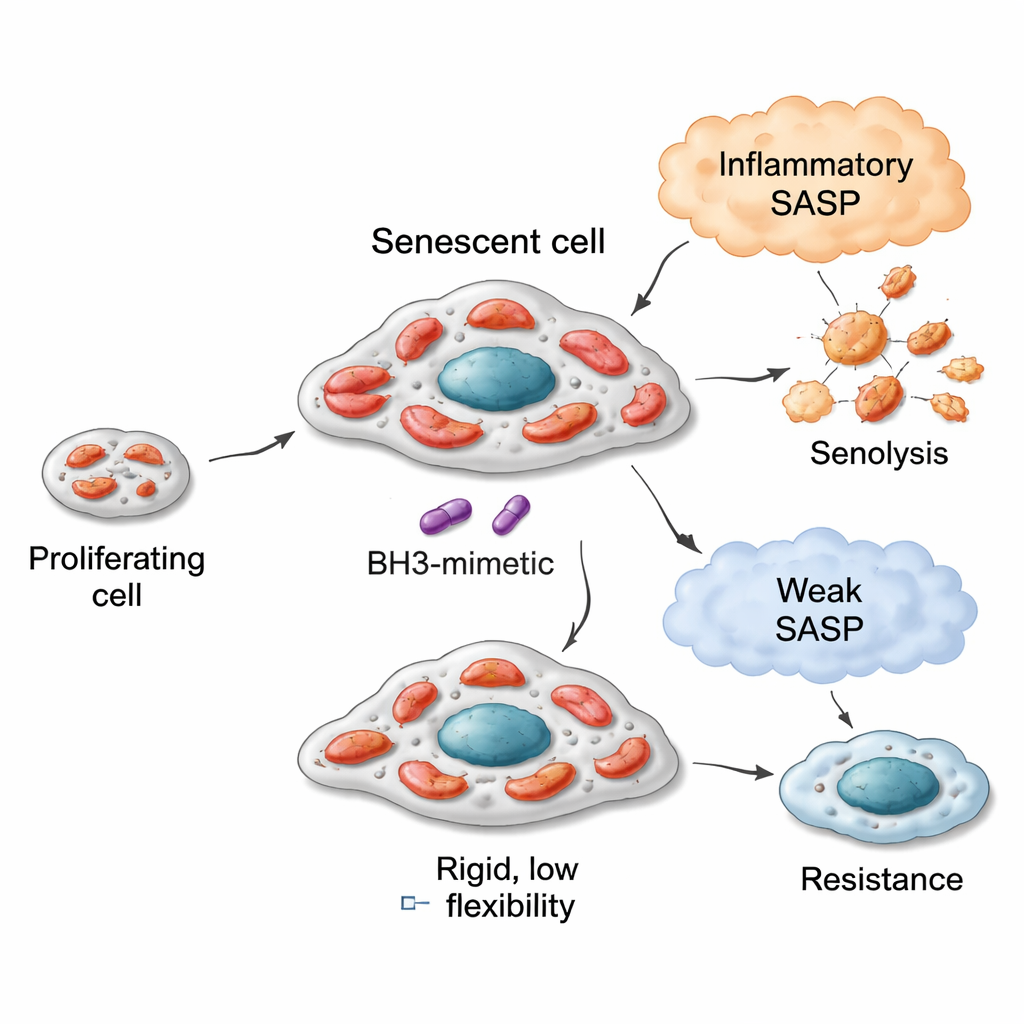
Flexibla motorer, olika bränslen och senolytisk känslighet
I modeller för lung‑, bröst‑ och tjocktarmscancer tenderade senescenta celler med mer flexibla mitokondrier—som kunde oxidera ett bredare spektrum av bränslen—att vara mer sårbara för BCL‑xL‑riktade senolytika som navitoclax (ABT‑263) och A1331852. Exempelvis utvecklade lungceller som tvingades in i senescens av läkemedlet bleomycin mitokondrier som energiskt använde många substrat, särskilt sådana kopplade till fettsyrekatabolism och vissa aminosyravägar. Dessa celler var mycket känsliga för senolytika. I kontrast visade celler som inducerades till senescens med en CDK4/6‑hämmare (palbociklib) ett smalare metaboliskt repertoar och svarade dåligt på samma senolytiska medel. Ändå hade detta samband gränser: bröstcancerceller kunde också bli metaboliskt flexibla efter senescens, men eftersom deras utgångsmitokondrier var mindre ”förberedda” för apoptos blev deras maximala senolytiska respons måttlig. Tjocktarmsceller med defekt apoptotisk maskineri förblev resistenta oavsett hur deras metabolism skiftade. Ett enkelt mått—hur väl cellerna oxiderade substratet succinat i baseline—tjänade som en enkel indikator på denna ärvda mitokondriella kapacitet.
När metabolism talar med inflammation
Senescenta celler är ökända för SASP, en cocktail av utsöndrade inflammatoriska och tillväxtfaktorer som kan påverka omgivande vävnader. Teamet undersökte hur mitokondriell metabolism kopplar till detta sekretoriska beteende med hjälp av celler konstruerade med en rapportör för miR‑146a, en mikroRNA som aktiveras av den inflammatoriska huvudregulatorn NF‑κB. De fann att medan övergripande SASP‑profiler i stor utsträckning bestämdes av celltypen, aktiverade endast vissa senescenta tillstånd denna NF‑κB/miR‑146a‑axel. Det var samma tillstånd som svarade väl på BCL‑xL‑senolytika. Viktigt var att dessa ”inflammatoriska SASP‑positiva” senescenta celler också visade ökad användning av fettsyreoxidation och en transkriptionell uppreglering av gener som transporterar långkedjiga fetter in i mitokondrierna. Att blockera fettsyretransporten med läkemedlet etomoxir dämpade miR‑146a‑aktiveringen utan att helt vända senescens, vilket tyder på att mitokondriellt val av bränsle bidrar till att möjliggöra en inflammatorisk, senolytik‑tillåtande SASP.
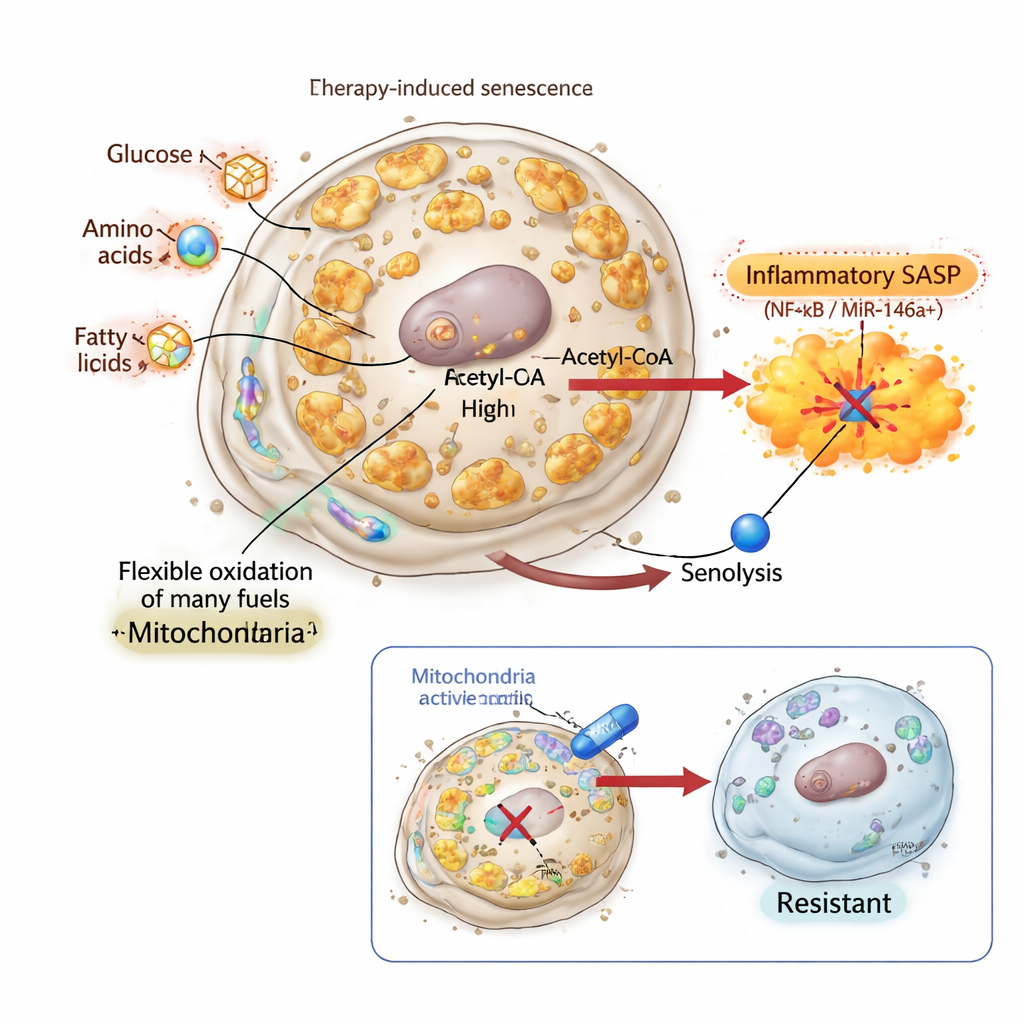
Tysta signalen och skapa odödliga senescenta celler
För att testa om den inflammatoriska SASP verkligen krävs för senolytisk död användte forskarna inflachromene, en förening som binder kromatinproteinerna HMGB1 och HMGB2 och blockerar deras roll i att aktivera SASP‑gener. I lung‑ och bröstcancerceller framkallade inflachromene en skolboksliknande senescent fenotyp: cellerna blev stora, slutade dela sig och ackumulerade senescensmarkörer. Deras mitokondriella massa och bioenergetiska aktivitet ökade avsevärt, och deras bränsleanvändning omprogrammerades tydligt. Ändå var deras SASP dämpad och miR‑146a‑rapportören förblev till stora delar tyst. Slående nog var dessa SASP‑negativa senescenta celler helt resistenta mot BCL‑xL‑riktade senolytika, trots att de hade bioenergetiskt aktiva, omprogrammerade mitokondrier och minskad uttryck av den klassiska anti‑apoptotiska genen BCL2. Detta visade att mitokondriella förändringar ensamma inte räcker; utan en mitokondriedriven inflammatorisk utsignal faller senolytikans ”andra slag”.
Vad detta betyder för framtida cancerbehandlingar
För en lekmannaläsare är studiens slutsats att dödandet av terapiinducerade ”zombieliknande” cancerceller styrs av en flerskiktad krets. För det första bestämmer en tumörcells ursprungliga mitokondriella hälsa och koppling hur långt senolytiska läkemedel någonsin kan gå. För det andra kan den särskilda behandling som orsakar senescens skjuta mitokondriell metabolism mot mer eller mindre flexibilitet, och flytta celler närmare eller längre från apoptosens rand. För det tredje—och mest avgörande—fungerar senolytika bara väl om metabol omprogrammering framgångsrikt engagerar ett inflammatoriskt SASP‑program som kommunicerar tillbaka till kärnan. Utan den inflammatoriska korspraten kan senescenta celler bli ett återvändsgrändigt, läkemedelsresistent tillstånd. Praktiskt innebär detta att framtida terapier kanske kan optimeras genom funktionella tester av både mitokondriell flexibilitet och SASP‑inflammation i tumörer, för att sedan välja kombinationer av senescensinducerande läkemedel och senolytika som ser till att ”zombiecellerna” inte bara fryses i stånd utan är förberedda för avlägsnande.
Citering: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
Nyckelord: cellulär senescens, mitokondrier, senolytika, cancermetabolism, inflammatorisk SASP