Clear Sky Science · sv
SREBP1-nedreglering utlöser ferroptos genom att undertrycka Nrf2-XCT/GPX4-axeln vid ovarialcancer
Att vända cancerens fettfabrik mot sig själv
Äggstockscancer upptäcks ofta sent och kan vara mycket svår att behandla. Denna studie undersöker en oväntad sårbarhet i dessa tumörer: deras beroende av att producera fetter och lipider. Forskarna visar att man genom att stänga av en nyckelregulator för fettproduktion i cancerceller både kan bromsa deras tillväxt och slå på en särskild form av celldöd, samtidigt som det blir lättare för immunsystemet att angripa tumören.
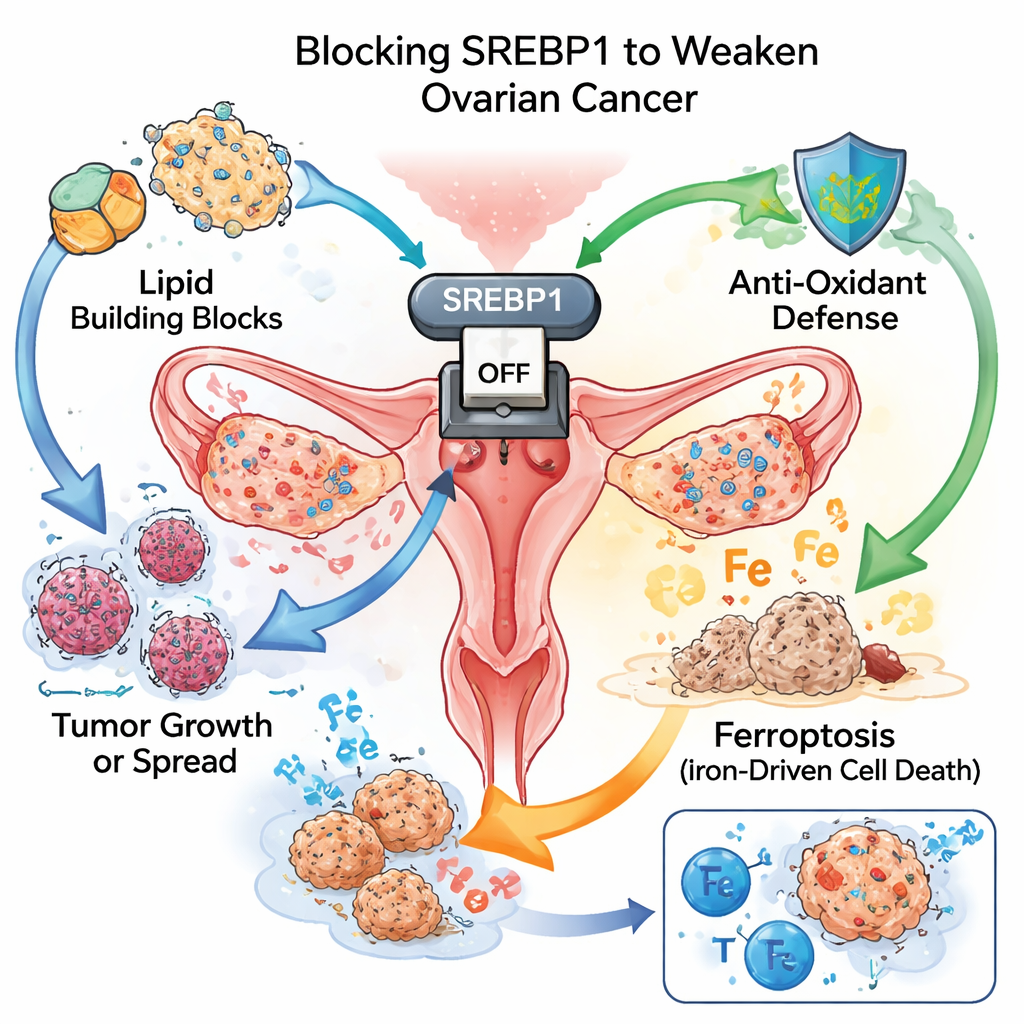
En huvudbrytare för tumörens bränsle
Liksom snabbväxande ogräs behöver cancerceller enorma mängder byggstenar och energi. Ett sätt de möter detta behov är genom att omprogrammera hur de tillverkar och använder fetter. Teamet fokuserade på SREBP1, ett protein som fungerar som en huvudbrytare för fettproduktion. I vävnadsprover från mer än hundra patienter hade äggstockstumörer mycket högre nivåer av SREBP1 än intilliggande normal vävnad. Kvinnor vars tumörer visade starkare SREBP1-färgning tenderade att ha mer aggressiv sjukdom och kortare överlevnad, vilket markerar detta protein både som en drivkraft för progression och ett varningstecken för dålig prognos.
Bromsa tillväxt och spridning genom att stänga av fettet
I äggstockscellinjer odlade i laboratoriet minskade nedreglering av SREBP1 kraftigt cellernas förmåga att föröka sig och bilda kolonier. Cellerna fastnade i specifika stadier av cellcykeln, vilket innebar att de inte längre kunde dela sig effektivt. Forskarna såg också färre tecken på rörelse och invasion: scratch‑ och Transwell‑tester visade att celler med mindre SREBP1 hade försämrad migrationsförmåga, och viktiga markörer för en formförändrande process kallad EMT skiftade tillbaka mot ett mer ”normalt” tillstånd. Samtidigt sjönk mätvärden för triglycerider och kolesterol, och färgning visade färre lipidkorn inuti cellerna, vilket bekräftar att deras interna fettproducerande maskineri hade nedreglerats.
Utlösa en järndriven celldöd
Det mest slående resultatet av att blockera SREBP1 var aktiveringen av ferroptos, en nyligen erkänd form av celldöd driven av järn och peroxidering (rostning) av cellmembran. Endast en ferroptoshämmare, och inte inhibitorer av andra dödsvägar, kunde rädda SREBP1‑tystade celler, vilket pekar på ferroptos som den huvudsakliga orsaken till deras undergång. Kemiska tester visade fler nedbrytningsprodukter från oxiderade fetter, mindre antioxidant glutation och högre nivåer av reaktiva lipidmolekyler. Två proteiner som normalt skyddar celler från ferroptos, kallade xCT och GPX4, var starkt minskade när SREBP1 slogs ned, vilket tog bort ett avgörande skyddsbuffer mot denna destruktiva process.
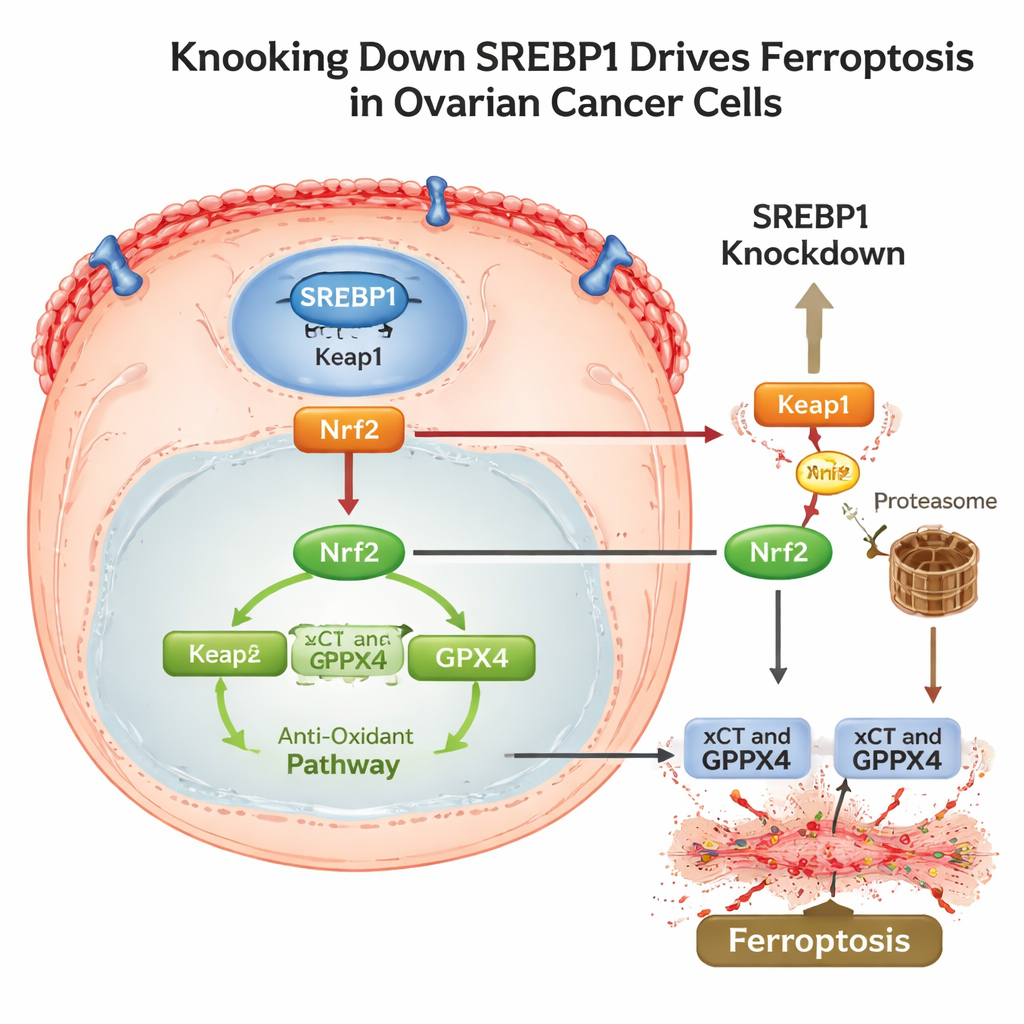
Avväpna cellens antioxidativa sköld och undanflykter
För att förstå hur SREBP1 kopplar till detta dödsprogram spårade forskarna en bana via ett annat stort stressresponssystem, proteinet Nrf2. Under normala förhållanden hjälper Nrf2 celler att överleva genom att slå på antioxidativa gener, inklusive xCT och GPX4. Studien fann att sänkning av SREBP1 ökade nivåerna av Keap1, ett protein som märker Nrf2 för nedbrytning, vilket ledde till mer nedbrytning av Nrf2 och mindre av det kunde nå kärnan. När Nrf2 minskade försvagades dess downstream‑försvar och ferroptos följde. Viktigt är att SREBP1‑rika tumörer också visade högre nivåer av PD‑L1, ett ytprotein som hjälper cancerceller att gömma sig från angripande T‑celler. När SREBP1 tystades i musmodeller växte tumörerna långsammare, visade mer tecken på lipidskador, mindre Nrf2 och GPX4 samt lägre PD‑L1, tillsammans med ökad immunaktivitet.
Varför detta är viktigt för framtida behandlingar
Kort sagt verkar äggstockstumörer använda SREBP1 som ett tveeggat överlevnadsverktyg: det matar deras tillväxt genom att öka fettproduktionen och utrustar dem samtidigt med en antioxidant sköld och ett immunologiskt kamouflage. Detta arbete visar att avstängning av SREBP1 kan svälta tumören på lipider, ta bort dess skydd mot järndriven skada och minska dess förmåga att undkomma immunangrepp. Det gör SREBP1 till ett attraktivt mål för nya läkemedel och tyder på att kombinera SREBP1‑hämmare med behandlingar som utlöser ferroptos eller frigör immunsystemet kan ge patienterna effektivare, mer långvarig kontroll över sjukdomen.
Citering: Nie, R., Zhou, H., Chen, L. et al. SREBP1 knockdown triggers ferroptosis by suppressing the Nrf2-XCT/GPX4 axis in ovarian cancer. Cell Death Discov. 12, 101 (2026). https://doi.org/10.1038/s41420-026-02964-9
Nyckelord: äggstockscancer, lipidmetabolism, ferroptos, SREBP1, tumörimmunitet