Clear Sky Science · sv
PDHA1 ökar motståndskraften mot ferroptos vid anoikis-resistent prostatacancer genom uppreglering av AIFM2
Varför vissa prostatacancerceller vägrar att dö
När cancerceller lossnar från en tumör och kommer in i blodbanan borde de flesta dö innan de når ett nytt organ. Ändå överlever en farlig minoritet, reser vidare och grundar metastaser som ofta är dödliga. Denna studie ställer en central fråga: vad gör att vissa prostatacancerceller motstår en form av celldöd som normalt inträffar när de förlorar kontakten med sitt ursprungliga vävnadsunderlag? Genom att avslöja en dold överlevnadskrets i dessa celler pekar forskningen på nya sätt att blockera metastasering vid dess källa.
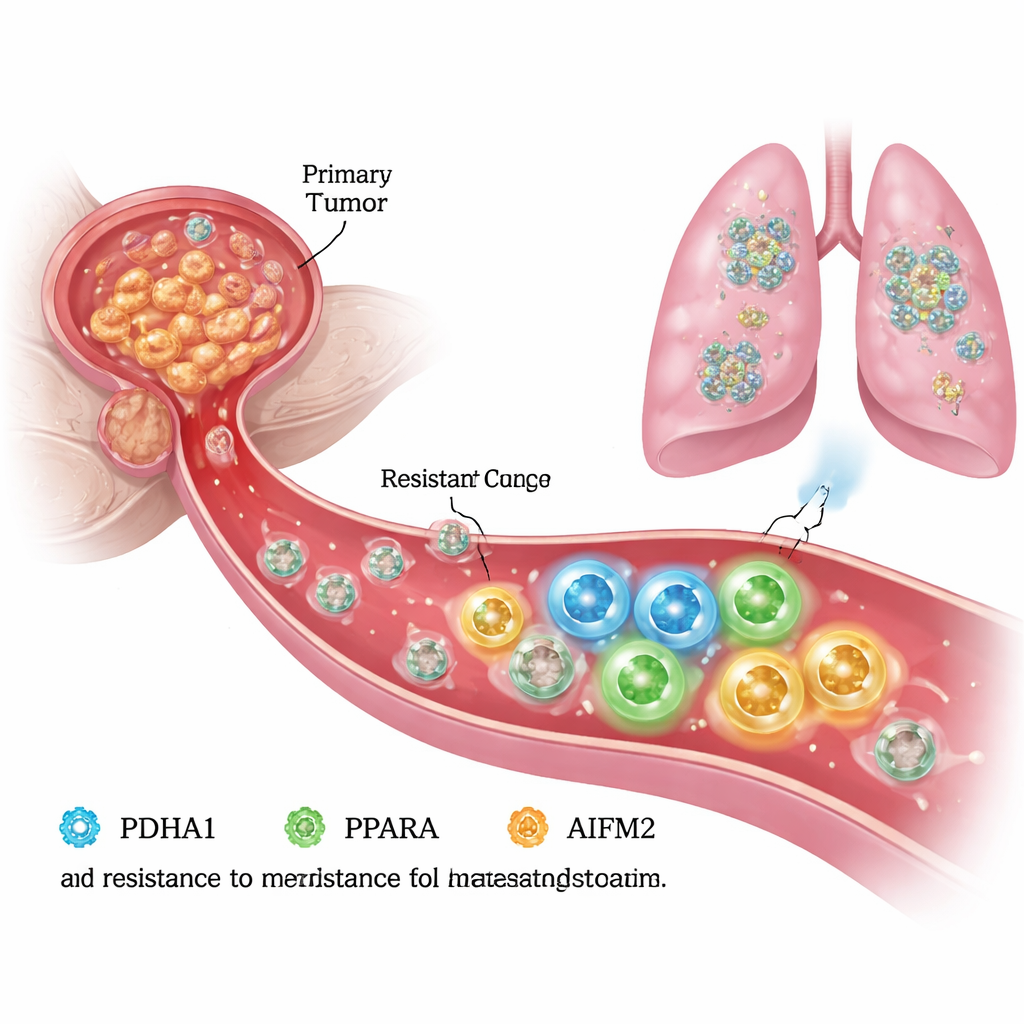
Att undkomma döden i blodomloppet
För att sprida sig måste prostatacancerceller klara livet utan stöd från den omgivande vävnaden, den extracellulära matrisen. Under dessa ”frikopplade” förhållanden genomgår friska celler en programmerad död som kallas anoikis, och många cancerceller är också sårbara för en närbesläktad järnberoende dödsprocess kallad ferroptos. Författarna framställde i laboratoriet anoikis-resistenta prostatacancerceller och jämförde dem med sina ursprungliga ”parental”-celler. De fann att de resistenta cellerna inte bara migrerade och invaderade aggressivare, utan också överlevde bättre under frikoppling, vilket tyder på att de hade omkopplat sin inre mekanik för att undvika ferroptos och fortsätta växa.
En metabolisk växling med ett andra uppdrag
Vid en närmare granskning fokuserade teamet på ett metabolt enzym kallat PDHA1, mest känt för att hjälpa celler omvandla sockeravledet pyruvat till acetyl-CoA i mitokondrierna och därigenom driva energiproduktion. I de anoikis-resistenta cellerna var PDHA1-nivåerna och aktiviteten markant högre, och patientprover visade mer PDHA1 i primära tumörer från män vars prostatacancer spridit sig till lymfkörtlar eller avlägsna platser. När forskarna minskade PDHA1 förlorade de resistenta cellerna mycket av sin förmåga att röra sig, invadera och överleva. Överraskande nog var en betydande del av PDHA1 i dessa celler inte längre begränsad till mitokondrierna; den hade flyttat in i cellkärnan, där DNA paketeras med histoner som kan kemiskt modifieras för att slå på eller av gener.
Att skriva om genaktivitet för att blockera ferroptos
Inne i kärnan verkade PDHA1 driva lokal produktion av acetyl-CoA, en viktig byggsten för histonacetylering. Författarna visade att kärn-PDHA1 ökade en specifik markör, H3K9-acetylering, i kontrollregionen för en gen kallad PPARA. Denna förändring fungerade som att lossa kromatinets ”spolar”, vilket gjorde det lättare att slå på PPARA. PPARA fungerade i sin tur som en huvudströmbrytare som ökade produktionen av ett annat protein, AIFM2, genom att binda till dess promotor och höja dess transkription. Istället för att direkt reglera AIFM2-genen arbetade PDHA1 alltså via PPARA och etablerade en flerstegs-väg från förändrad metabolism till förändrad genreglering.
Att bygga en sköld mot järninducerad skada
AIFM2 är känt som en intern broms på ferroptos: det hjälper till att skydda fetter i cellmembranen från förödande oxidation. I de resistenta prostatacancercellerna höjde PDHA1-uppreglering AIFM2-nivåerna, medan PDHA1-nedtystning sänkte dem. Funktionella tester visade att minskad PDHA1 förvärrade kännetecken för ferroptos—mer reaktiva syrearter, mer lipidoxidation, lägre mitokondriellt membranpotential och karakteristisk mitokondrie-förminskning—särskilt när cellerna utsattes för det ferroptos-inducerande läkemedlet erastin. Överuttryck av AIFM2 återställde dessa effekter, räddade cellöverlevnad i rätter och återställde lungmetastaser i möss, även när PDHA1 var hämmat. Detta bekräftade att AIFM2 är en kritisk downstream-effektor för PDHA1-drivet motstånd mot ferroptos.
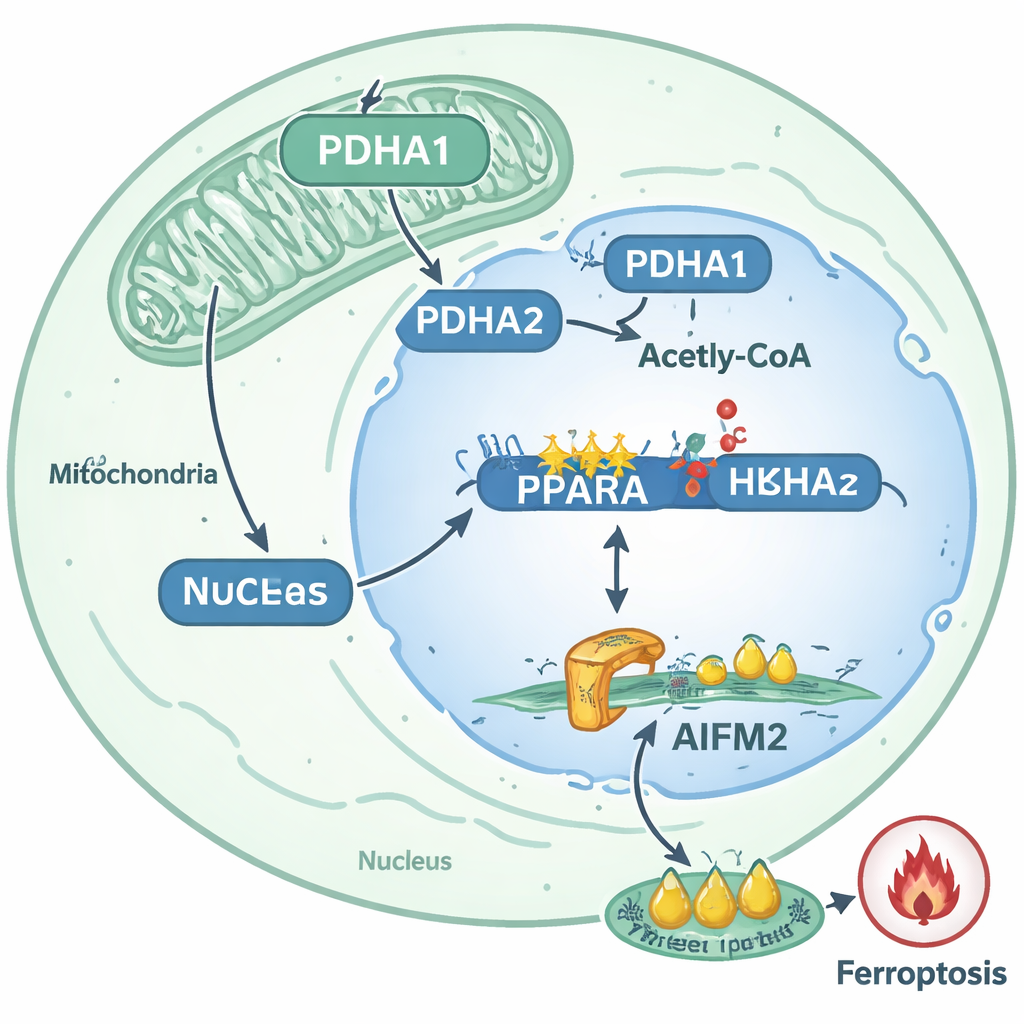
Från molekylär krets till behandlingsidéer
Genom att kartlägga dessa händelser beskriver studien en tydlig väg genom vilken frikopplade prostatacancerceller blir svårare att döda: PDHA1 flyttar in i kärnan, ökar histonacetylering vid PPARA-genen, förstärker PPARA-aktivitet och höjer därigenom AIFM2-nivåerna för att blockera ferroptos. Denna bana är starkt kopplad till metastatisk beteende i patienttumörer och i djurmodeller. För icke-specialister är slutsatsen att vissa cancerceller återanvänder ett normalt metabolt enzym som ett epigenetiskt verktyg som skriver om genaktivitet och bygger en biokemisk sköld mot en kraftfull form av celldöd. Författarna föreslår att läkemedel som riktar sig mot PDHA1, PPARA eller AIFM2—eller terapier som avsiktligt utlöser ferroptos—en dag skulle kunna kombineras för att beröva metastatiska prostatacancerceller denna överlevnadsfördel och göra dem mycket mer sårbara under deras mest utsatta resa: hoppet från ett organ till ett annat.
Citering: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
Nyckelord: prostatacancer metastasering, ferroptos, anoikis-resistens, PDHA1, AIFM2