Clear Sky Science · sv
Kolorektal cancers härledda osteopontin omprogrammerar makrofager till ett pro-metastatiskt M2-tillstånd via PI3K/AKT/CSF1-CSF1R-axeln
Varför detta är viktigt för personer med tjock- och ändtarmscancer
De flesta dödsfall vid kolorektal (tjock- och ändtarms) cancer orsakas inte av den ursprungliga tumören utan av dess spridning till andra organ. Denna studie undersöker hur cancerceller "pratar" med närliggande immunceller för att underlätta tumörspridning. Genom att avslöja ett nyckelbudskap som cancerceller skickar för att omprogrammera immunceller till medhjälpare snarare än kämpar pekar arbetet på nya behandlingsstrategier som kan bromsa eller stoppa metastasering vid avancerad kolorektal cancer.
Ett klibbigt protein med en mörk sida
Forskarna fokuserade på ett protein som kallas osteopontin, eller OPN, som produceras både av cancerceller och av vissa immunceller i tumörer. OPN har länge kopplats till sämre utfall i många cancerformer, men exakt hur det gynnar spridning vid kolorektal cancer var oklart. Genom att analysera stora patientdatabaser och tumörprover fann teamet att OPN-nivåerna var mycket högre i kolorektalt tumörvävnad än i normal tarmvävnad, särskilt hos patienter med avancerad sjukdom och avlägsna metastaser. Patienter vars tumörer uppvisade högre OPN hade i allmänhet sämre överlevnad, vilket tyder på att OPN är nära förknippat med aggressiv, svårbehandlad cancer.
Det är inte bara cancercellerna i sig
Överraskande nog, när forskarna tvingade kolorektala cancerceller i laboratoriet att producera mer eller mindre OPN blev cellerna inte i sig mer invasiva eller mobila. Deras tillväxt, migration och förmåga att tränga igenom konstgjorda membran förändrades mycket lite. Det utmanade den vanliga idén att OPN huvudsakligen verkar genom att direkt stärka cancercellernas egna aggressivitet. Istället riktade teamet in sig på tumörens omgivning – det så kallade tumörmikromiljön – särskilt en grupp immunceller kallade makrofager, som antingen kan attackera tumörer (ett “M1”-tillstånd) eller stödja dem (ett “M2”-tillstånd).
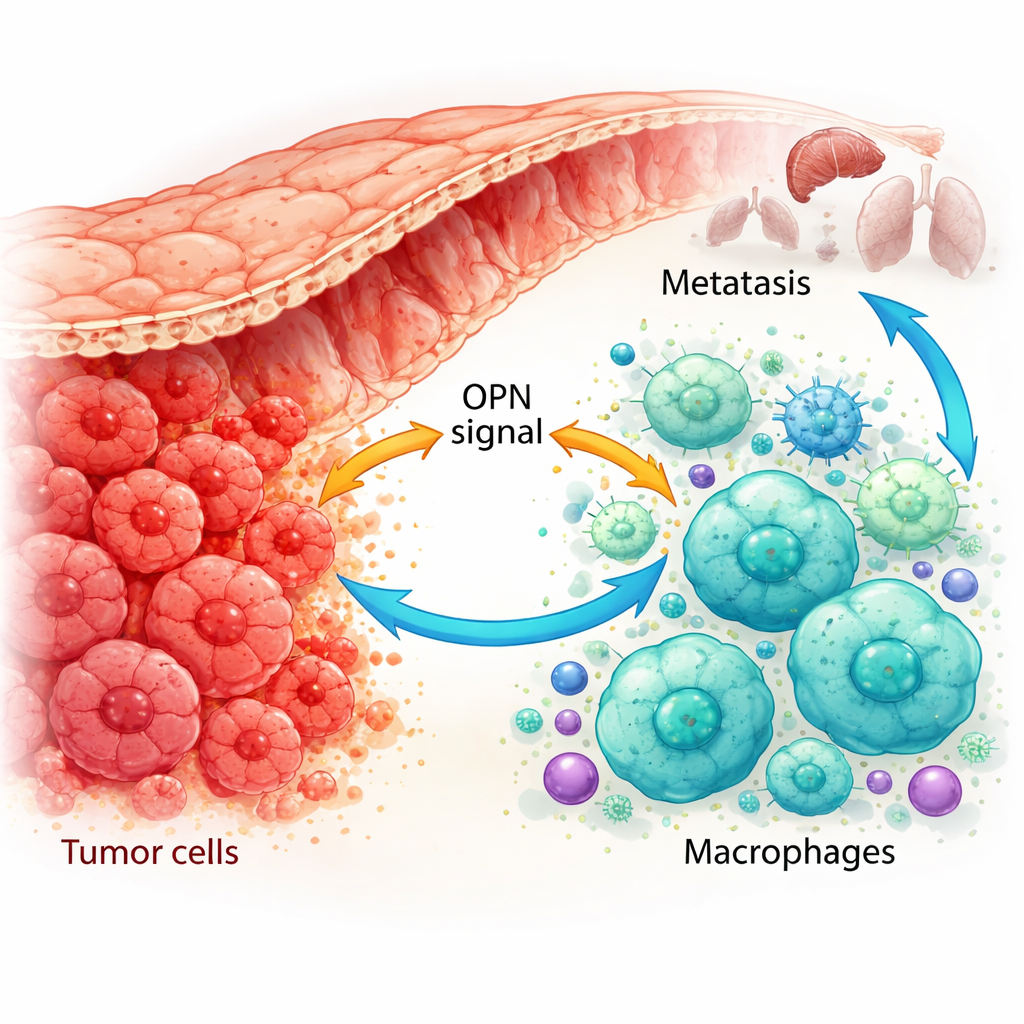
Hur immunceller omprogrammeras till tumörhjälpare
Genom att använda single-cell-genetiska kartor och avancerad färgning av patientvävnader visade forskarna att OPN produceras inte bara av cancerceller utan också av tumörassocierade makrofager. I tumörer som redan hade spridit sig var både cancerceller och en specifik undertyp av makrofager rika på OPN. Dessa makrofager tenderade att vara i ett M2-likt, tumörstödjande tillstånd och var mer talrika när tumörens OPN-nivåer var höga. I musemodeller drogs tumörer som konstruerats för att producera mer OPN till sig fler av dessa M2-lika makrofager och växte snabbare, medan tumörer med minskad OPN hade färre M2-makrofager och växte långsammare. Detta tyder på att OPN är en potent rekryterare och omprogrammerare av makrofager i tumörmiljön.
Den dolda signaleringskedjan: från OPN till metastas
För att kartlägga den molekylära händelsekedjan odlade teamet humana makrofager tillsammans med kolorektala cancerceller som producerade olika mängder OPN. De fann att cancerceller med höga OPN-nivåer drev makrofager mot M2-tillståndet och uppmuntrade en tvåvägsrörelse: makrofager migrerade mot tumören, och tumörceller blev mer invasiva som svar på signaler från dessa makrofager. Vidare upptäckte forskarna att OPN aktiverar en signalväg inne i makrofager som kallas PI3K/AKT. Denna aktivering får i sin tur makrofager att frisätta stora mängder av en annan molekyl, CSF1, och öka uttrycket av dess receptor, CSF1R, på sin yta. CSF1 agerar sedan i en loop för att ytterligare befästa M2-, pro-metastatiska tillståndet och fortsätta dra makrofager in i tumören.
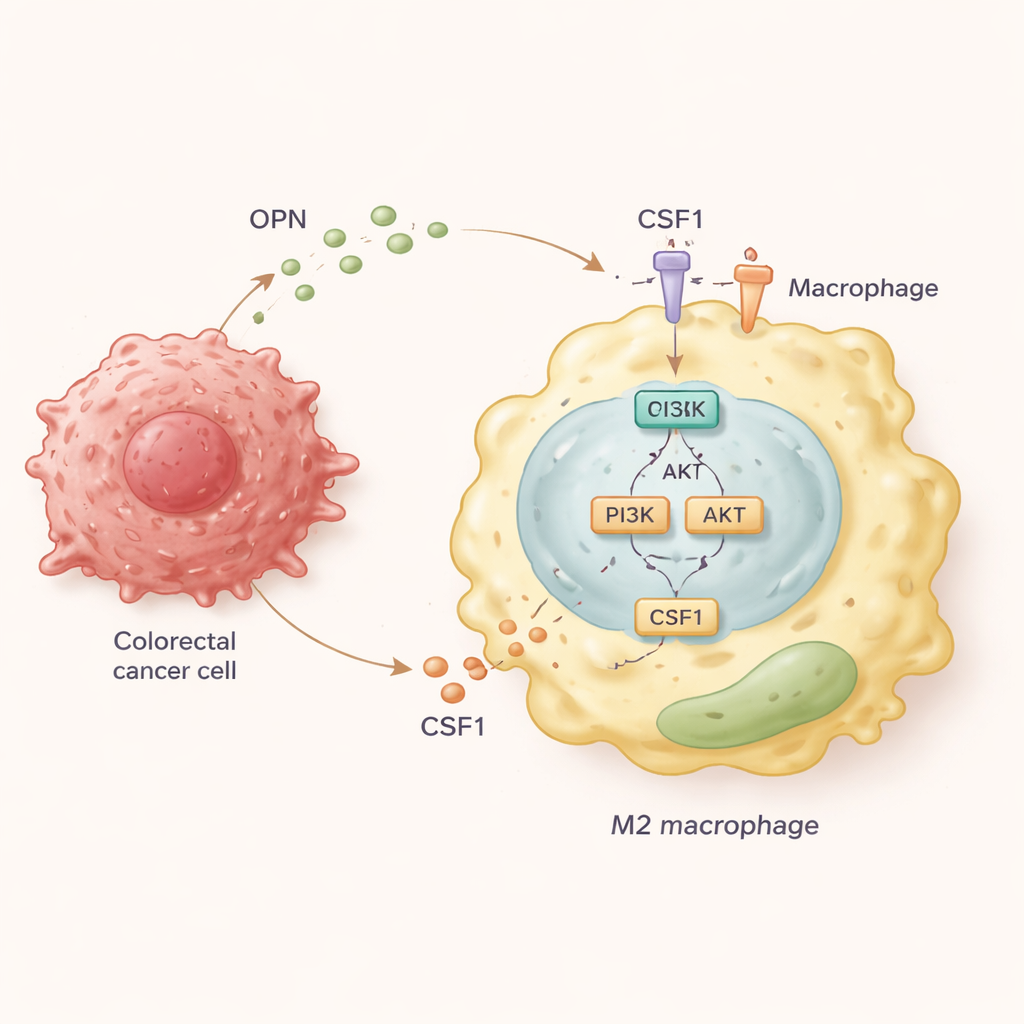
Blockera loopen för att bromsa spridning
I musemodeller av kolorektal cancer som spridit sig i buken testade forskarna ett CSF1R-blockerande läkemedel kallat PLX3397. Möss med OPN-höga tumörer utvecklade många metastatiska noduli, men behandling med CSF1R-hämmaren minskade signifikant både antalet metastaser och förekomsten av M2-lika makrofager i tumörerna. Tumörceller visade mindre tillväxt och fler tecken på programmerad celldöd. Viktigt är att läkemedlet främst utarmade de tumörfrämjande makrofagerna utan att i hög grad påverka den mer inflammatoriska typen, vilket tyder på ett relativt riktat sätt att försvaga tumörens stödsystem.
Vad detta betyder för framtida behandlingar
För en lekmannapublik är huvudbudskapet att vissa kolorektala cancerformer lyckas sprida sig inte bara för att cancercellerna är aggressiva, utan för att de kapar närliggande immunceller och gör dem till medbrottslingar. I denna studie fungerar cancercellsderiverat OPN som en huvudströmbrytare som omprogrammerar makrofager via PI3K/AKT- och CSF1/CSF1R-signalvägen och skapar en bördig mark för metastaser. Genom att bryta denna kedja – särskilt vid CSF1R-steget – kunde forskarna minska tumörspridning i möss. Det tyder på att mätning av OPN-nivåer kan hjälpa till att identifiera patienter som kan dra nytta av läkemedel som riktar sig mot makrofager, och att kombinera sådana läkemedel med befintliga behandlingar eller immunoterapier kan ge nytt hopp för personer med avancerad kolorektal cancer.
Citering: Liang, X., Qin, F., Yuan, Z. et al. Colorectal cancer-derived osteopontin rewires macrophages into a pro-metastatic M2 state via the PI3K/AKT/CSF1-CSF1R axis. Cell Death Discov. 12, 92 (2026). https://doi.org/10.1038/s41420-026-02945-y
Nyckelord: kolorektal cancer, osteopontin, tumörassocierade makrofager, metastas, CSF1R-hämning