Clear Sky Science · sv
Rottlerin utlöser dubbel nedbrytning av SLC7A11 och GPX4 för att driva ferroptos och känsliggöra vid hepatocellulärt karcinom
Varför denna naturliga förening är viktig för levercancer
Hepatocellulärt karcinom, den vanligaste formen av primär levercancer, upptäcks ofta sent och är fortsatt svårt att behandla. Den här studien undersöker om ett växt‑härlett molekylärt ämne kallat rottlerin, länge känt för sina breda anticancer‑effekter, kan utnyttjas för att utlösa en nyare form av celldöd kallad ferroptos i levercancerceller. Genom att förstå hur rottlerin verkar på molekylär nivå hoppas forskarna öppna nya vägar för mer effektiva behandlingar som är svårare för tumörer att motstå.
Ett nytt sätt att döda cancerceller
Traditionella anticancerläkemedel skjuter vanligtvis tumörceller in i välkända dödsprogram som apoptos. Ferroptos skiljer sig: det är en järnavhängig process som drivs av uppbyggnad av toxiska fetter i cellmembran. Levercancerceller är särskilt sårbara för denna typ av skada eftersom de i hög grad förlitar sig på antioxidativa system för att hålla dessa fettbaserade toxiner i schack. Forskarna frågade om rottlerin kunde sabotera dessa försvar och därigenom tvinga levercancerceller in i ferroptos.
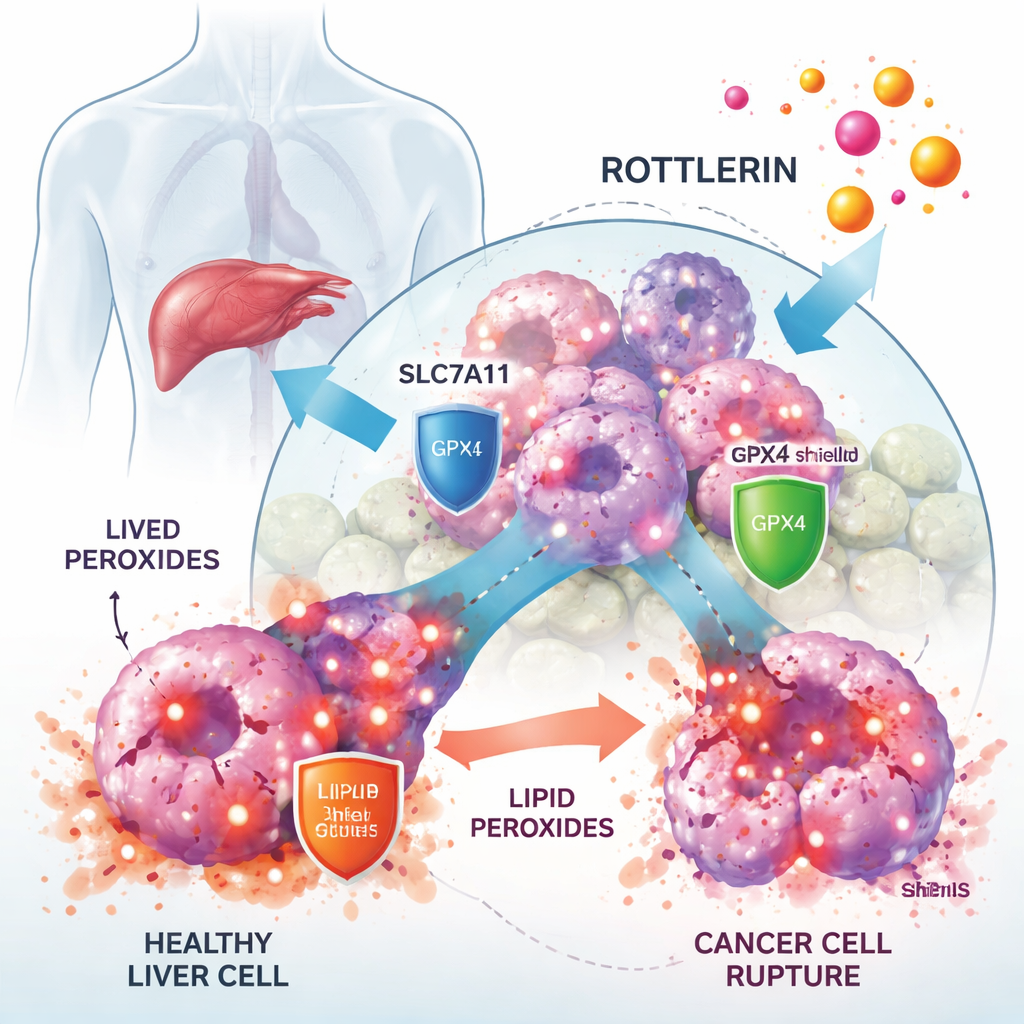
Hur rottlerin bromsar tumörtillväxt
Genom att arbeta med humana levercancercellinjer visade forskarna att rottlerin kraftigt minskade cancercellernas tillväxt vid låga mikromolära doser, medan normala leverrelaterade celler påverkades mindre. När de tillsatte en specifik ferroptos‑blockerare kallad Ferrostatin‑1 räddades mycket av den rottlerin‑inducerade celldöden, vilket starkt tyder på att ferroptos var huvudmekanismen för dödandet. Mikroskopi och biokemiska tester stödde detta: rottlerin‑behandlade celler ackumulerade höga nivåer lipidperoxider, visade förändrade mitokondrier och uppvisade minskade mängder av antioxidationsmolekylen glutation, alla kännetecken för ferroptos.
Avväpna cellernas antioxidant‑sköldar
Levercancerceller överlever genom att luta sig mot en kritisk försvarsaxel uppbyggd av transportören SLC7A11 och enzymet GPX4. SLC7A11 importerar cystin, en byggsten för glutation, medan GPX4 använder glutation för att neutralisera lipidperoxider innan de skadar membranen. Studien fann att rottlerin orsakade att både SLC7A11‑ och GPX4‑proteinnivåer minskade över tid. Detta berodde inte på att cellerna slutade tillverka dem, utan på att proteinerna markerades med små ”förstör mig”‑taggar (ubiquitin) och matades in i cellens protein‑nedbrytande maskineri, proteasomen. Blockering av proteasomen vände denna förlust, och konstgjord överuttryck av SLC7A11 eller GPX4 i cellerna skyddade dem delvis mot rottlerin. Tillsammans visar dessa fynd att rottlerin fungerar som en dubbel degraderare av två centrala ferroptosförsvar.
Förstärka befintliga läkemedel mot levercancer
Många patienter med avancerad levercancer får sorafenib, ett standardläkemedel i första linjen som i sig kan inducera ferroptos, men resistens begränsar ofta dess nytta. Författarna testade om låga, i övrigt svaga doser av rottlerin kunde göra tumörceller mer känsliga för ferroptos‑inducerande läkemedel som sorafenib och RSL3. I cellkultur ökade kombinationen av lågdos‑rottlerin med antingen läkemedel avsevärt cancercelldöd och försköt dos–svarskurvor, vilket indikerar ökad potens. Viktigt är att denna sensibiliserande effekt bestod även när det klassiska rottlerin‑målproteinet PKCδ genetiskt minskades, vilket visar att huvudverkan inte gick via denna kinas utan snarare genom nedbrytning av SLC7A11 och GPX4. I musemodeller med humana levertumörer bromsade kombinationsbehandling med rottlerin och sorafenib tumörtillväxten mer än sorafenib ensam och sänkte ytterligare SLC7A11‑ och GPX4‑nivåerna i tumörerna.
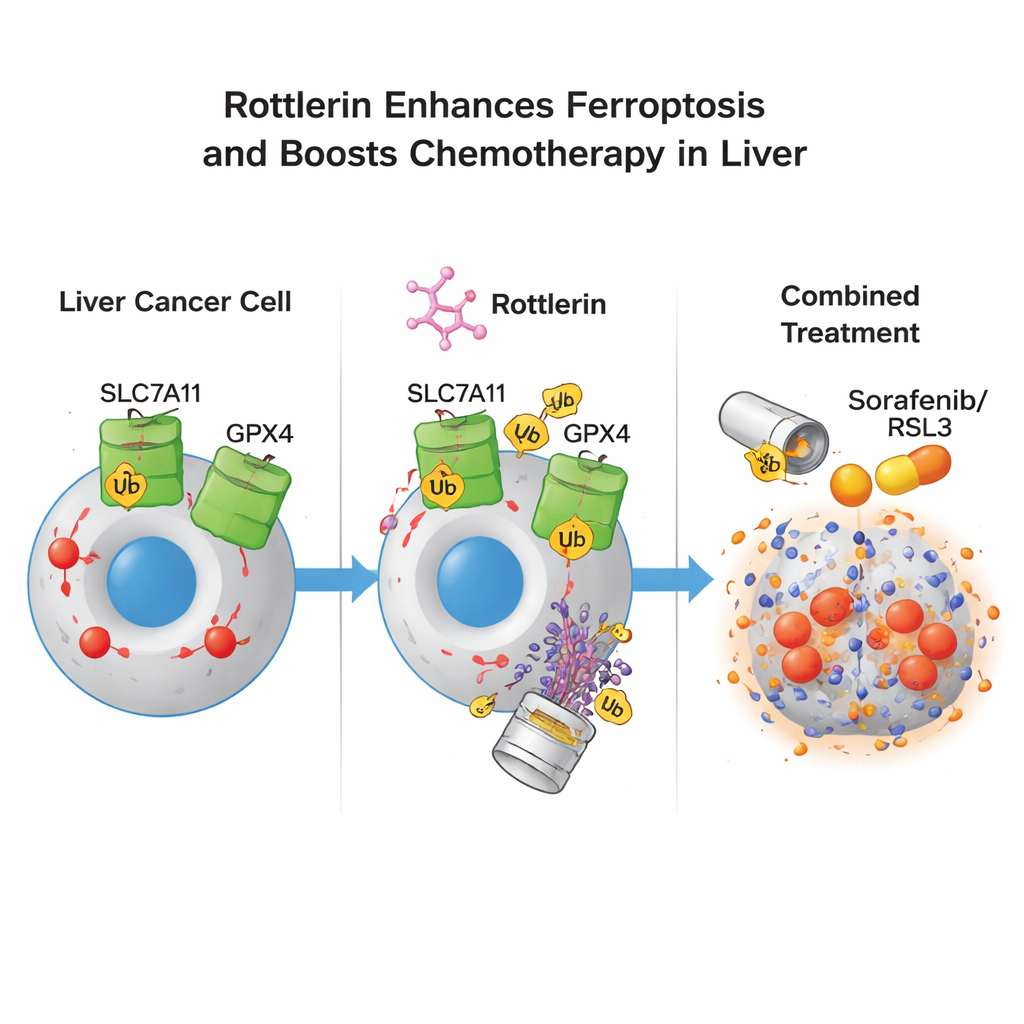
Vad detta kan innebära för framtida behandlingar
För icke‑specialister är budskapet att rottlerin verkar som ett ”två‑låspass” på levercancerceller: det tar samtidigt bort två avgörande lås—SLC7A11 och GPX4—som normalt skyddar celler från en dödlig våg av fettbaserad oxidation. När dessa lås är borta blir cancerceller mycket mer benägna att genomgå ferroptos, särskilt i kombination med befintliga läkemedel som trycker dem i den riktningen. Även om mer arbete krävs innan rottlerin eller relaterade föreningar kan användas på patienter, erbjuder denna strategi med dubbel degradering ett lovande sätt att överlista de adaptiva försvar som ofta gör levertumörer så svåra att behandla.
Citering: Luo, H., Jin, X., Gao, C. et al. Rottlerin triggers dual degradation of SLC7A11 and GPX4 to drive ferroptosis and chemosensitization in hepatocellular carcinoma. Cell Death Discov. 12, 89 (2026). https://doi.org/10.1038/s41420-026-02942-1
Nyckelord: levercancer, ferroptos, rottlerin, SLC7A11, GPX4