Clear Sky Science · sv
Aktivering av GCN2 och därefter det veckade proteinsvar (UPR) med den lilla orala molekylen NXP800 fördröjer tumörtillväxt i osteosarkom
Göra cancerens stress till en svaghet
Osteosarkom är en sällsynt men aggressiv bencancer som främst drabbar barn och unga vuxna. I årtionden har behandling byggt på intensiv cytostatika och kirurgi, men överlevnaden för patienter med avancerad sjukdom har knappt förbättrats. I den här studien undersöks en ny tablett, kallad NXP800, som syftar till att utnyttja en dold svaghet hos cancerceller: deras ständiga kamp med inre stress. Genom att driva denna stress förbi en brytpunkt kan NXP800 tvinga tumörceller att självdö samtidigt som de flesta friska celler skonas.
En svårbehandlad bencancer i behov av nya alternativ
Osteosarkom växer vanligtvis i långa rörben i armar och ben och kan snabbt sprida sig till lungorna. Standardbehandling kombinerar flera kraftfulla cytostatika med operation för att avlägsna tumören. Medan denna strategi botar många patienter med lokaliserad sjukdom är prognosen dålig för dem vars tumörer återkommer eller redan har spridit sig vid diagnos. Eftersom de nuvarande läkemedlen nått sina begränsningar söker forskare terapier som angriper osteosarkom på helt nya sätt, helst genom att rikta in sig på egenskaper som skiljer cancerceller från normalt vävnad.
Få stressen att verka mot tumörcellerna
Cancerceller lever under ständig press. De delar sig snabbt, förbrukar stora mängder energi och syre och utsätts ofta för hårda förhållanden som låg syrehalt eller exponering för cytostatika. För att hantera detta förlitar de sig på nödsystem som hjälper dem att vika och bearbeta proteiner korrekt och att justera sin ämnesomsättning. Ett av dessa system kallas det veckade proteinsvaret (unfolded protein response), som triggas när cellens proteinfabrik, det endoplasmatiska nätverket, är överbelastad. Ett annat system, det integrerade stresssvaret, känner av olika typer av stress och sänker proteinproduktionen. Normalt hjälper dessa vägar cancerceller att överleva — men om de pressas för hårt under för lång tid kan de växla från att skydda cellen till att utlösa dess död.
NXP800 slår mot en nyckel i stresskänningen
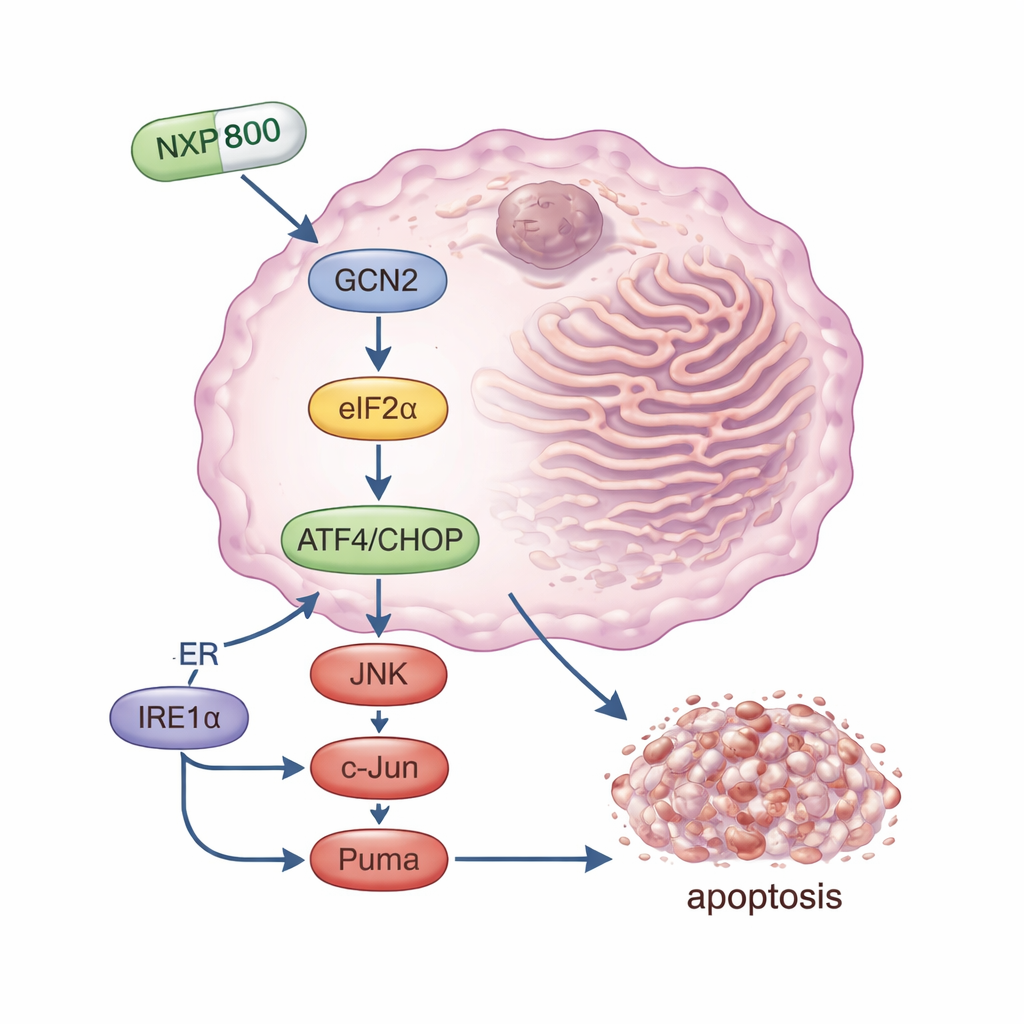
NXP800 är en oral liten molekyl som ursprungligen utvecklades för att blockera en heat shock‑väg som är involverad i cancertillväxt. I denna studie fann forskarna att dess huvudeffekt i osteosarkomceller är annorlunda: den aktiverar starkt ett stresskännande protein kallat GCN2. När GCN2 slås på modifierar det en annan faktor, eIF2α, vilket snabbt minskar den totala proteinproduktionen samtidigt som nivåerna av specifika stress‑"mästare", särskilt proteinet ATF4 och dess partner CHOP, ökar. Tillsammans driver dessa molekyler cellen mot programmerad död. Teamet visade att när de blockerade GCN2 — antingen genom att tysta dess gen eller med en separat hämmare — kunde NXP800 inte längre effektivt utlösa denna kedjereaktion, och cancercellerna blev mycket mindre känsliga för läkemedlet. Detta pekar ut GCN2 som ett avgörande mål för NXP800 i osteosarkom.
Aktivering av flera dödsvägar i tumören
Utöver GCN2‑armen i stressnätverket aktiverade NXP800 också en annan bana kopplad till celldöd. Det slog på en sensor kallad IRE1α, som i sin tur stimulerade signalproteinerna JNK och c‑Jun. Denna gren är känd för att främja produktionen av Puma, en potent dödsfrämjande molekyl som skadar cellens interna överlevnadsmekanismer. I laboratorieförsök hämnade NXP800 osteosarkomcellernas tillväxt, stoppade deras cellcykel och aktiverade enzymer och proteinförändringar som kännetecknar apoptos, det kontrollerade celldödsprogrammet. Viktigt är att normala benrelaterade stamceller påverkades mycket mindre, vilket tyder på en viss selektivitet för tumörceller som redan lever på gränsen för tolererbar stress.
Från labb bänk till levande modeller
För att se om dessa cellulära effekter översattes till verklig tumörkontroll testade forskarna NXP800 i möss med mänskliga osteosarkomceller implanterade nära tibia. Möss som fick NXP800 peroralt utvecklade tumörer som växte avsevärt långsammare och vid studiens slut var ungefär hälften så stora som tumörerna i obehandlade möss. Tumörprover från behandlade djur visade tydliga tecken på läkemedlets verkningsmekanism: högre nivåer av stressmarkörer såsom eIF2α och ATF4, färre celler i aktiv delning och fler celler som genomgick apoptos. Separata säkerhetsstudier i friska möss visade ingen större organskada och leverprover förvärrades inte, vilket stöder en hanterbar säkerhetsprofil vid de använda doserna.
Vad detta kan innebära för patienter
Tillsammans visar detta arbete att NXP800 kan fördröja osteosarkomtillväxt genom att avsiktligt överaktivera cancercellens egna stressförsvar tills de utlöser självdöd. Genom att rikta in sig på stressens sensor GCN2 och relaterade vägar erbjuder läkemedlet ett helt nytt sätt att försvaga tumörer som varit resistenta mot traditionell cytostatika. Eftersom NXP800 redan testas i tidiga kliniska prövningar för andra cancerformer öppnar dessa resultat möjligheten att omlokalisera det för osteosarkom, antingen ensamt eller i kombination med befintliga läkemedel. Medan humana prövningar krävs för att bekräfta nytta och säkerhet, ger studien ett övertygande proof‑of‑principle: att vända cellstress mot tumören kan öppna ett nytt behandlingskapitel för patienter med denna svårbehandlade bencancer.
Citering: Racineau, E., Lallier, M., Postec, A. et al. Activating GCN2 and subsequently the Unfolded Protein Response with the small oral molecule NXP800 delays tumor growth in osteosarcoma. Cell Death Discov. 12, 94 (2026). https://doi.org/10.1038/s41420-026-02941-2
Nyckelord: osteosarkom, NXP800, stressrespons, GCN2‑väg, apoptos