Clear Sky Science · sv
Förlust av DIAPH3 påskyndar gliombildning hos möss
Varför denna studie av hjärnan är viktig
Glioblastom är en av de dödligaste hjärntumörerna, och trots kirurgi, strålning och kemoterapi överlever de flesta patienter knappt mer än ett år. Denna studie ställer en grundläggande men avgörande fråga: vilka tidiga förändringar inne i hjärnceller driver dem mot att bli så aggressiva tumörer, och varför är dessa tumörer så svåra att slå ut med strålning? Genom att följa ett enda strukturellt protein i musens hjärnceller visar forskarna hur dess förlust destabiliserar kromosomer, påskyndar tumörernas uppkomst och hjälper cancerstamliknande celler att klara av strålning som borde förstöra dem.
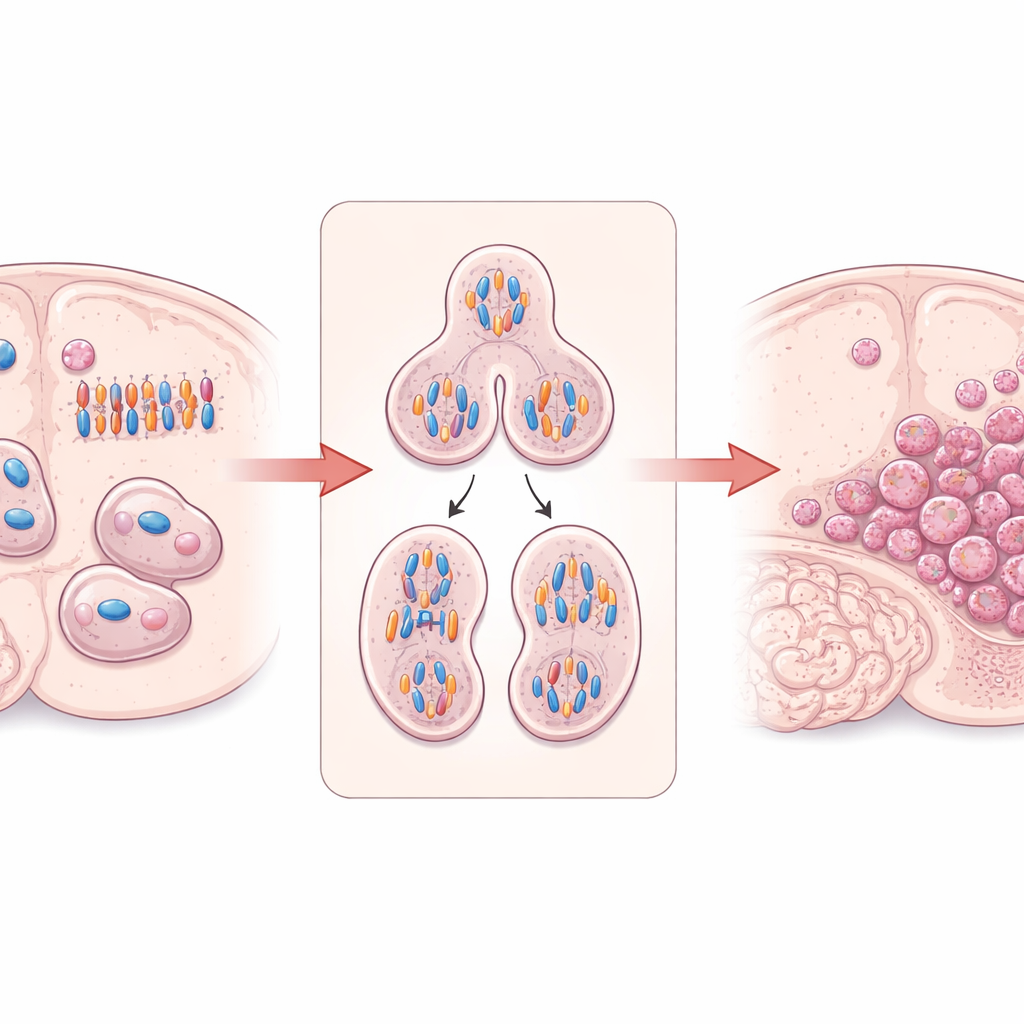
En cellens ”byggare” som håller celldelningen på rätt spår
Arbetet kretsar kring DIAPH3, ett protein som hjälper till att bygga och organisera cellens interna skelett av aktinfilament och mikrotubuli. I delande hjärnstamceller är DIAPH3 avgörande för att bilda en korrekt spindel—strukturen som drar isär duplicerade kromosomer—och för att snöra av en cell i två. Tidigare forskning visade att när DIAPH3 saknas i utvecklande mushjärnor hanterar delande celler ofta kromosomer felaktigt, vilket leder till onormala kromosomantal (aneuploidi), stopp i cellcykeln och celldöd. Intressant nog raderas ofta en liten region på människans kromosom 13 som innehåller DIAPH3-genen i glioblastom, och högre DIAPH3-nivåer har kopplats till bättre överlevnad hos vissa patienter, vilket antyder att detta protein kan fungera som en tumörsuppressor i hjärnan.
Genmodifierade mushjärnor som utvecklar tumörer
För att testa om förlust av DIAPH3 verkligen främjar hjärncancer skapade teamet möss där två gener selektivt kunde raderas i cortexbildande stamceller: Diaph3 och Trp53, den senare kodar för den välkända genomboxens väktare p53. Möss som saknade endast Diaph3 i detta område utvecklade inga tumörer ens efter två år, vilket tyder på att p53 fortfarande kan eliminera starkt avvikande celler. Däremot bildade möss som saknade Trp53 ensamt, eller både Trp53 och Diaph3, så småningom höggradiga diffusa gliom som under mikroskop liknade mänsklig sjukdom. Med upprepade ultrahöga fält-MR-undersökningar visade forskarna att djur som saknade båda generna utvecklade påvisbara tumörer tidigare, och vid medelåldern hade de oftare stora gliom, särskilt i luktbulberna, än möss som saknade endast Trp53. Tumörtillväxthastigheten, när den väl startat, var likartad mellan grupperna—det som förändrades var hur snabbt tumörerna dök upp.
Kromosomkaos och omkopplad genaktivitet
För att förstå varför DIAPH3-förlust snabbar på tumöruppkomst undersökte teamet genaktiviteten i luktbulberna hos unga möss innan några tumörer gick att se. Hos djur som saknade både Diaph3 och Trp53 uttrycktes 126 gener på olika nivåer jämfört med Trp53-enda mutanter, och nästan hälften av dessa hade tidigare kopplingar till cancer. Många förändringar klustrade i signalvägar som driver celltillväxt, migration och blodkärlsbildning, inklusive VEGF, MAPK, RAS, Rap1 och cAMP‑signalering, samt G‑protein‑knyckta receptor‑nätverk. Detta förändrade molekylära landskap antydde att celler tidigt trycktes mot ett cancerliknande tillstånd. Hela genomet‑kopieringsanalys av fullbildade tumörer visade att DIAPH3‑brist inte i hög grad ökade små, fokala DNA‑förändringar utan snarare ökade stora, helkromosom‑vinster och‑förluster—just den aeuploidi som förväntas vid felaktig kromosomsegregering.
Inbyggd DNA‑skada och tuffare cancerstamceller
Aneuploida tumörceller bar mer intern DNA‑skada, påvisad av förhöjda nivåer av DNA‑brottmarkören γ‑H2AX spridd över cellkärnorna. Ändå växte dessa tumörer vidare, vilket antyder att de skaffat sätt att tolerera sådan stress. Vid jämförelse av genuttryck i etablerade tumörer fann forskarna hundratals gener som påverkades av DIAPH3‑förlust, inklusive markant amplification och överproduktion av tillväxtfaktorreceptorn FGFR2 i många dubbelmutanta tumörer. FGFR2 är känt för att stärka DNA‑reparationsmaskineriet i glioblastomceller, och dess aktivering har kopplats till strålningsresistens. Teamet isolerade gliom‑stamliknande celler från musstumörer och testade deras respons på en kliniskt relevant dos joniserande strålning. Före behandling var frekvensen av stamliknande celler likartad i båda genotyperna, men efter bestrålning behöll kulturer från DIAPH3‑defekta tumörer ungefär dubbelt så många aktiva stamliknande celler som de från Trp53‑enda tumörer, vilket visar på ökad radioresistens.
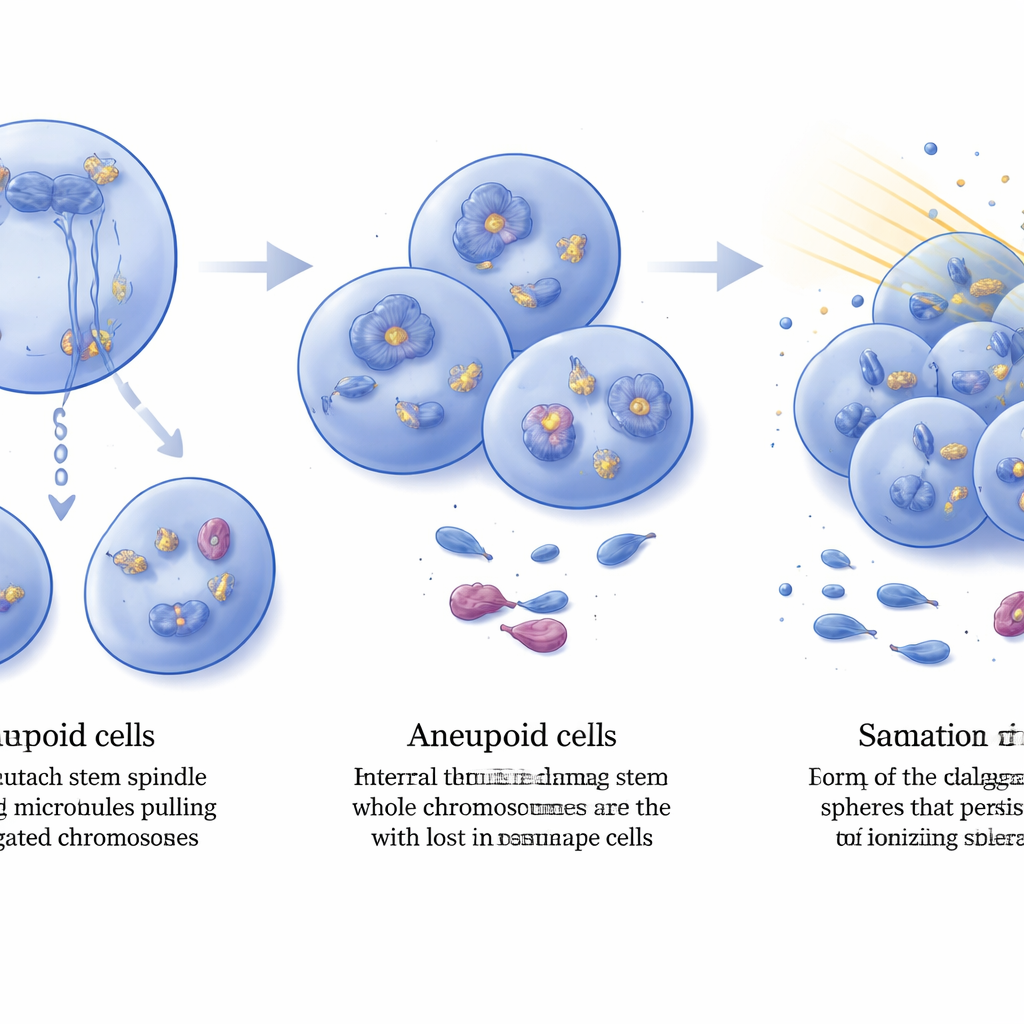
Vad detta betyder för hjärncancer
Sammantaget målar studien upp DIAPH3 som en väktare som hjälper hjärnstamceller att dela sig med rätt antal kromosomer. När både DIAPH3 och p53 saknas blir celldelningen felbenägen, hela kromosomer går förlorade eller vinns, och DNA‑skada ackumuleras. Istället för att dö av detta anpassar sig vissa celler genom att amplifiera reparationskopplade faktorer såsom FGFR2, och omvandlas till aneuploida, höggradiga gliom vars stamliknande celler är ovanligt motståndskraftiga mot strålning. Även om musmodeller inte fångar alla egenskaper hos mänskligt glioblastom stöder dessa fynd DIAPH3 som både en potentiell prognostisk markör och en nod i det nät av processer som styr tumörinitiering, genomomstabilitet och behandlingssvar—vilket öppnar nya vägar för terapier som en dag kan göra denna förödande hjärncancer mer mottaglig för befintliga behandlingar.
Citering: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
Nyckelord: glioblastom, kromosominstabilitet, hjärntumör-stamceller, strålningsresistens, tumörsupressorgener