Clear Sky Science · sv
Glioblastomceller som undviker celldöd orsakad av kemoradioterapi uppvisar ett bifurkerat glykolytiskt program
Varför denna hjärncancerstudie är viktig
Glioblastom är en av de dödligaste hjärntumörerna hos vuxna och återkommer nästan alltid efter operation, kemoterapi och strålning. Den här studien ställer en avgörande fråga: vad är det som är speciellt med den lilla grupp tumörceller som överlever behandlingen och senare återstartar sjukdomen? Genom att följa hur dessa celler hanterar socker över tid avslöjar forskarna en dold överlevnadsstrategi som kan förklara varför nuvarande behandlingar så ofta misslyckas — och som antyder nya sätt att skära av tumörens livlina.
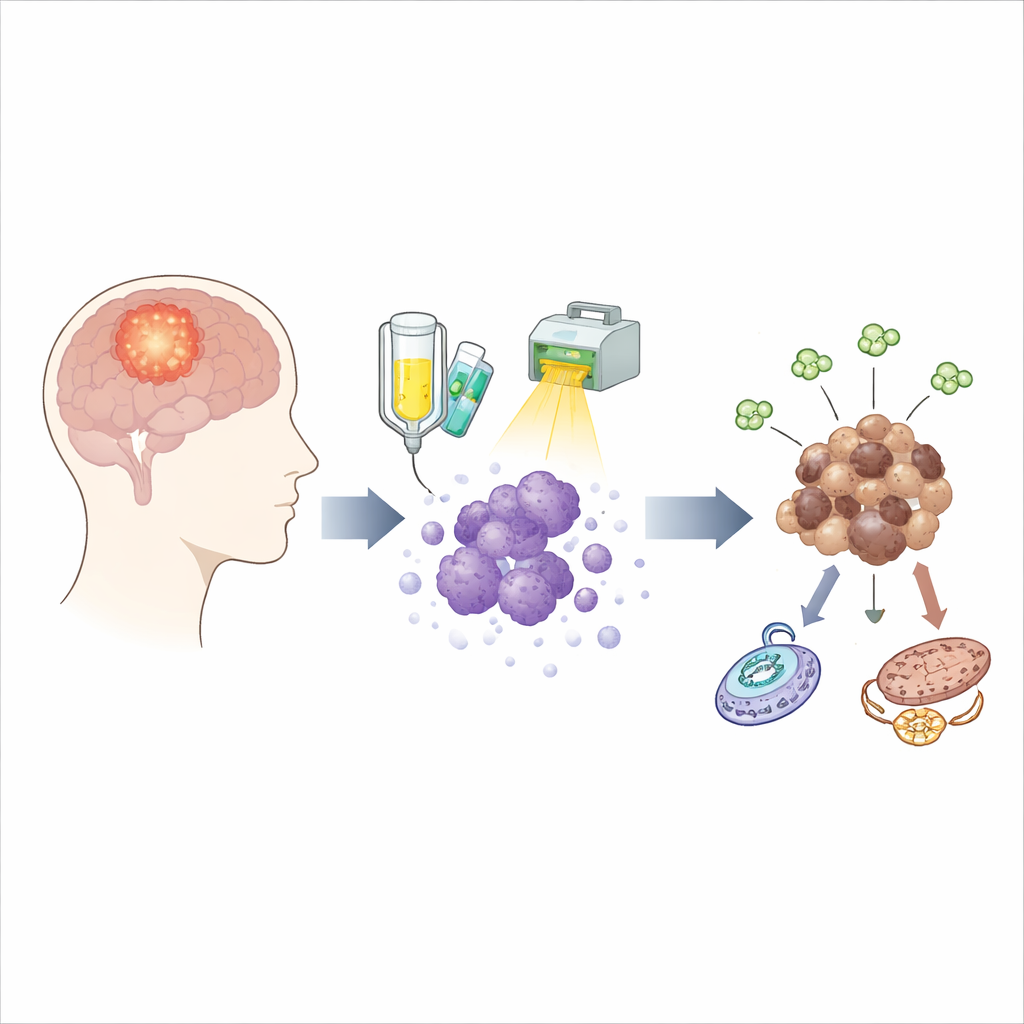
De dolda överlevarna efter behandling
Standardbehandling för glioblastom kombinerar en substans kallad temozolomid med strålning. Medan denna kombination dödar majoriteten av tumörcellerna, överlever en envis minoritet och kan slå rot som en ny tumör månader senare. För att fånga dessa överlevare i handling använde teamet tumörceller tagna direkt från tio olika patienter och utsatte dem för ett behandlingsschema utformat för att nära efterlikna vad människor får i kliniken. De tog prov på levande celler vid flera tidpunkter under och efter behandlingen, och studerade även matchande tumörer odlade i möss, vilket gjorde det möjligt att följa hur överlevarna förändras över tid i stället för att enbart jämföra tumörer före och efter återfall.
Hur tumörceller förändrar sitt sockerutnyttjande
Hjärnvävnad konsumerar en ovanligt stor andel av kroppens socker, och glioblastomceller är särskilt glupska efter det. Forskarna fann att när behandlingen fortskred drog de överlevande cellerna in ännu mer glukos från omgivningen. I en vändning brände de dock inte bara denna extra energi snabbare. Istället minskade dessa celler sin produktion av laktat, den typiska restprodukten från snabb sockernedbrytning i cancer. Mätningar av nyckelproteiner visade ett slående delat mönster: komponenter som för in socker i cellen och initierar nedbrytningen ökade, medan de som hanterar senare steg och bildar laktat minskade. Detta "bifurkade" program betyder att socker kommer in och börjar bearbetas, men den vanliga utgångsvägen till laktat är delvis stängd.
Omdirigering av bränsle till byggstenar och kraftverk
Vart tar det omdirigerade sockret vägen? Genom att använda särskilt märkta glukosmolekyler och avancerade mätningar av metaboliter visade teamet att de överlevande cellerna styr mycket av detta kol till två huvudsakliga destinationer. Den ena är en sidoväg kallad pentosfosfatvägen, som genererar råmaterial för att bygga DNA- och RNA-komponenter. I dessa celler ökade många nukleotidkomponenter och relaterade gener, vilket tyder på ett starkt fokus på att reparera och förbereda för förnyad tillväxt. Den andra destinationen är cellens kraftstationer, mitokondrierna. Enzymer i mitokondriens energicykel ökade, och tidigare arbete från samma grupp visade större import av sockerbaserat bränsle in i dessa strukturer. Tillsammans visar detta en koordinerad omkoppling: mindre slösaktig fermentation till laktat, mer investering i reparation, byggmaterial och flexibel energiproduktion.
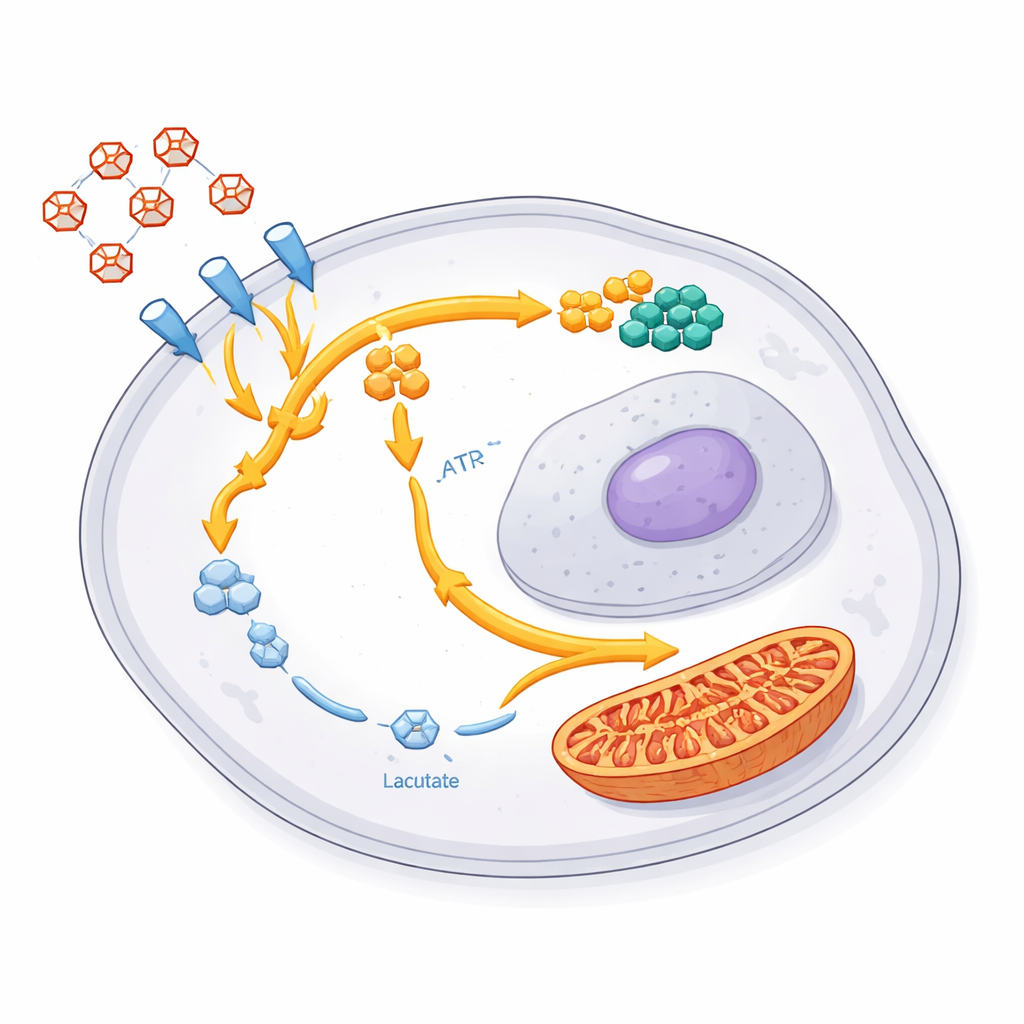
En gemensam överlevnadsmanual över tumörer och i djurmodeller
Glioblastomtumörer skiljer sig mycket mellan patienter, vilket ofta sätter käppar i hjulen för universella behandlingar. Trots denna mångfald visade var och en av de tio patientbaserade modellerna samma grundläggande skift efter kemoradioterapi: ökade tidiga steg i sockerhanteringen, minskade sena steg och laktatutflöde samt högre mitokondrieaktivitet. Viktigt är att samma signatur framträdde i mus‑hjärntumörer odlade från patientceller och behandlade med anpassade versioner av standardterapin. Återfallna tumörer i dessa djur bar fortfarande det förändrade sockerprogrammet, vilket indikerar att detta inte är en flyktig effekt utan ett stabilt drag hos celler som lyckas överleva behandlingen och återuppbygga cancern.
Vad detta betyder för framtida behandling
För lekmannen är huvudbudskapet att överlevande glioblastomceller inte bara "gömmer sig" för behandlingen; de omskolar aktivt hur de använder socker för att hålla sig vid liv. De tar in mer glukos, undviker att omvandla det till avfall och kanaliserar det istället till att skapa DNA‑byggstenar och driva mitokondrier — vilket hjälper dem att reparera skador, behålla ett flexibelt, stamcellslikt tillstånd och så småningom återväxa tumören. Genom att blottlägga detta delade metaboliska överlevnadstillstånd pekar studien på nya terapeutiska idéer: att rikta in sig mot de tidiga stegen i sockerbearbetningen, sidovägen för DNA‑byggstenar eller cellernas mitokondrieberoende skulle kunna göra standard kemoradioterapi mer fullständig och lämna färre flyktningar kvar som kan återstarta sjukdomen.
Citering: Martell, E., Kuzmychova, H., Chawla, U. et al. Glioblastoma cells that evade chemoradiotherapy-induced cell death exhibit a bifurcated glycolytic program. Cell Death Dis 17, 348 (2026). https://doi.org/10.1038/s41419-026-08646-9
Nyckelord: glioblastom, cancermetabolism, glukosanvändning, terapimotstånd, pentosfosfatvägen