Clear Sky Science · sv
Metabolisk orkestrering styrd av GGCT: omdirigering av glutamin till glutationbiosyntes samtidigt som glukosanapleros förstärks för tumörtillväxt
Varför detta spelar roll för cancerbehandling
Cancerceller växer snabbt och förbrukar stora mängder bränsle samtidigt som de ständigt måste skydda sig mot giftiga biprodukter från sin egen metabolism. Denna studie avslöjar hur ett relativt okänt enzym, GGCT, hjälper lever- och prostatatumörer att smart omdirigera två vanliga näringsämnen — glutamin och glukos — så att de både kan driva tillväxt och hålla de skadliga molekylerna, reaktiva syreradikaler, under kontroll. Att förstå denna metaboliska balansakt kan öppna nya vägar för att svälta ut tumörer eller överväldiga deras försvar.
Hur tumörceller jonglerar bränsle och skydd
Tumörceller är starkt beroende av glutamin, en aminosyra som har en dubbel funktion: den kan brytas ner för att mata cellens centrala energicykel, och den levererar också byggstenar för glutation, en kraftfull antioxidant som neutraliserar reaktiva syreradikaler. Författarna bekräftade först att glutaminnivåerna är högre i levertumörer än i närliggande frisk vävnad, och att cancerceller som odlas med mer glutamin delar sig snabbare både i skålar och i möss. När glutamin är knapp saktar cellerna ner, nyckelproteiner i cellcykeln minskar, och tumörer i djur krymper — delvis därför att antioxidantförsvaret försvagas och reaktiva syreradikaler ackumuleras.
En metabolisk brytare som gömmer sig i fullt dagsljus
Genom att granska patientprover och stora cancerregister fann teamet att enzymet GGCT konsekvent är mer förekommande i lever- och prostatatumörer än i normala vävnader, och att högre GGCT-nivåer förutspår sämre utfall. I både tumörprover och odlade celler stiger GGCT-nivåerna i takt med glutaminkoncentrationen, vilket tyder på att tumörer ”läser av” glutamintillgången genom detta protein. Forskarna kartlade en kontrollkedja: glutamin håller den tillväxtfrämjande faktorn c-Myc aktiv, vilket undertrycker en liten reglerande RNA kallad miR-29b-3p; när miR-29b-3p är låg släpps hämningen av GGCT och enzymet ackumuleras. Vid glutaminbrist vänder denna kedja, miR-29b-3p ökar, GGCT-meddelanden bryts ner snabbare och enzymnivån sjunker.
Omdirigering av glutamin och ökat glukosupptag
För att se vad GGCT faktiskt gör inne i cellen minskade eller ökade författarna dess nivåer och mätte både cellbeteende och hundratals metaboliter. Att tysta GGCT stannade cellerna i delningscykeln, krympte deras kolonier och sänkte kraftigt glutation samtidigt som reaktiva syreradikaler ökade; tillsats av en kemisk antioxidant återställde delvis tillväxten. Under mikroskopet blev mitokondrierna onormalt förlängda och mindre effektiva på att konsumera syre, samtidigt som cellerna försökte kompensera genom att öka glykolysen, första steget i sockernedbrytning. Detaljerad metabolisk profilering visade att mellanprodukter i den centrala energicykeln minskade när GGCT förlorades och ökade när det överproducerades.
Spåra kolatomernas väg
Teamet följde sedan märkta glutamin- och glukosatomer när de flödade genom tumörens metabolism. Vid överuttryck av GGCT hamnade mindre märkt glutamin i energicykeln och mer kanaliserades till nyligen syntetiserat glutation, vilket stödde antioxidantförsvaret. Samtidigt bidrog märkt glukos starkare till cykeln och kompenserade för det omdirigerade glutaminet. En mutant form av GGCT som saknade normal enzymatisk aktivitet kunde inte driva dessa skiften eller främja proliferation, vilket visar att GGCT:s katalytiska funktion är avgörande. Viktigt är att tillskott av extra pyruvat eller justering av inflödet till energicykeln återställde cellulära energinivåer men inte minskade reaktiva syreradikaler, vilket indikerar att GGCT främst styr redoxbalansen via glutation, inte genom enkla förändringar i energitillförseln.
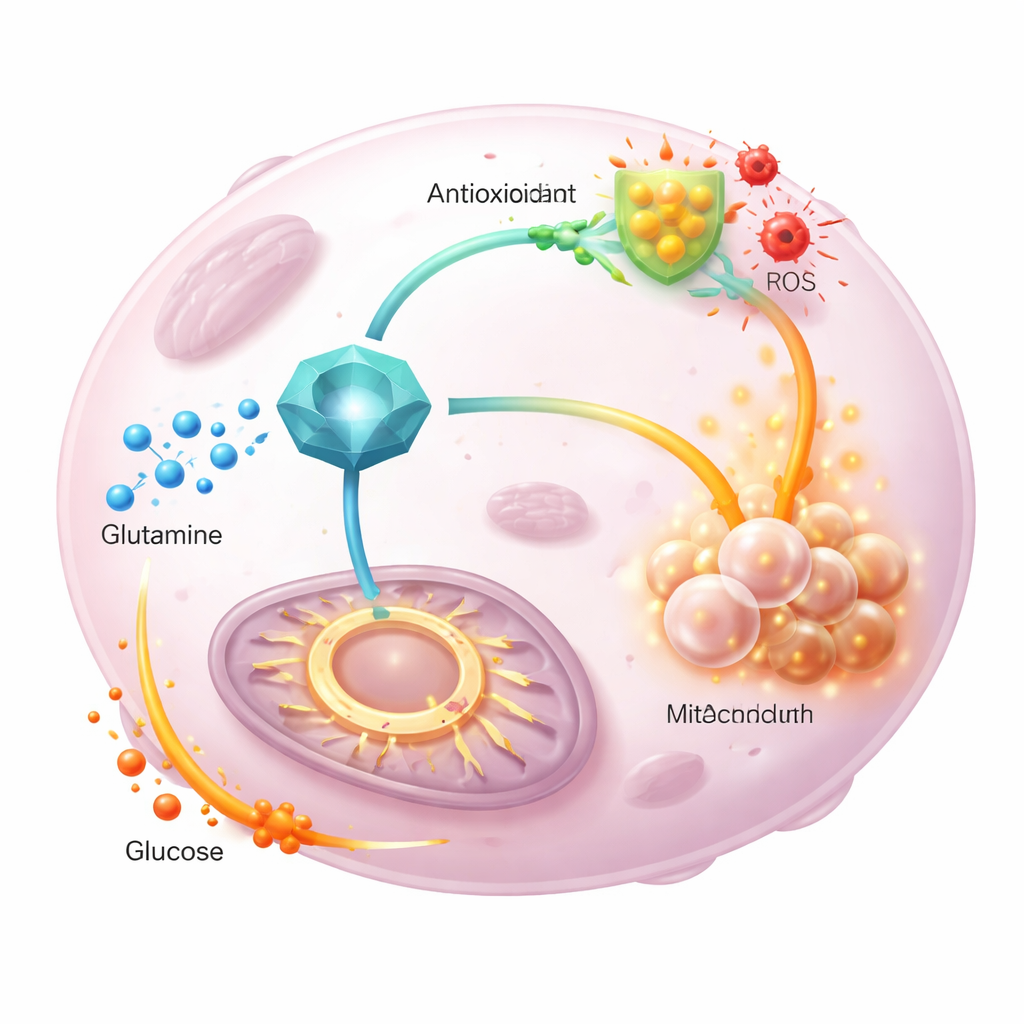
Vad detta betyder för framtida terapier
Sammantaget placerar fynden GGCT som en central koordinator som låter tumörer dela upp glutaminets uppgifter: det styr mer av detta näringsämne mot antioxidantproduktion samtidigt som det drar in glukos till energicykeln för att hålla celldelningen igång. I djurmodeller bromsade nedreglering av GGCT tumörtillväxt, minskade glutation och ökade oxidativ stress, och dessa effekter kunde delvis vändas med ett antioxidantläkemedel. För en lekmannaläsare är budskapet att vissa cancerformer överlever genom att använda GGCT som en metabolisk kopplingscentral; läkemedel som inaktiverar denna brytare skulle samtidigt kunna försvaga tumörens försvar mot oxidativ skada och rubba dess flexibla näringsanvändning, vilket gör standardbehandlingar mer effektiva.
Citering: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
Nyckelord: cancermetabolism, glutamin, glutation, oxidativ stress, GGCT-enzym