Clear Sky Science · sv
Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51
Varför denna forskning är viktig
För många som diagnostiserats med äggstockscancer fungerar dagens riktade läkemedel endast för en liten minoritet vars tumörer bär på särskilda genetiska defekter. Denna studie undersöker ett sätt att utvidga fördelarna med en viktig läkemedelsklass, PARP‑hämmare, till den betydligt större grupp patienter vars tumörer saknar dessa mutationer. Genom att kombinera en ny experimentell förening med befintliga läkemedel visar forskarna en strategi för att pressa cancerceller in i en dödlig återvändsgränd samtidigt som frisk vävnad skonas.
Ett hinder i dagens behandling av äggstockscancer
Äggstockscancer upptäcks ofta sent och är fortfarande en av de dödligaste cancerformerna bland kvinnor. PARP‑hämmare, såsom olaparib, kan vara mycket effektiva, men främst hos patienter vars tumörer redan har brister i en DNA‑reparationsväg kopplad till BRCA1‑ och BRCA2‑generna. De flesta tumörer har dock fortfarande intakt reparationsmaskineri och kan åtgärda den DNA‑skada som dessa läkemedel orsakar, vilket tillåter cancercellerna att överleva. En central del av detta reparationslag utgörs av två proteiner, BRCA2 och Rad51, som hjälper till att laga brutna DNA‑strängar genom homolog rekombination. Att hitta sätt att selektivt försvaga denna reparationsväg i cancerceller skulle kunna göra PARP‑hämmare användbara för långt fler patienter.
Roll för en välkänd tillväxtbrytare
Forskargruppen fokuserade på en välkänd cancerkopplad molekyl, epidermal tillväxtfaktorreceptor (EGFR), som sitter på ytan av många tumörceller och driver deras tillväxt. De fann att EGFR gör mer än att sända tillväxtsignaler: i äggstockscellinjer med normala BRCA‑gener kopplades höga nivåer av EGFR till sämre patientöverlevnad och resistens mot PARP‑hämmare. När EGFR minskades eller stängdes av i cellkulturer och hos möss blev tumörerna mycket mer sårbara för olaparib. Forskarna visade att EGFR hjälper till att föra BRCA2 och Rad51 in i cellkärnan efter DNA‑skada, där de kan reparera brott och dämpa behandlingens effekt. Att bara blockera EGFR:s enzymatiska aktivitet var inte tillräckligt; den totala mängden EGFR‑protein behövde minskas för att avsevärt rubba denna reparationsväg.
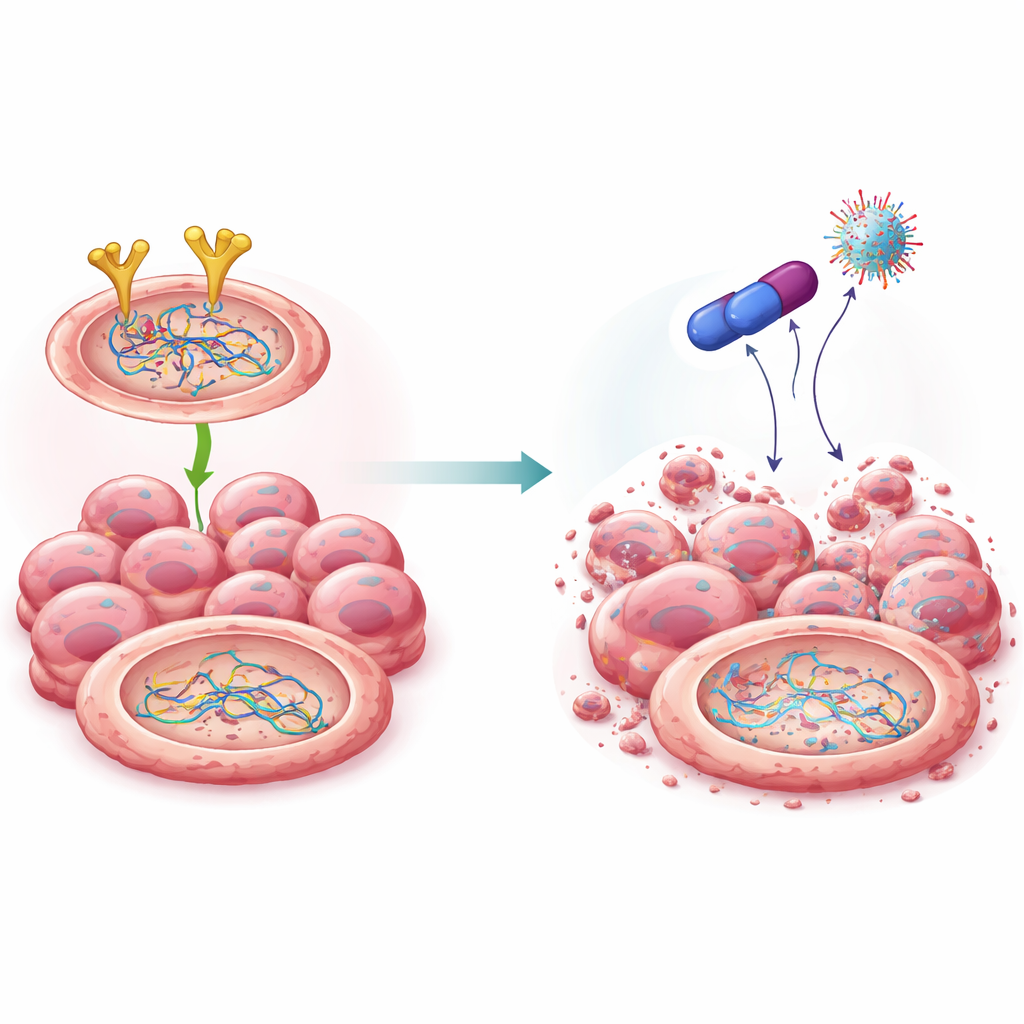
En ny förening som avväpnar reparationslaget
Byggt på tidigare arbete med en läkemedelsfamilj känd som biguanider syntetiserade forskarna flera kemiska släktingar och identifierade en framstående molekyl, kallad 4C. Denna förening var starkt giftig för äggstocksceller men relativt skonsam mot normala celler. Datorbaserade modeller och laboratorietester indikerade att 4C binder direkt till EGFR och märker det för nedbrytning i cellens proteinnedbrytningsmaskineri. Till skillnad från vissa befintliga EGFR‑läkemedel minskade 4C den totala mängden EGFR i stället för att bara tysta dess aktivitet. När EGFR‑nivåerna sjönk minskade också stabiliteten hos BRCA2 och Rad51: de märktes för borttagning, bröts ner och kunde inte längre stödja effektiv DNA‑reparation. Viktigt är att denna beskärning skedde på protein‑nivå utan att förändra de underliggande generna.
Blockerar en räddningsväg inne i cellen
Studien avslöjade en mer detaljerad händelsekedja som kopplar DNA‑skada till tumöröverlevnad. Efter att PARP‑hämmare skadat DNA sänder en annan sensorsprotein, ATM, ett meddelande från kärnan ut till cellkroppen. Som svar samarbetar EGFR med BRCA2 och Rad51 och hjälper dem att flytta in i kärnan, där de reparerar skadorna. Forskarna upptäckte att ett tredje protein, c‑Cbl, normalt fungerar som en sorts märkningsenzym som sätter degraderingsmärken på BRCA2 och Rad51. EGFR konkurrerar med c‑Cbl om tillgång till dessa reparationsproteiner och skyddar dem från att märkas för nedbrytning. När 4C sänker EGFR‑nivåerna kan c‑Cbl lättare binda till BRCA2 och Rad51, vilket leder till deras märkning, nedbrytning och förlust. Med färre reparationsproteiner i kärnan ackumuleras DNA‑skador och cancerceller blir mycket känsligare för PARP‑hämmare.
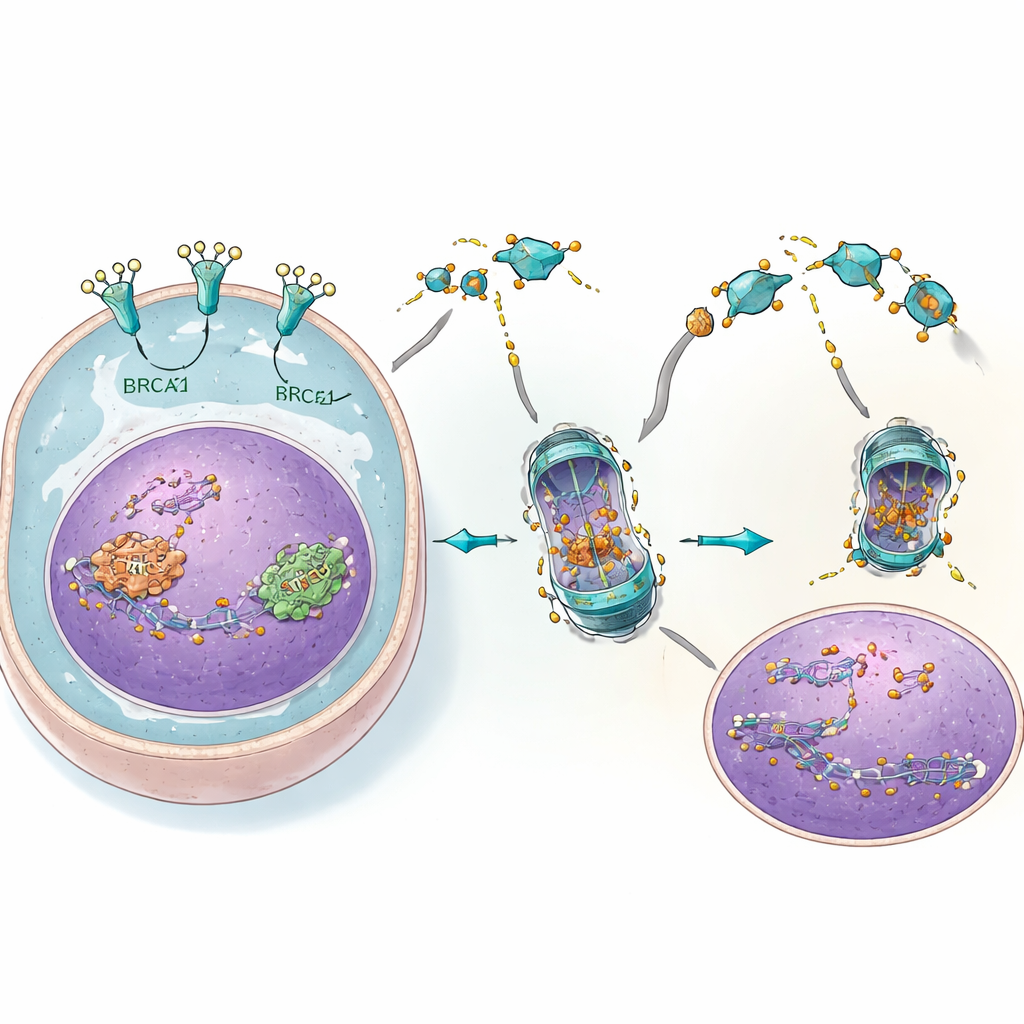
Från celler till djur: en potent kombination
I både odlade celler och musemodeller gav kombinationen av 4C och PARP‑hämmare en kraftfull dubbelattack. Tumörer med normala BRCA‑gener som motstod någon av läkemedlen ensamt krympte dramatiskt eller slutade växa när de utsattes för båda tillsammans. Markörer för DNA‑skada steg kraftigt, i linje med idén att reparationskapaciteten överväldigades. Samtidigt visade normala celler och viktiga organ som lever och njurar få tecken på skada, troligen eftersom de har mycket lägre EGFR‑nivåer och i mindre grad förlitar sig på denna särskilda reparationsgenväg. Kombinationens fördelar sträckte sig även till att minska spridningen av äggstockscellernas spridning i kroppen.
Vad detta kan betyda för patienter
Detta arbete föreslår ett sätt att vända en cancercells styrka till en svaghet. Genom att rikta in sig på EGFR med den nya föreningen 4C tar forskarna bort det skydd som BRCA2 och Rad51 ger, vilket gör att tumörer med i övrigt normal DNA‑reparation beter sig mer som BRCA‑mutanta cancerformer i sin respons på PARP‑hämmare. Denna påtvingade sårbarhet, känd som ”syntetisk letalitet”, skulle kunna utöka räckvidden för befintliga läkemedel till många fler kvinnor med äggstockscancer, samtidigt som biverkningarna förblir hanterbara. Även om 4C fortfarande är experimentell och kommer att kräva omfattande prövningar i mer avancerade modeller och i kliniska studier, erbjuder studien en tydlig plan för hur man genom att demontera specifika reparationshjälpare i tumörceller kan förbättra behandlingsresultaten.
Citering: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
Nyckelord: ovarian cancer, PARP inhibitors, EGFR, DNA repair, targeted therapy