Clear Sky Science · sv
Förlust av PRKACB underlättar metastasering av diffus typ av magcancer genom aktivering av RhoA-signalering
Varför denna studie är viktig för magcancer
Diffus typ av magcancer är en särskilt aggressiv form av magsäckscancer som ofta sprider sig vida inom buken, vilket gör den svår att behandla och ofta dödlig. Denna studie undersöker varför dessa tumörer är så benägna att sprida sig och avslöjar ett molekylärt bromssystem som normalt hindrar cancerceller från att vandra — och visar vad som händer när den bromsen sviktar. Att förstå denna dolda kontrollknapp kan öppna nya vägar för att förutsäga vilka patienter som har högst risk och för att utveckla läkemedel som bromsar eller stoppar farlig spridning.
En farlig form av magsäckscancer
Alla magcancerformer beter sig inte lika. Intestinala tumörer tenderar att bilda mer strukturerade massor, medan diffus typ av magcancer (DGC) består av utspridda celler som lätt glider iväg från den primära tumören. Patienter med DGC har högre dödlighet än de med intestinal typ, delvis för att deras tumörer lättare sår nya tillväxter i bukhålan. Tidigare genetiska studier hade redan länkat DGC till återkommande förändringar i en gen som heter RHOA, som påverkar hur celler rör sig och ändrar form. Men det var oklart hur dessa förändringar kopplade till de bredare signalnätverk som styr om cancerceller stannar kvar eller migrerar.
Att hitta en förlorad broms i tumörprover
Forskarna fokuserade på ett protein kallat PRKACB, en katalytisk subenhet i det välkända enzymet protein kinase A, som finjusterar många cellbeteenden genom att tillsätta fosfatgrupper till andra proteiner. En tidigare proteomikstudie antydde att PRKACB-nivåerna var ovanligt låga i aggressiv DGC. För att testa detta undersökte teamet tumörprover från 376 patienter och jämförde diffus- och intestinaltyp samt närliggande icke-cancerös vävnad. De fann att PRKACB-nivåerna var markant reducerade i diffus-typ tumörer, särskilt i avancerade stadier, men inte i intestinal typ. Patienter vars tumörer hade låg PRKACB hade betydligt sämre total överlevnad, även efter att andra kliniska faktorer beaktats, vilket tyder på att PRKACB fungerar som en tumörsuppressor i detta sammanhang.
Hur låg PRKACB främjar cellflykt
För att se vad PRKACB gör inne i cancerceller använde teamet odlade cellinjer som modellerar diffus typ av magcancer. När de artificiellt minskade PRKACB blev cellerna mer rörliga och invasiva i laboratorietester, lättare att pressa genom barriärer och bildade fingerlika utskott kallade pseudopodier som hjälper celler att krypa. Dessa celler skiftade också från ett mer ordnat, epitelialt tillstånd mot ett lösare, mesenkym-liknande tillstånd som förknippas med metastasering, och förlorade adhesionsmolekylen E‑cadherin som normalt hjälper celler att hålla ihop. Omvänt gjorde ökad PRKACB nivå cellerna mindre migratoriska och mindre invasiva. Viktigt är att dessa förändringar inte påverkade hur snabbt cellerna delade sig, vilket pekar på en specifik roll för PRKACB i att möjliggöra spridning, inte tillväxt.
Fördjupning i RhoA-signalens brytare
Forskarna undersökte sedan hur PRKACB utövar denna anti-metastatiska effekt. Genom protein–protein interaktionsmetoder och strukturell modellering visade de att PRKACB direkt binder till RhoA, en molekylär brytare som växlar mellan inaktiva och aktiva former för att styra cellform och rörelse. PRKACB tillsätter en fosfatgrupp på en specifik position på RhoA (serin 188), vilket dämpar RhoA och dämpar de nedströms ROCK- och FAK-vägarna som driver cytoskelettomläggningar och cellmotilitet. När PRKACB sänktes var RhoA mindre fosforylerad, mer aktiv och ROCK/FAK-signalering intensifierades, vilket ledde till mer aggressiv cellrörelse. I musmodeller där humanliknande tumörer implanterades i magsäcksväggen orsakade minskad PRKACB fler och större metastatiska noduler i buken och tidigare uppkomst av synlig spridning, återigen utan att förändra hur snabbt etablerade metastaser växte.
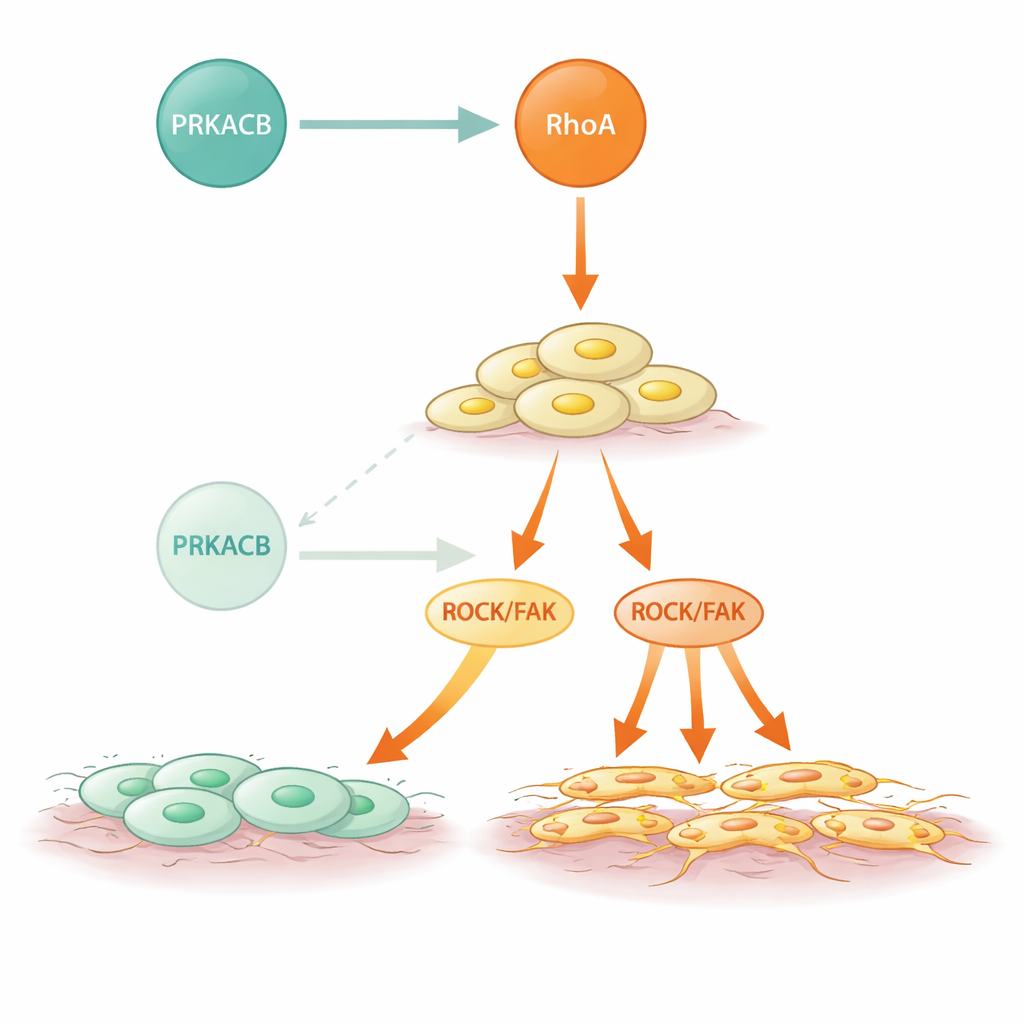
Mutant signalering och en möjlig interventionsväg
Diffus typ av magcancer bär ofta RHOA-mutationer, och denna studie visar hur vissa av dessa förändringar förvärrar problemet. Flera vanliga DGC-associerade mutationer i RhoA försvagade eller avskaffade dess bindning till PRKACB men påverkade inte RhoA:s förmåga att aktivera sina nedströms partners. Som ett resultat undkom dessa mutanta former den dämpande fosforyleringen av PRKACB och visade förhöjd ROCK-aktivitet och starkare invasivt beteende. Slående nog, när forskarna behandlade celler och möss med en RhoA-blockerande förening återställdes den ökade metastaseringen orsakad av låg PRKACB i stor utsträckning. Detta tyder på att även i tumörer där den naturliga bromsen är svag eller saknas kan man genom att rikta in sig mot den överaktiva RhoA-vägen direkt hämma spridningen.
Vad detta betyder för patienter och framtida behandlingar
Enkelt uttryckt identifierar detta arbete PRKACB som en nyckelkomponent i en intern "anti-migrerings"-krets i diffus typ av magcancer. När PRKACB-nivåerna sjunker, eller när RhoA är muterat så att PRKACB inte kan binda och modifiera det, ökar RhoA-signaleringen och cancerceller blir bättre på att bryta sig loss och kolonisera bukhålan. Att mäta PRKACB- och RhoA-status i tumörer skulle kunna hjälpa läkare att bedöma hur sannolikt det är att en patients cancer metastaserar och vem som mest kan gynnas av läkemedel som hämmar RhoA–ROCK–FAK-vägen. Även om sådana behandlingar kräver vidare utveckling och kliniska prövningar, kartlägger studien en tydlig molekylär väg från en förlorad broms till dödlig spridning — och pekar på nya sätt att sakta ner den resan.
Citering: Sun, J., Zhao, J., Yang, X. et al. Loss of PRKACB facilitates metastasis of diffuse-type gastric cancer through RhoA signaling activation. Cell Death Dis 17, 281 (2026). https://doi.org/10.1038/s41419-026-08553-z
Nyckelord: diffus typ av magcancer, metastas, PRKACB, RhoA-signalering, ROCK-FAK-vägen