Clear Sky Science · sv
Den långa icke-kodande RNA-axeln ADEI/miR-93-3p/STAT3 främjar progression och immunundvikande hos Epstein–Barr-virus-positiv diffus stor B-cellslymfom genom reglering av PD-1/PD-L1-kontrollpunkten
Varför detta är viktigt för vårt immunskydd
Vissa lymfom kopplade till det vanliga Epstein–Barr-viruset (EBV) är ovanligt svårbehandlade och undkommer ofta kroppens immunsvar. Denna studie avslöjar ett dolt budskapssystem i dessa tumörer: små blåsor kallade exosomer som bär en lång RNA-molekyl som hjälper tumörer att växa och gömma sig för immunceller. Att förstå detta dolda samtal kan öppna nya vägar för diagnos och behandling av dessa svårbotade blodcancerformer.
Ett virus som rubbar jämvikten
Diffust storcelligt B-cellslymfom (DLBCL) är det vanligaste aggressiva lymfomet. När tumörceller bär på EBV tenderar patienter att svara sämre på standard kemoterapi kombinerad med immunterapi. Forskarna jämförde först EBV-positiva och EBV-negativa lymfomceller i laboratoriet. De fann att EBV-infektion gjorde att lymfomceller delade sig snabbare, bildade fler kolonier och gav större tumörer i möss. EBV-positiva celler visade också högre nivåer av ett ytprotein som kallas PD-L1, vilket interagerar med PD-1 på immunceller för att stänga av deras angrepp. När teamet blandade lymfomceller med mördande CD8-T-celler minskade EBV-positiva tumörer antalet och styrkan hos dessa T-celler, en effekt som kunde återställas med antikroppar som blockerar PD-1/PD-L1-bromsen.
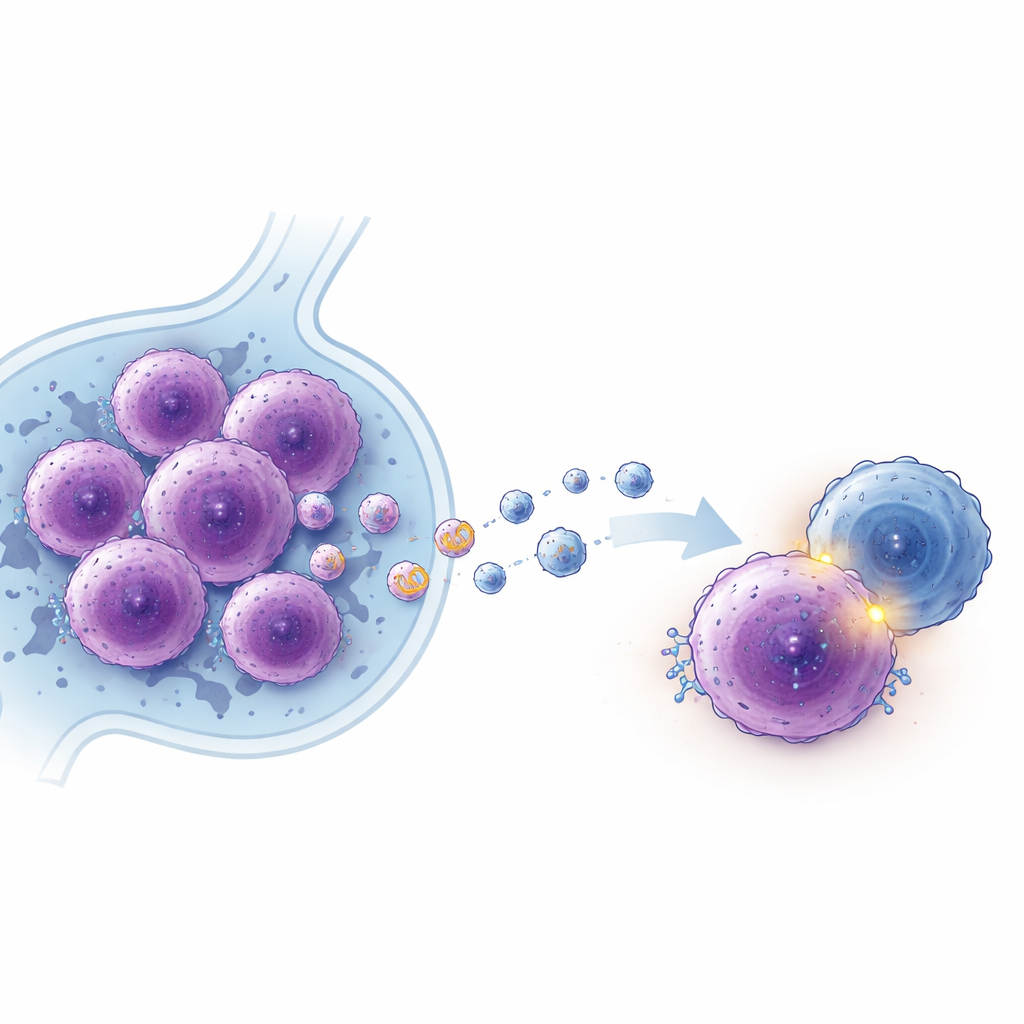
En lång RNA som hjälper tumörer att växa och dölja sig
För att förstå hur EBV omformar tumörbeteendet undersökte teamet långa icke-kodande RNA—RNA-sekvenser som inte kodar för proteiner men kan reglera många cellulära processer. Genom att kartlägga RNA-innehållet i exosomer som frisattes från EBV-positiva och EBV-negativa DLBCL-celler upptäckte de en tidigare okarakteriserad RNA, som de kallade lncADEI, som var starkt uppreglerad i EBV-positiva celler och deras exosomer. När de tvingade lymfomceller att producera mer lncADEI prolifererade cellerna snabbare, bildade fler kolonier och blev motståndskraftiga mot programmerad celldöd. Att minska lncADEI gav motsatt effekt, långsammare tillväxt och ökad celldöd både i odlingsskålar och i musmodeller.
Hur lncADEI kopplar om immunundvikande
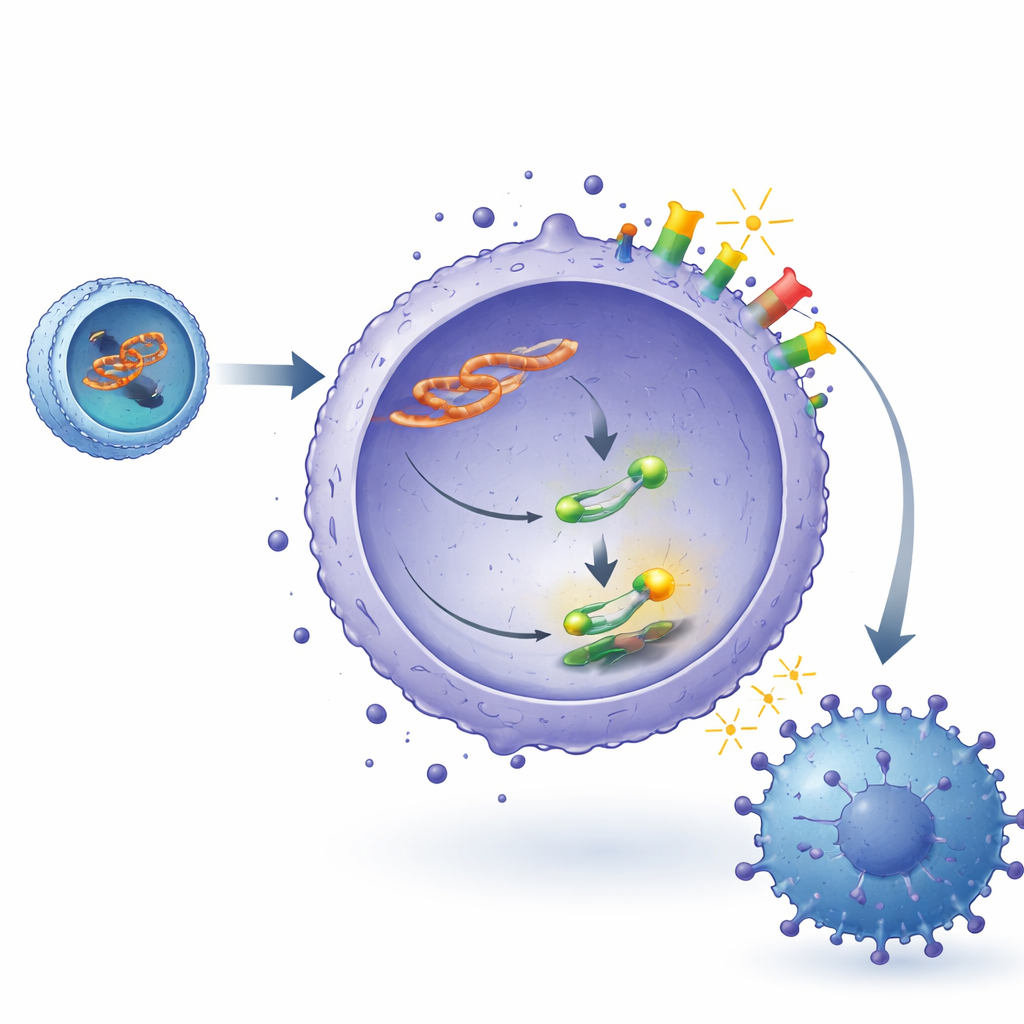
Forskarna följde sedan hur lncADEI hänger samman med PD-1/PD-L1-immuncheckpointen. Inuti lymfomceller ligger lncADEI främst i cytoplasman, där den fungerar som en svamp för en liten reglerande RNA kallad miR-93-3p. Under normala förhållanden hjälper miR-93-3p till att hålla ett viktigt signalprotein, STAT3, i schack genom att binda dess budskap och begränsa dess produktion. När lncADEI binder upp miR-93-3p ökar mängden STAT3 som syntetiseras och aktiveras. STAT3 binder i sin tur direkt till regleringsregionen av PD-L1-genen i lymfomceller och ökar PD-L1-produktionen. Denna kedja—lncADEI som fångar miR-93-3p, frigör STAT3 och driver PD-L1—resulterar i högre PD-L1 på tumörceller, starkare avstängningssignaler mot CD8-T-celler och minskad T-cellsaktivitet.
Exosomligt ”post” som sprider skadliga instruktioner
EBV-positiva lymfomceller behåller inte lncADEI för sig själva. De utsöndrar betydligt fler exosomer än EBV-negativa celler, och dessa exosomer är packade med lncADEI. När EBV-negativa lymfomceller exponerades för exosomer från EBV-positiva celler tog de upp dem, deras interna lncADEI-nivåer ökade och de började uppträda mer aggressivt—de delade sig snabbare och bildade fler kolonier. I blandade kulturer som inkluderade T-celler minskade lncADEI-rika exosomer antalet och dödande effekten hos CD8-T-celler och ökade PD-1 på dessa immunceller, vilket ytterligare försvagade immunsvaret. Detta tyder på att EBV-positiva tumörer kan "lära upp" närliggande tumörceller och omforma sin omgivning genom lncADEI-rika exosomer.
Ledtrådar från patienternas blodprover
För att koppla dessa laboratoriefynd till verklig sjukdom mätte teamet lncADEI i blodets exosomer från 47 patienter med DLBCL. De vars tumörer var EBV-positiva hade signifikant högre nivåer av exosomal lncADEI än EBV-negativa patienter. Hög lncADEI i blodet var också förenat med mer avancerad sjukdomsstadium, mer aggressiv tumörsubtyp, högre standardriskpoäng och förhöjda markörer för vävnadsskada. Dessa mönster tyder på att exosomal lncADEI i blodet kan fungera som en minimalt invasiv indikator på EBV-driven lymfom och dess svårighetsgrad.
Vad detta betyder för framtida vård
Enkelt uttryckt visar detta arbete ett trestegs-trick som EBV-kopplade lymfom använder: de överproducerar en lång RNA (lncADEI), packar den i resande blåsor och använder den både inne i tumören och i närliggande celler för att öka en välkänd immunbroms, PD-L1. Resultatet blir snabbare tumörtillväxt och dämpat T-cellsangrepp. Eftersom varje steg i denna kedja—lncADEI självt, dess interaktion med miR-93-3p och STAT3, och frisättningen av lncADEI-rika exosomer—erbjuder en möjlig interventions- eller mätpunkt, pekar studien mot nya strategier för att förbättra immunterapi och för att övervaka EBV-associerade lymfom med ett enkelt blodprov.
Citering: Zheng, W., Lai, G., Liao, Z. et al. Long noncoding RNA ADEI/miR-93-3p/STAT3 axis promotes Epstein–Barr virus-positive diffuse large B-cell lymphoma progression and immune evasion through regulating the PD-1/PD-L1 checkpoint. Cell Death Dis 17, 280 (2026). https://doi.org/10.1038/s41419-026-08532-4
Nyckelord: Epstein–Barr-virus-lymfom, immuncheckpoint, lång icke-kodande RNA, exosomer, STAT3-signalering