Clear Sky Science · sv
PD-1 skyddar expanderande mänskliga T‑celler från för tidigt restimuleringsinducerat celldöd genom att modulera TCR- och CD28‑signalering
Varför det spelar roll att stoppa vänligt eld från immunsystemet
Våra immunsystem är beroende av arméer av T‑celler som snabbt multiplicerar för att bekämpa infektioner och cancer. Men denna explosiva tillväxt är farlig: om för många T‑celler förblir aktiva för länge kan de skada frisk vävnad eller driva autoimmuna sjukdomar. Denna studie undersöker hur en välbekant ”broms” på T‑celler, en molekyl kallad PD‑1, hjälper expanderande mänskliga T‑celler att undvika att dö för tidigt av sin egen överstimulering. Att förstå denna balans är avgörande för säkrare cancerimmunoterapier och för att förhindra skadliga överreaktioner i immunsystemet.
En inbyggd självdestruktion som måste tajmas noggrant
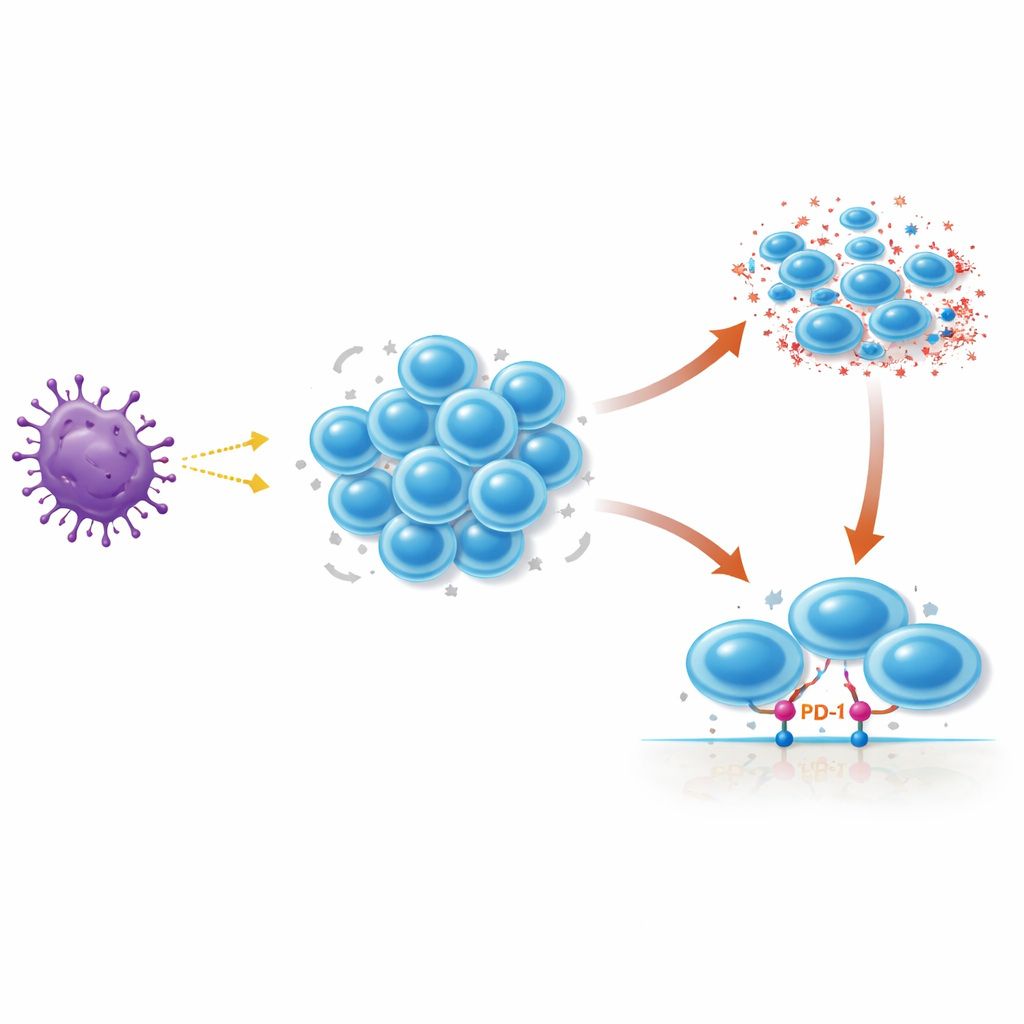
När T‑celler känner igen ett hot delar de sig i stora kloner av identiska kämpar. För att förhindra att denna respons spårar ur bär T‑celler ett inbyggt självdestruktionsprogram kallat restimuleringsinducerad celldöd (RICD). När en redan aktiverad T‑cell starkt triggas igen via sin huvudsensor, T‑cellreceptorn, kan RICD slås på för att ta död på den cellen. Detta hjälper till att krympa armén när hotet är undanröjt och undviker farliga lymfoproliferativa sjukdomar där T‑celler samlas i överskott. Tidigt i en respons behöver dock T‑celler tid att expandera innan denna självdestruktionsväg blir dominerande, och hur den tidpunkten styrs hos människor har inte varit helt klarlagt.
Den överraskande skyddande sidan av en immunbroms
PD‑1 är berömt som ett mål för ”checkpoint”‑läkemedel som används i cancerbehandling, där blockering av det kan återväcka uttröttade T‑celler i tumörer. Traditionellt ses PD‑1 som en molekyl som försvagar T‑cellsaktivitet; PD‑1 sätts dock snabbt på när mänskliga T‑celler först möter ett stimulus och kvarstår på måttliga nivåer under deras tidiga expansion. I denna studie isolerade forskarna mänskliga CD4‑ och CD8‑T‑celler från friska donatorer, aktiverade dem i kultur och följde PD‑1 och dess partner PD‑L1 över tid. De fann att PD‑1 och PD‑L1 når en topp inom några dagar efter aktivering—precis när T‑cellerna multipliceras—och sedan minskar när cellerna mognar. När teamet blockerade PD‑1 eller PD‑L1 under upprepad stimulering dog fler T‑celler, vilket indikerar att normal PD‑1‑signalering faktiskt skyddar dessa expanderande celler från för tidig RICD.
Hur PD‑1 omformar kommunikationen vid cellsytan
För att undersöka detta skydd mer precist byggde forskarna artificiella ”proxy” antigen‑presenterande pärlor täckta med aktiverande signaler (för att efterlikna T‑cellreceptorn och dess huvudhjälpare CD28) och i vissa fall PD‑L1. När expanderande T‑celler restimulerades med pärlor som bar PD‑L1 förlorade de konsekvent färre celler än med kontrollpärlor, och standardmarkörer för tidig och sena apoptosstadier sjönk mot baslinjen. Denna överlevnadsökning berodde på hur mycket PD‑L1 som fanns och på att PD‑L1 var placerad intill de aktiverande signalerna, vilket speglar den täta organisationen i den naturliga immunsynapsen. Intressant nog var den skyddande effekten starkast när CD28 engagerades tillsammans med T‑cellreceptorn, vilket tyder på att PD‑1 lugnar båda aktiveringsvägarna samtidigt. Utan PD‑1 gjorde CD28 cellerna mer benägna att genomgå RICD, men tillsats av PD‑L1 utplånade denna extra känslighet.
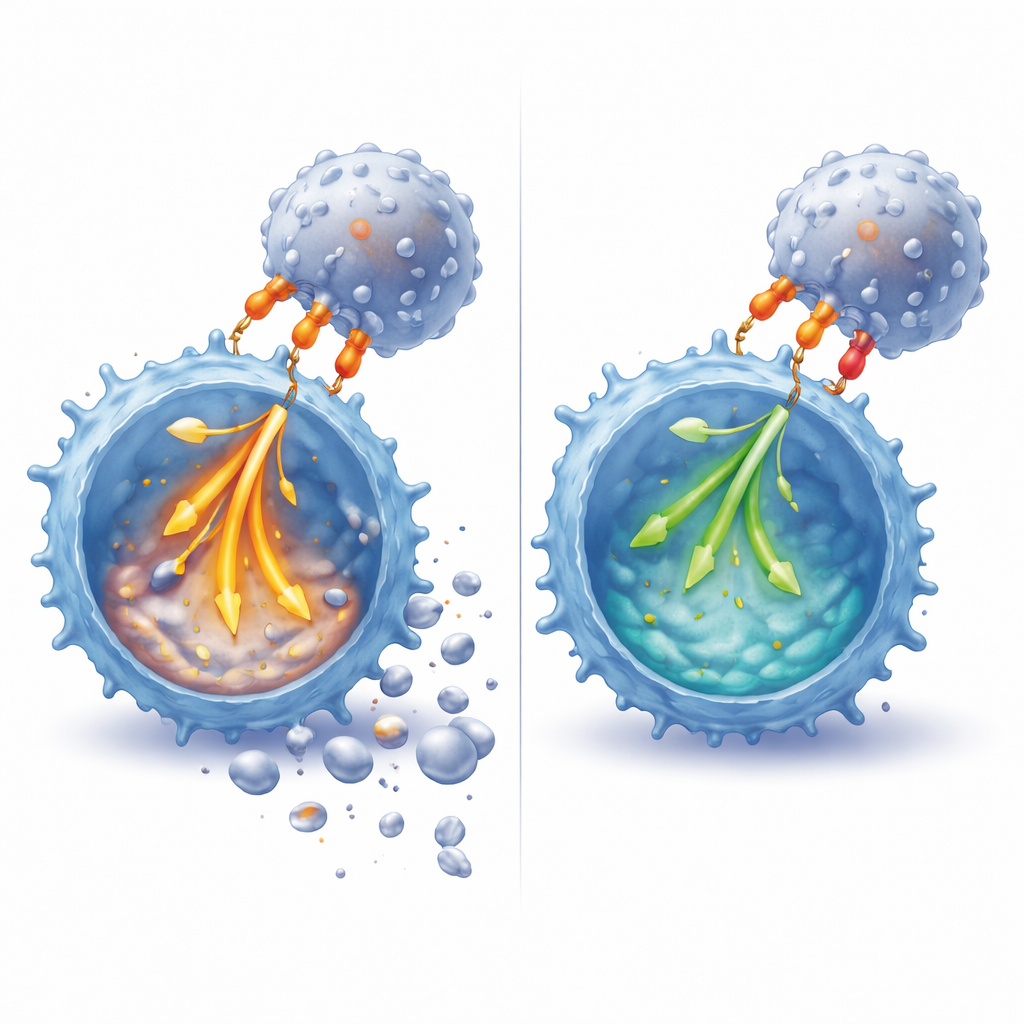
Att dämpa signaler och vinkla överlevnadsmolekyler
Vid inspektion inuti cellerna fann forskarna att PD‑1‑engagemang dämpade ett brett spektrum av tidiga signalhändelser som följer på T‑cellsrestimulering. Fosfatmärken på nyckelproteiner i signalvägarna—including komponenter direkt kopplade till receptorn och ett centralt reläenzym kallat ERK—var märkbart minskade när PD‑L1 var närvarande. Denna utjämning var särskilt framträdande när CD28 också engagerades, vilket speglar den större påverkan på RICD i detta läge. PD‑1‑signalering påverkade också cellcykeln, så att fler celler hölls i G1‑”checkpoint”‑fasen istället för att drivas aggressivt in i DNA‑replikation, ett tillstånd som är känt för att öka känsligheten för dödssignaler. På proteinnivå försköt PD‑1 balansen mellan dödsfrämjande och överlevnadsfrämjande molekyler: den dämpade induktionen av FAS‑ligand, en viktig utlösare av T‑cellsdöd, och hjälpte till att bevara survivin, en faktor som stödjer både överlevnad och kontrollerad delning av T‑celler.
Vad dessa fynd betyder för terapier och immunhälsa
Tillsammans visar resultaten att PD‑1 inte enbart är en strömbrytare som stänger av T‑celler, utan en nyanserad ställskruv som skyddar nyaktiverade mänskliga T‑celler från att dö för tidigt under deras expansion. Genom att tona ner styrkan i upprepade signaler via både T‑cellreceptorn och CD28, och genom att gynna överlevnadsfrämjande molekyler framför dödssignaler, tillåter PD‑1 att en robust men kontrollerad T‑cellsarmé bildas innan självdestruktionsprogrammet fullt ut träder i kraft. För patienter innebär detta att läkemedel som blockerar PD‑1—kraftfulla verktyg inom onkologi—kan göra vissa T‑celler mer sårbara för RICD, vilket potentiellt kan förändra normal immunbalans eller bidra till biverkningar. Framtida terapier och cellbaserade behandlingar som CAR‑T‑celler kan dra nytta av att medvetet modulera PD‑1 och relaterade vägar för att bevara tillräckligt många långlivade, effektiva T‑celler samtidigt som skadlig överaktivitet i immunsystemet förhindras.
Citering: Lee, K.P., Elster, S., Epstein, B. et al. PD-1 protects expanding human T cells from premature restimulation-induced cell death by modulating TCR and CD28 signaling. Cell Death Dis 17, 272 (2026). https://doi.org/10.1038/s41419-026-08530-6
Nyckelord: PD-1‑signalering, T‑cellsöverlevnad, immunkontroller, aktiveringsinducerad celldöd, cancerimmunoterapi