Clear Sky Science · sv
Kärnmyosin 1 länkar genomisk arkitektur till ombyggnad av fettvävnad, metabol inflammation och fetma hos möss
Varför cellens skelett spelar roll för kroppsfett
Fetma tillskrivs ofta vad vi äter och hur mycket vi rör på oss, men djupt inne i våra celler kan också hur DNA packas och läses påverka balansgången. Den här studien visar att ett litet motorprotein, kärnmyosin 1 (NM1), som hjälper till att organisera DNA inne i cellkärnan, spelar en oväntad roll i hur fettceller bildas, lagrar energi och utlöser inflammation. Genom att studera möss som saknar detta protein upptäckte forskarna en direkt länk mellan den fysiska arkitekturen hos våra gener och utvecklingen av ohälsosamt visceralt fett och metaboliska problem.
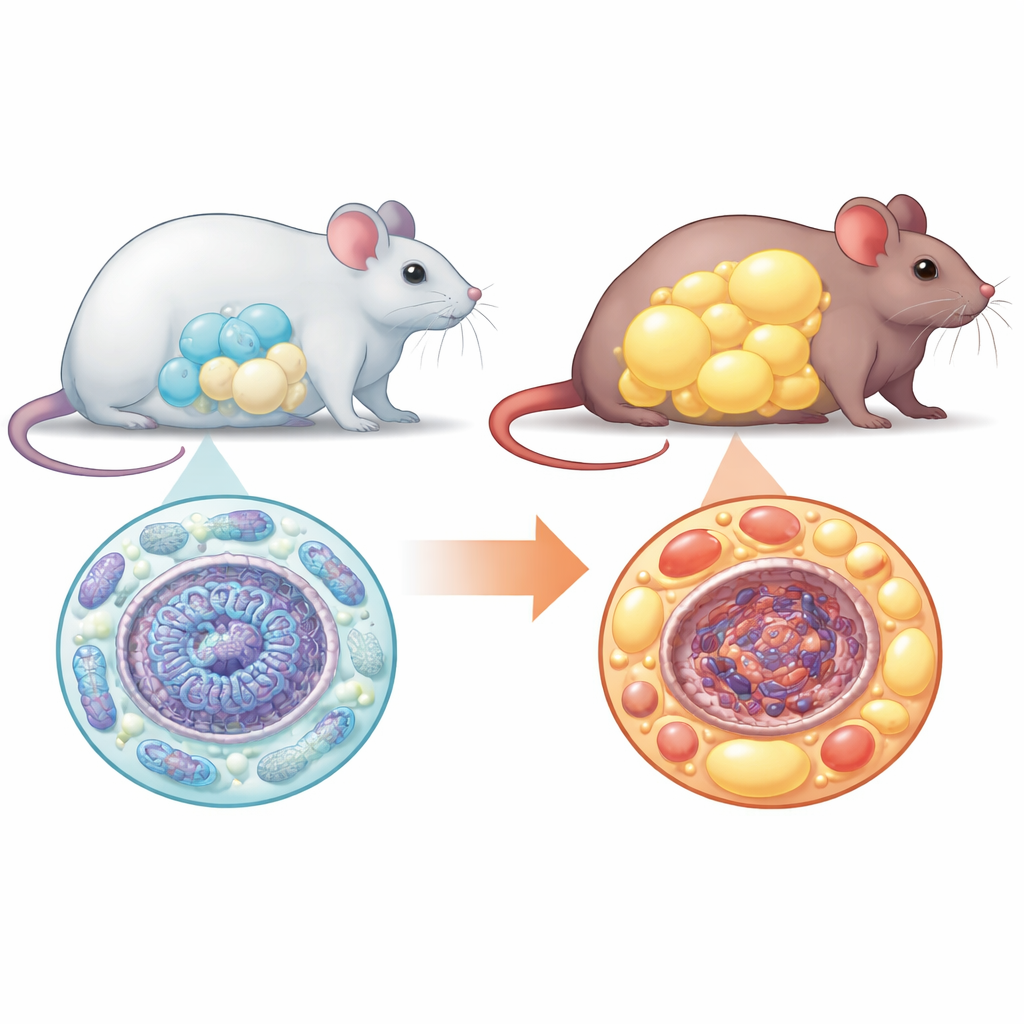
Från stamceller till fettceller
Fettceller utvecklas från mångsidiga föregångare som kallas mesenkymala stamceller. Normalt multiplicerar dessa föregångare sig, ändrar sitt energianvändande och mognar till många små, välfungerande fettceller som säkert lagrar överflödiga kalorier. Teamet fann att utan NM1 faller denna ordnade process samman. När de odlade stamceller från normala möss och från möss utan NM1 i laboratoriet och pressade dem att bli fettceller, fullföljde betydligt färre celler övergången i frånvaro av NM1. De celler som ändå mognade var märkbart större än normalt, fyllda med fett men saknade den vanliga signaturen av friska fettceller på gen- och proteinnivå. Detta mönster – färre celler men varje cell förstorad – är ett kännetecken för ohälsosam fettvävnad.
Hur genpackning formar fettcellers beteende
NM1 verkar i kärnan där det hjälper till att hålla DNA-stråk tillgängliga så att viktiga gener kan slås på. För att förstå hur dess förlust förändrar cellbeteende överlagrade forskarna kartor över öppna DNA-regioner med mätningar av genaktivitet i celler med och utan NM1. De såg att många gener som behövs för fettcellsbildning, hantering av fettdroppar och mitokondriellt underhåll förlorade både tillgänglighet och aktivitet när NM1 saknades. Samtidigt blev andra gener kopplade till tillväxt- och signalvägar mer öppna och mer aktiva. Detta pekade på NM1 som en viktig trafikledare: det hjälper till att upprätthålla ett balanserat landskap av öppna och stängda DNA-regioner så att rätt nätverk av gener driver sund fettcellsutveckling och ämnesomsättning.
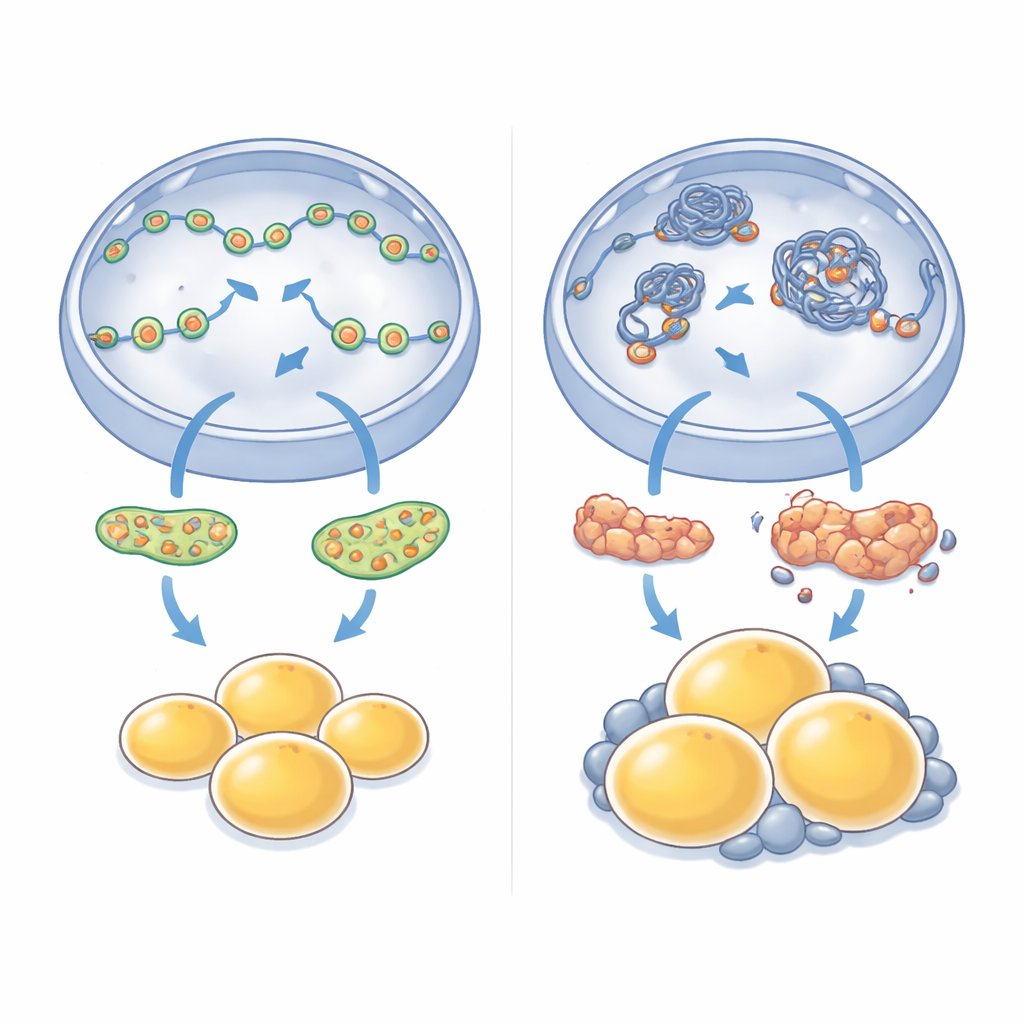
När lokala förändringar blir helkroppsviktökning
Konsekvenserna av att förlora denna enda kärnmotor stannade inte vid celler i ett odlingskärl. Möss som saknade NM1 blev gradvis tyngre än sina normala kullsyskon, trots att de inte åt mer mat. Avbildning och vävnadsanalys visade en tydlig ansamling av fett, särskilt runt inre organ i buken, och de enskilda fettcellerna i dessa områden var slående förstorade. När forskarna mätte vilka gener som var upp- eller nedreglerade i detta viscerala fett fann de omfattande förändringar: vägar involverade i energianvändning, insulinsignalering och vävnadsombyggnad var omprogrammerade. Gener som är förknippade med fettcellstillväxt och expansion var ofta uppreglerade, medan flera centrala regulatorer för sund fettcellsbildning dämpades, vilket speglade de defekter som sågs i odlade stamceller.
Inflammerat fett och störda energimaskiner
Bortom ren storlek visade fettvävnaden hos NM1‑deficienta möss tecken på inflammation och metabol stress. En detaljerad väg-analys framhöll stark aktivering av immunsignaler drivna av molekyler som interferon‑gamma och tumörnekrosfaktor, vilka är kända för att bidra till insulinresistens och metabola sjukdomar. Samtidigt undertrycktes regulatorer som stöder lugn, energieffektiv fettvävnad. Studien kopplade också NM1‑förlust till störda mitokondrier – cellens energimaskiner. Gener som normalt övervakar mitokondriell kvalitet och skiftet mellan effektiv energiproduktion och snabb glykolytisk energi var felreglerade, vilket tyder på att när NM1 saknas antar fettceller en mindre effektiv, mer stresskänslig energistrategi.
Delade signaler mellan möss och människor
För att undersöka om denna kärnmotorväg kan vara relevant för människor granskade författarna stora genetiska dataset från mänskligt visceralt fett. De fokuserade på en mänsklig motsvarighet till NM1 kallad MYO1C och tittade på nätverk av varianter som finjusterar aktiviteten hos närliggande gener. De fann att många av samma teman som observerats hos möss – cytoskelettkontroll, immunsignalering och metabol reglering – dök upp i mänskliga gennätverk centrerade kring MYO1C. Flera gener som förändrats i NM1‑deficient musfett var också inbäddade i dessa mänskliga nätverk och har kopplats till ombyggnad av fettvävnad och ämnesomsättning. Denna överlappning mellan arter tyder på att liknande kärnmekanismer kan påverka risken för fetma hos människor.
Vad detta betyder för fetma och metabol hälsa
Sammantaget visar arbetet att NM1 är mycket mer än en kärnhjälpare; det är en central nav som knyter DNA‑organisation till hur fettceller växer, lagrar energi och kommunicerar med immunsystemet. När NM1 saknas ställs genreglage i fettföregångare fel, mitokondrier fungerar dåligt, fettceller förstoras istället för att föröka sig, och visceralt fett blir inflammerat – en kombination som liknar den ohälsosamma fettbildning som ses vid fetma och insulinresistens. För en allmän läsare är budskapet att den fysiska ordningen av DNA och dess hjälpande proteiner inne i kärnan kan predisponera vävnader mot hälsosam eller skadlig fettutvidgning. Proteiner som NM1 och dess mänskliga motsvarighet MYO1C kan en dag bli mål för behandlingar som syftar till att omforma fettvävnad inifrån och ut och erbjuda ett mer precist sätt att angripa sjukdomar relaterade till fetma.
Citering: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
Nyckelord: adipogenes, kromatin, mitokondrier, visceralt fett, metabol inflammation