Clear Sky Science · sv
M2-makrofager främjar lymfatisk metastasering genom att reglera PKM2:s nukleära translokation i trippelnegativ bröstcancer
Varför denna forskning är viktig
För personer som diagnostiserats med trippelnegativ bröstcancer är en av de största farhågorna att cancern ska sprida sig till närliggande lymfkörtlar, ett avgörande steg mot spridning i hela kroppen. Denna studie undersöker hur vissa immunceller som borde skydda oss i stället hjälper denna typ av bröstcancer att invadera lymfsystemet, och identifierar en molekylär ”omkopplare” som kan vara måltavla för läkemedel för att bromsa eller stoppa denna spridning.
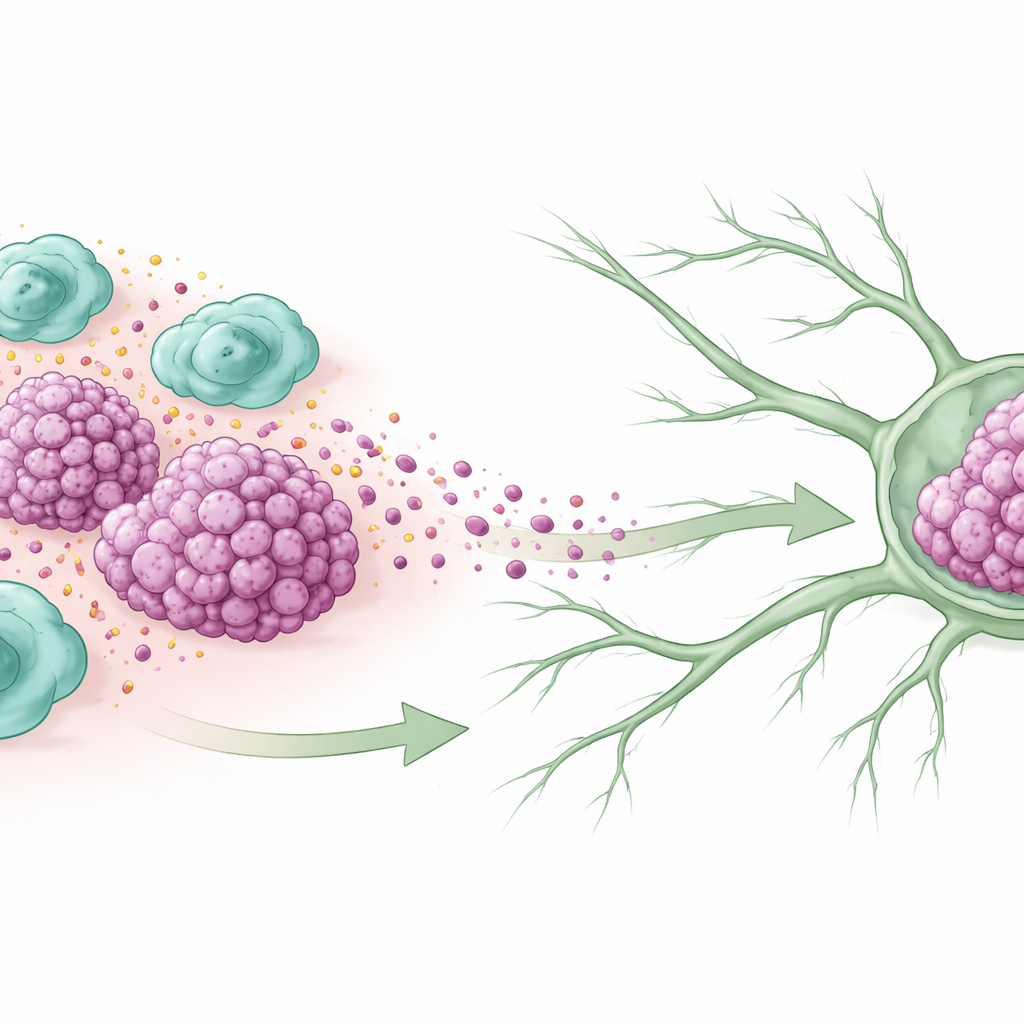
Immuna medhjälpare som blir medbrottslingar
Inuti många tumörer samlas immunceller kallade makrofager i stora antal. Vissa antar ett vårdande, sår-läkande läge känt som M2-tillståndet, vilket i cancer ofta slutar med att de hjälper tumörer istället för att bekämpa dem. Forskarna undersökte vävnad från kvinnor med trippelnegativ bröstcancer och fann att tumörer som redan spridit sig till lymfkörtlar innehöll betydligt fler av dessa M2-typ makrofager. Patienter vars tumörer var fyllda med dessa celler tenderade att ha större cancer, mer aggressiva egenskaper och kortare överlevnad, vilket tyder på att dessa ”vänskaplig eld”-immunceller är nära kopplade till att cancern förvärras.
Bygger nya lymf-”motorvägar” för cancerceller
Cancerceller når vanligtvis inte lymfkörtlar av en slump; de färdas ofta längs nybildade lymfkärl, små kanaler som dränerar vätska från vävnader. I denna studie hade tumörer rika på M2-makrofager också fler av dessa lymfkärl genomvävda i sig. I odlingsskålar, när bröstcancerceller växte i närvaro av M2-makrofager, utsöndrade de signaler som fick mänskliga lymfatiska celler att bilda rörliknande nätverk och migrera snabbare, vilket efterliknar tillväxten av nya lymfkanaler. I möss producerade cancerceller som exponerats för M2-makrofager fler lymfkärl i tumören och oftare metastaser till närliggande lymfkörtlar, vilket bekräftar att dessa immunceller aktivt hjälper till att konstruera flyktvägar.
Den dolda signalvägen inne i cancercellerna
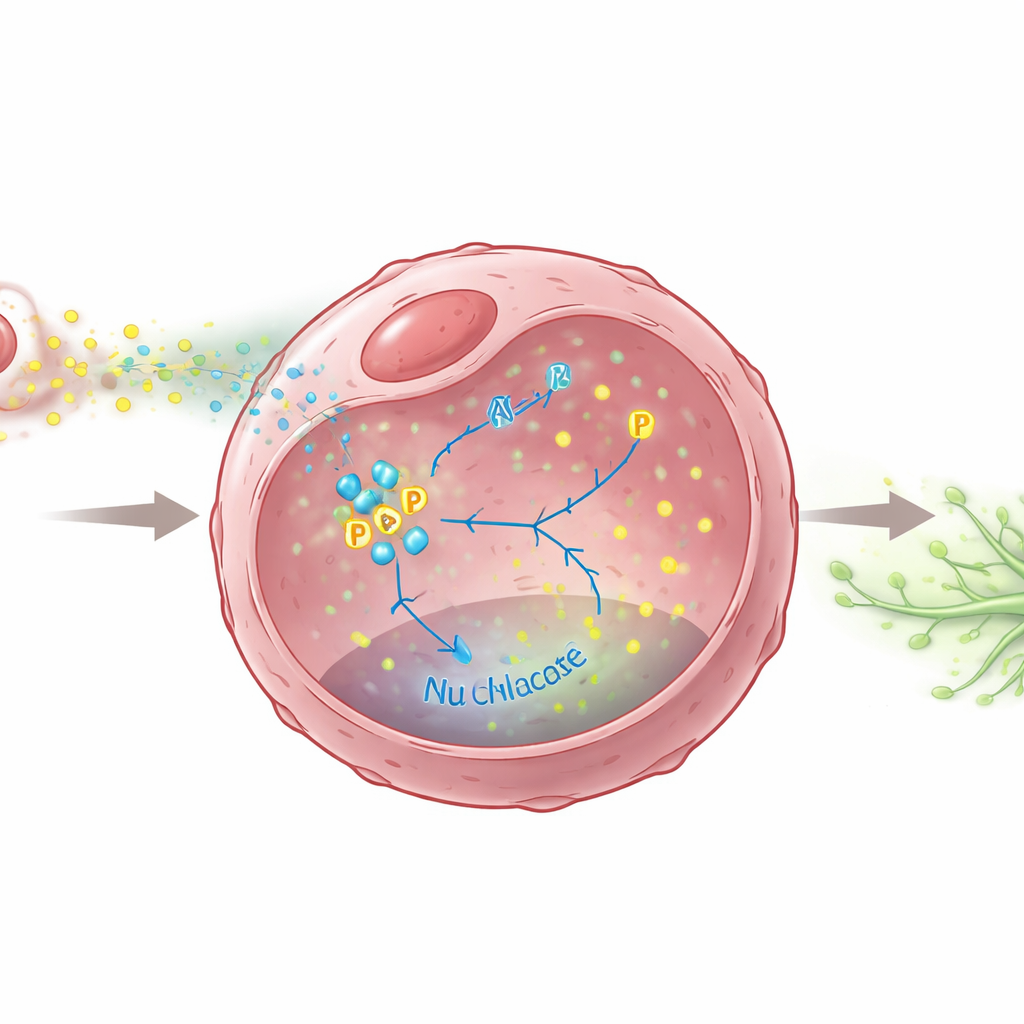
Teamet frågade sig sedan vilka kemiska budskap M2-makrofager skickar för att skjuta tumörer mot lymfatisk spridning. De identifierade en välkänd molekyl, TGF-β, som frisätts i högre mängder av M2-makrofager. Denna signal fick bröstcancerceller att öka produktionen av två tillväxtfaktorer, VEGFC och VEGFD, som är kraftfulla drivkrafter för lymfkärlstillväxt. Avgörande visade forskarna att ett metaboliskt enzym inne i cancerceller, PKM2, fungerar som en central omkopplare i denna process. Vid stimulering med TGF-β ökar PKM2 inte bara cellens sockerförbränning utan blir också kemiskt modifierat och förflyttar sig in i nukleus, där det hjälper till att slå på generna för VEGFC och VEGFD. Utan PKM2, eller när dess förflyttning till kärnan blockerades, producerade cancerceller mycket mindre av dessa lymftillväxtsignaler och hade sämre förmåga att stimulera lymfkärlsbildning.
Test av en möjlig broms på spridning
Eftersom PKM2 sitter vid denna avgörande korsväg mellan ändrad metabolism och pro-metastatisk signalering testade forskarna om att stänga ner det kunde sakta den lymfatiska spridningen. De använde shikonin, en förening som stör PKM2:s aktivering och inträde i kärnan. I cellexperiment minskade shikonin kraftigt nivåerna av VEGFC och VEGFD och försvagade cancercellernas utsöndringars förmåga att inducera lymfkärlstillväxt och migration. I musmodeller minskade behandling med shikonin både antalet och storleken av lymfkörtelmetastaser och reducerade tätheten av lymfkärl i tumörerna, utan uppenbara toxiska effekter på djuren. Dessa fynd tyder på att blockering av PKM2 samtidigt kan svälta cancerceller på vissa metabola fördelar och dämpa deras förmåga att omforma lymfsystemet till sin fördel.
Vad detta betyder för patienter
Sammantaget föreslår studien en tydlig händelsekedja: M2-makrofager i trippelnegativa brösttumörer utsöndrar TGF-β, som vrider PKM2 inne i cancerceller till en dubbel roll—drivande hög sockerkonsumtion och agerande i kärnan för att slå på VEGFC och VEGFD. Dessa faktorer stimulerar sedan tillväxten av lymfkärl som cancerceller använder för att nå lymfkörtlar och längre bort. Genom att identifiera PKM2 som en kritisk knutpunkt i denna kedja föreslår arbetet nya sätt att förutsäga och potentiellt behandla lymfatisk spridning, särskilt hos patienter vars tumörer visar höga nivåer av M2-makrofager, PKM2 eller VEGFC/D. Även om fler tester på människor krävs, kan riktning mot denna väg hjälpa till att återställa lymfsystemet från en cancermotorväg till en barriär.
Citering: Yang, Y., Ye, H., Zhong, D. et al. M2 macrophages promote lymphatic metastasis by regulating PKM2 nuclear translocation in triple-negative breast cancer. Cell Death Dis 17, 262 (2026). https://doi.org/10.1038/s41419-026-08524-4
Nyckelord: trippelnegativ bröstcancer, lymfkörtelmetastas, tumörassocierade makrofager, PKM2, lymfangiogenes