Clear Sky Science · sv
Deubiquitinase UCH-L1 ger paclitaxelresistens genom att stabilisera PKM2 för att främja glykolys i trippelnegativ bröstcancer
Varför denna forskning spelar roll för patienter
Kemoterapi är fortfarande ett av få alternativ för personer med trippelnegativ bröstcancer, en aggressiv form av sjukdomen som saknar vanliga läkemedelsmål. Ändå lär sig många tumörer så småningom att avvärja kraftfulla läkemedel som paclitaxel, vilket gör att cancern kan återkomma och sprida sig. Denna studie avslöjar en dold koppling inne i cancerceller som hjälper dem att motstå paclitaxel genom att omprogrammera hur de förbränner socker, och pekar på en ny svaghet som framtida behandlingar skulle kunna utnyttja för att få kemoterapi att fungera längre.
En svårbehandlad bröstcancer
Trippelnegativ bröstcancer definieras av vad den saknar: den uttrycker varken östrogen- eller progesteronreceptorer, eller HER2-växtfaktorn som många moderna läkemedel riktar sig mot. Därför är standardkemoterapi fortfarande huvudbehandlingen. Paclitaxel är ett sådant arbetsdjur som används världen över. En betydande andel patienter svarar dock inte väl från början eller utvecklar resistens över tid, vilket leder till tumöråterfall och sämre överlevnad. Kliniskt har man länge sett detta mönster men saknat tydliga markörer som kan förutsäga vilka tumörer som kommer att bli resistenta mot paclitaxel och vilka molekylära omkopplare som driver den resistensen.
Ett nervprotein dyker upp i brösttumörer
Forskarna fokuserade på ett protein kallat UCH‑L1, bäst känt för sin roll i nervceller och hjärnsjukdomar. Genom att gräva i offentliga cancer-databaser och undersöka tumörprover från patienter med trippelnegativ bröstcancer fann de att nivåerna av UCH‑L1 var mycket högre i dessa tumörer än i normal bröstvävnad. Patienter vars tumörer hade mer UCH‑L1 tenderade att ha kortare överlevnad och drog sig mindre nytta av kemoterapi, särskilt paclitaxel eller besläktade läkemedel. I laboratorieodlade cancercellinjer gjorde ökade nivåer av UCH‑L1 cellerna svårare att döda med paclitaxel, medan minskad UCH‑L1 hade motsatt effekt, både i odlingsskålar och i musmodeller. 
Cancercellernas sockersug och läkemedelsresistens
Cancerceller föredrar ofta ett snabbt men ineffektivt sätt att förbränna socker, känt som aerob glykolys eller Warburg-effekten. Denna sockerdrivna metabolism levererar snabb energi och byggstenar för tillväxt och har kopplats till resistens mot många behandlingar. När teamet jämförde cancerceller med och utan UCH‑L1 observerade de tydliga förändringar i detta metaboliska beteende. Celler med mindre UCH‑L1 konsumerade mindre glukos, producerade mindre laktat och genererade mindre cellulär energi, medan celler med extra UCH‑L1 visade motsatt mönster och en starkare försurning kopplad till glykolys. Viktigt är att när de blockerade glykolys med en förening kallad 2‑DG försvann till stor del UCH‑L1:s skyddande effekt mot paclitaxel. Det visade att UCH‑L1 hjälper cancerceller att överleva kemoterapi till stor del genom att öka deras sockerförbränningsmaskineri.
En proteinpartnerskap som skyddar tumörens bränsle
Vidare sökte forskarna efter direkta partnerproteiner till UCH‑L1 inne i cellen och inriktade sig på PKM2, ett nyckelenzym vid en avgörande knutpunkt i glykolysvägen. Normalt regleras PKM2-nivåer av en cellulär återvinningsmärkning kallad ubiquitin, som markerar proteiner för nedbrytning. UCH‑L1 är ett ”av-märkande” enzym som kan avlägsna ubiquitin. Studien visade att UCH‑L1 fysiskt binder till svansregionen av PKM2 och specifikt avlägsnar en typ av ubiquitinkedja som skickar PKM2 till cellens sophanteringssystem. Genom att kapa dessa kedjor vid en särskild plats på PKM2 förhindrar UCH‑L1 dess nedbrytning och stabiliserar enzymet. Med mer PKM2 närvarande går glykolysen varmare, vilket matar tumören och hjälper den att klara stressen av paclitaxelbehandling. 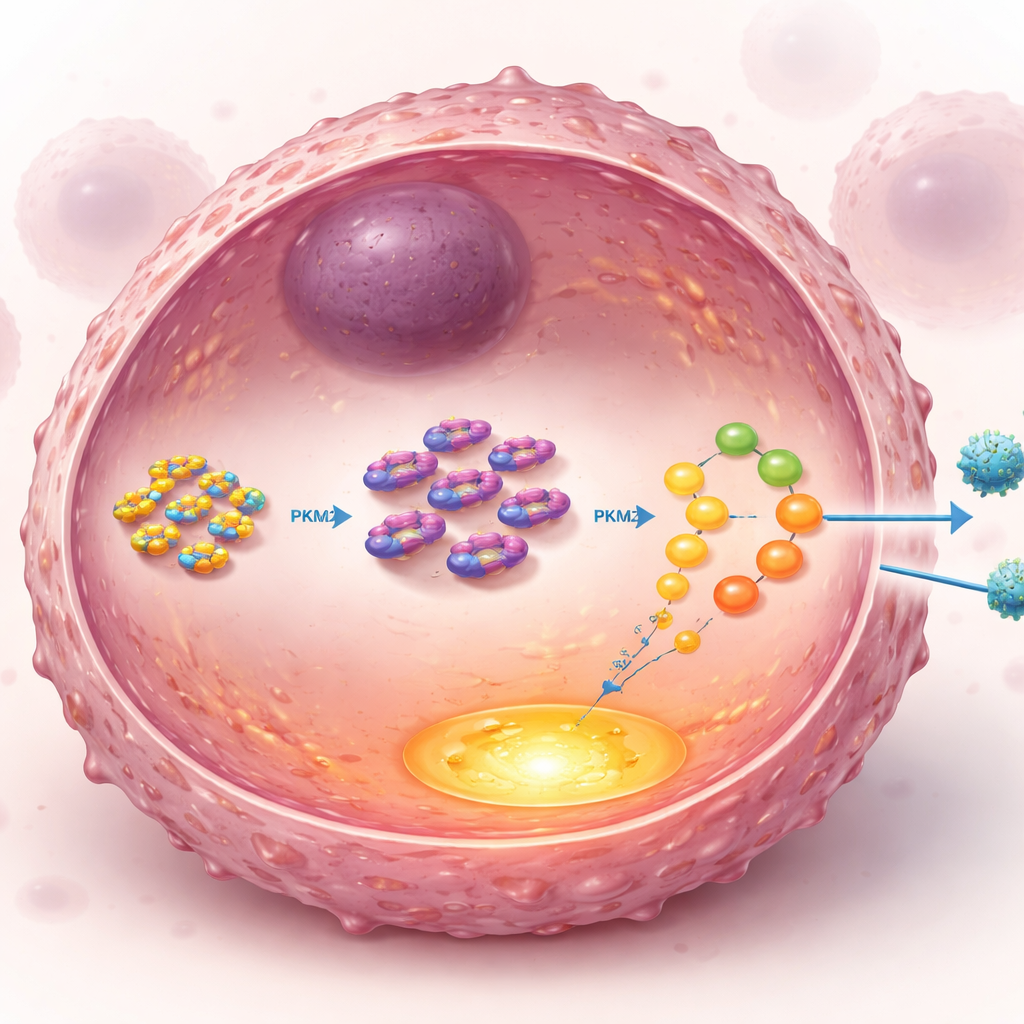
Att vända resistens i envisa tumörer
Teamet vände sig sedan till paclitaxelresistenta trippelnegativa bröstcancerceller, både från patienthärledda dataset och från laboratoriemodeller. I dessa resistenta celler var både UCH‑L1 och PKM2 uppreglerade, och glykolysen var förhöjd. Att tysta UCH‑L1 eller PKM2, eller kemiskt blockera glykolys, gjorde dessa hårdnackade celler återigen sårbara för paclitaxel, återställde celldöd och krympte tumörer i möss. Återinförande av PKM2 i UCH‑L1‑utarmade tumörer utplånade mycket av denna fördel, vilket understryker att PKM2 är den viktiga nedströmsaktören i denna resistenskrets. I patienttumörprover förekom UCH‑L1 och PKM2 ofta höga tillsammans, och hög PKM2 var också kopplat till sämre utfall efter kemoterapi.
Vad detta betyder för framtida behandling
För icke-specialister är budskapet att vissa trippelnegativa bröstcancerformer överlever paclitaxel genom att öka en sockerförbrännande motor som drivs av ett samarbete mellan UCH‑L1 och PKM2. UCH‑L1 fungerar som en skyddande mekaniker som hindrar PKM2 från att brytas ner, vilket gör att cancerceller kan generera mer energi och motstå skador orsakade av kemoterapi. Att mäta UCH‑L1 eller PKM2 i tumörer kan hjälpa till att förutsäga hur väl en patient kommer att svara på paclitaxel, och läkemedel som hämmar UCH‑L1, PKM2 eller glykolys kan en dag kombineras med standardkemoterapi för att övervinna eller förebygga resistens och förbättra prognosen för personer med denna svåra cancer.
Citering: Chen, X., Zhou, X., Meng, Y. et al. Deubiquitinase UCH-L1 confers paclitaxel resistance via stabilizing PKM2 to promote glycolysis in triple-negative breast cancer. Cell Death Dis 17, 261 (2026). https://doi.org/10.1038/s41419-026-08521-7
Nyckelord: trippelnegativ bröstcancer, paclitaxelresistens, tumörmetabolism, glykolys, PKM2