Clear Sky Science · sv
Trimetylering av histon 3 lysin 36 av SETD2 formar ett epigenetiskt landskap i tarmstamceller för att orkestrera lipidmetabolism och dämpa cellsenesens
Varför tarmstamceller är viktiga när vi blir äldre
Längst inne i tarmens slemhinna arbetar små stamceller dygnet runt för att förnya den vävnad som hjälper oss att bryta ner mat och ta upp näringsämnen. När vi åldras blir dessa stamceller slitna, vilket gör tarmen mer sårbar för sjukdom och långsammare att läka. Denna studie undersöker hur subtila kemiska markörer på DNA-packande proteiner hjälper till att hålla tarmstamceller ungdomliga, hur deras försvinnande stör fettoxidationen i cellerna, och hur noga utvalda läkemedel möjligen en dag kan bromsa denna nedgång.
Åldrande celler i en krävande miljö
Tarmens inre yta är en av kroppens snabbast förnyande vävnader. Stamceller som ligger vid botten av små fickor, så kallade kryptor, delar sig för att ersätta miljarder celler var några dagar. Detta konstanta arbete kräver ett stabilt energitillskott, mycket av det från nedbrytning av fetter. Samtidigt styrs dessa stamceller av en ”epigenetisk” kod—kemiska märkningar på histonproteiner som hjälper bestämma vilka gener som är aktiva eller tysta. Författarna fokuserade på en sådan markör, känd som H3K36-trimetylering, som skapas av enzymet SETD2, och frågade om förändringar i denna markör kan förklara varför tarmstamceller förlorar sin kraft med åldern.
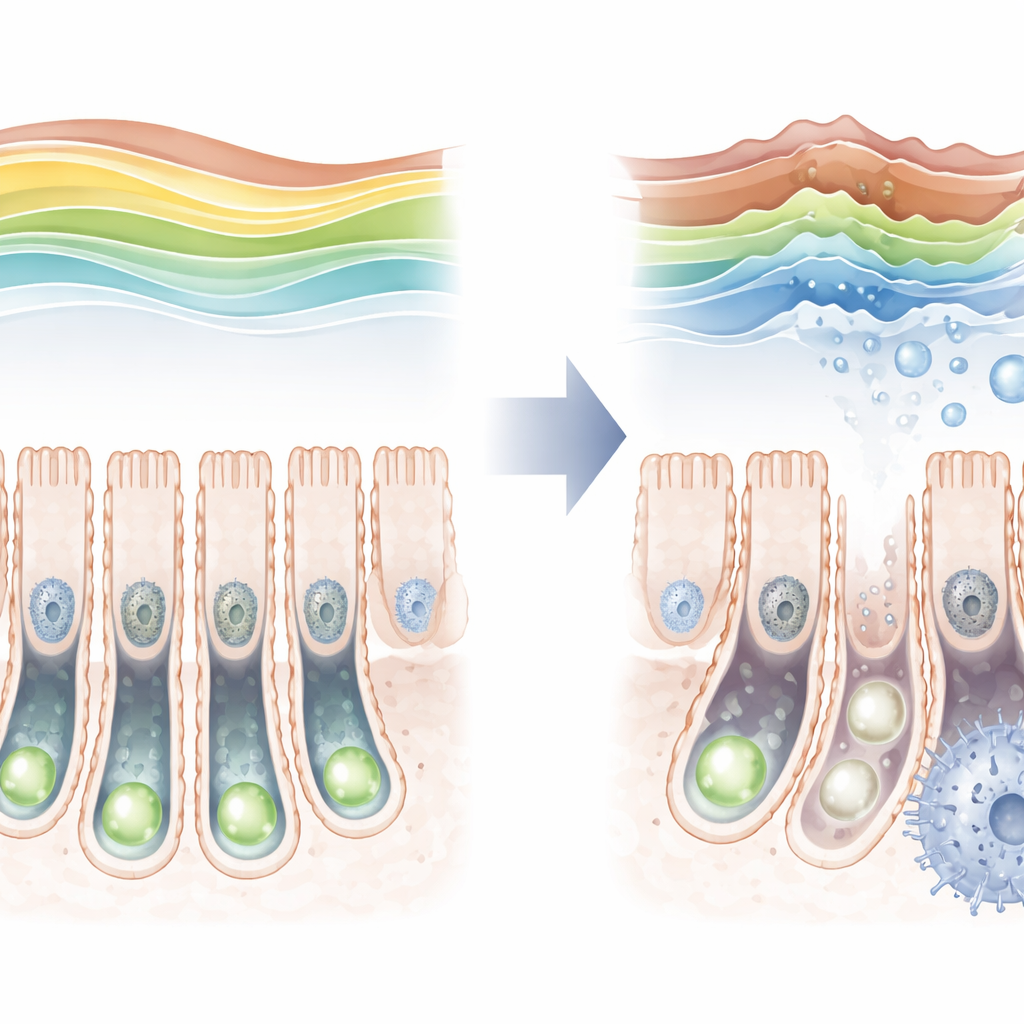
En skyddande markör som bleknar med åldern
Genom att undersöka möss tarmar över livsloppet fann forskarna att H3K36-trimetyleringen inte är statisk. Den är relativt låg direkt efter födseln, stiger till en topp hos unga vuxna för att sedan falla igen i hög ålder. När denna markör minskade hos äldre djur ökade samtidigt markörer för cellulärt åldrande i stamcellerna, vilket antyder en koppling mellan dem. För att testa detta mer direkt konstruerade teamet möss där SETD2 kunde tas bort endast i tarmstamceller. När detta enzym raderades försvann den skyddande markören nästan helt, stamceller delade sig mer sällan och de hade svårt att producera det fulla spektrum av specialiserade tarmcellstyper.
Hur epigenetiska förändringar spårar ur fettoxidationen
Förlusten av denna enda histonmarkör utlöste en kaskad av förändringar i stamcellerna. Mätningar av genaktivitet visade att många gener involverade i cellcykeln och DNA-replikation nedreglerades, medan gener kopplade till stress och åldrande uppreglerades. Slående nog pekade det starkaste signalen mot störd lipidhantering: gener som normalt stöder beta-oxidation av fettsyror—den kontrollerade förbränningen av fett för energi—dämpades, och fett började ansamlas i kryptorna. Metabolitprofiler bekräftade att långkedjiga fettsyror ackumulerades, ett tecken på att de vanliga fettbearbetningsvägarna sviktade. Samtidigt förändrades det fysiska paketerandet av DNA i kärnan, där många regioner blev mer exponerade eller mer tätt slutna, vilket omformade vilka gener cellen lätt kunde använda.
Kromatinremodellerare och marschen mot senescens
För att förstå hur dessa förändringar i DNA-packningen uppstår kartlade författarna både öppna kromatinregioner och en uppsättning andra histonmarkörer över genomet. När H3K36-trimetyleringen försvann, fick stora DNA-sträckor ”aktiva” markörer och blev mer tillgängliga, särskilt nära gener kopplade till metabolism och åldrande. En nyckelspelare i denna övergång var SWI/SNF-kromatinremodelleringskomplexet, drivet av en kärnsubenhet kallad SMARCA4. I stamceller utan SETD2 steg SMARCA4-nivåerna, och komplexet verkade hjälpa till att öppna regioner som driver senescensprogram. När forskarna minskade SMARCA4-aktiviteten genetiskt eller med en riktad hämmare återfick stamceller delvis sin förmåga att bilda friska mini-tarmar i odlingsskålar, och åldersmarkörer minskade—vilket tyder på att överdriven ombyggnad skjuter dessa celler mot ett utmattat, senescent tillstånd.
Återväcka energivägar för att rädda stamceller
Eftersom störd fettoxidation framträdde som ett centralt problem testade teamet om förstärkning av denna väg kunde motverka stamcellsåldrandet. De använde ett läkemedel som aktiverar PPARα, en huvudreglerare av beta-oxidation. I organoider odlade från SETD2-bristfälliga stamceller ökade behandlingen tillväxten, återställde de knoppande strukturer som kännetecknar kraftfulla stamceller och minskade fettansamling. I levande möss återfyllde samma intervention delvis stamcellsförrådet, sänkte markörer för senescens och normaliserade lipiduppbyggnaden i tarmkryptorna. Dessa fynd placerar beta-oxidation som en avgörande länk mellan epigenetisk kontroll och stamcellshälsa.
Vad detta betyder för ett hälsosamt åldrande
Sammantaget visar arbetet att en specifik histonmarkör, insatt av SETD2, hjälper till att upprätthålla ett balanserat epigenetiskt landskap i tarmstamceller. När denna markör bleknar blir kromatinet abnormt ombyggt, fettförbränningsvägar sviktar, lipider ansamlas och celler driver in i senescens, vilket försvagar tarmens reparationssystem. Genom att antingen dämpa det överaktiva remodelleringsmaskineriet eller återställa fettmetabolismen med riktade läkemedel kan det bli möjligt att bevara stamcellsfunktionen och tarmhälsan senare i livet. Även om dessa rön kommer från möss, speglar de mönster som ses vid mänskliga tarmsjukdomar, vilket ger möjligheten att noggrant anpassade metaboliska terapier en dag skulle kunna hjälpa till att motverka åldersrelaterad nedgång i våra egna tarmstamceller.
Citering: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
Nyckelord: tarmstamceller, epigenetik, beta-oxidation av fettsyror, cellulär senescens, SETD2