Clear Sky Science · sv
En Lamp2a-länkad RNA utsöndrad av ADSC:er förhindrar ENO1–laktylation–glykolys-återkoppling och cellernas maligna beteende vid trippelnegativ bröstcancer
Varför detta spelar roll för patienter
Trippelnegativ bröstcancer är en av de mest aggressiva formerna av bröstcancer och saknar hormon- eller tillväxtfaktormål som gör andra subtyper mer behandlingsbara. Denna studie avslöjar hur dessa tumörer omkopplar sin energianvändning för att överleva i lågsyremiljöer och beskriver ett uppfinningsrikt sätt att angripa den omkopplingen. För läsaren erbjuder den en inblick i hur förståelsen av cancermetabolism kan leda till nya, mycket riktade terapier som skiljer sig markant från traditionell kemoterapi.
Hur dessa tumörer driver sig själva
Många cancerformer förlitar sig i hög grad på ett snabbt men ineffektivt sätt att skapa energi kallat glykolys, som omvandlar socker till biprodukten laktat. Genom att granska patientprover, offentliga genbanker och flera bröstcancercellinjer visar forskarna att trippelnegativa tumörer förlitar sig ännu mer på glykolys än andra bröstcancerformer. Ett nyckelenzym i denna väg, ENO1, finns i särskilt höga nivåer i dessa tumörer och är kopplat till sämre överlevnad. När ENO1-nivåerna minskades i labbodlade trippelnegativa celler skiftade cellerna från glykolys mot mer normal energiproduktion i mitokondrierna, växte långsammare och var mindre benägna att invadera eller bilda kolonier.
En farlig återkopplingsslinga inne i cancerceller
När teamet grävde djupare upptäckte de att laktat självt stärker ENO1 och låser cancerceller i en ond cirkel. Laktat kan kemiskt modifiera proteiner i en process kallad laktylation. I trippelnegativa celler ökade extra laktat laktylationen av ENO1, vilket i sin tur ökade enzymets aktivitet och stabilitet, accelererade glykolysen ytterligare och producerade ännu mer laktat. Under lågsyreförhållanden—typiska för solida tumörer—blev denna loop starkare, vilket hjälpte cancerceller att motstå celldöd och fortsätta proliferera. Att blockera ENO1:s aktivitet med en liten molekylinhibitor eller att reducera laktatproduktionen försvagade denna loop, dämpade glykolysen och bromsade tumörtillväxt hos möss.
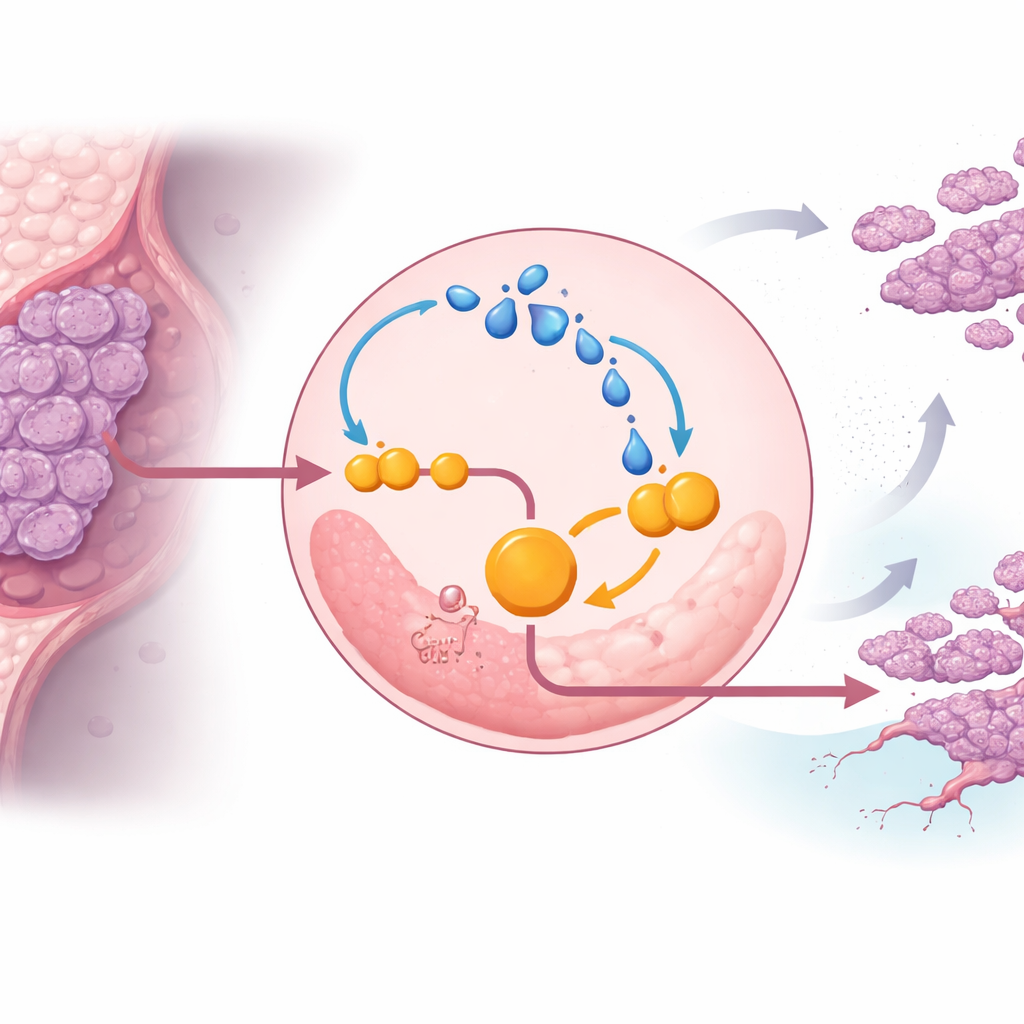
Den molekylära strömbrytaren som skyddar ENO1
Studien identifierade en specifik kontrollpunkt på ENO1 som möjliggör denna loop. Ett protein känt som EP300 lägger till laktatbaserade märkningar på flera lysinplatser på ENO1, där en plats, benämnd K262, visade sig vara avgörande. När denna plats muterades så att den inte längre kunde laktyleras transporterades ENO1 snabbt till cellens återvinningscentraler, lysosomerna, och bröts ner. Utan detta skyddande märke förlorade trippelnegativa celler mycket av sin glykolytiska drivkraft och sin förmåga att bilda tumörer och metastaser i djurmodeller. Detta pekar ut laktylation av ENO1 vid K262 som en molekylär brytare som skyddar enzymet från nedbrytning och upprätthåller tumorns omställda metabolism.
Ett nytt sätt att märka ENO1 för nedbrytning
I stället för att bara blockera ENO1 utformade författarna en strategi för att selektivt avlägsna det från cancerceller. ENO1 fungerar också som ett RNA-bindande protein och känner igen specifika korta RNA-sekvenser. Teamet konstruerade syntetiska RNA-bitar som binder ENO1 starkt och kopplade dem till Lamp2a, ett lysosomalt membranprotein som är involverat i riktad proteinnedbrytning. Människans fettframställda stamceller modifierades genetiskt för att producera detta RNA–Lamp2a-par och paketera det i små vesiklar kallade exosomer. När dessa konstruerade exosomer tillsattes till trippelnegativa celler fäste RNA-delen vid ENO1, medan Lamp2a-delen styrde hela komplexet in i lysosomerna, där ENO1 bröts ner även om det bar det stabiliserande laktylationsmärket.
Test av den riktade nedbrytningsmetoden i djur
För att föra denna idé närmare en praktisk terapi odlade forskarna de modifierade stamcellerna på ett biologiskt nedbrytbart byggnadsstöd och implanterade konstruktionen under huden på möss, nära trippelnegativa tumörer. Från denna plats släppte stamcellerna kontinuerligt ut exosomer som bar ENO1‑inriktade komplex. Tumörer hos dessa möss visade markant lägre ENO1-proteinnivåer, minskad glykolys, färre delande celler och fler tecken på celldöd jämfört med kontrollgrupper. Tumörerna växte långsammare och deras maligna beteende var tydligt dämpat, vilket visar att riktning av ENO1 till lysosomer effektivt kan beröva cancern dess föredragna bränsleväg.
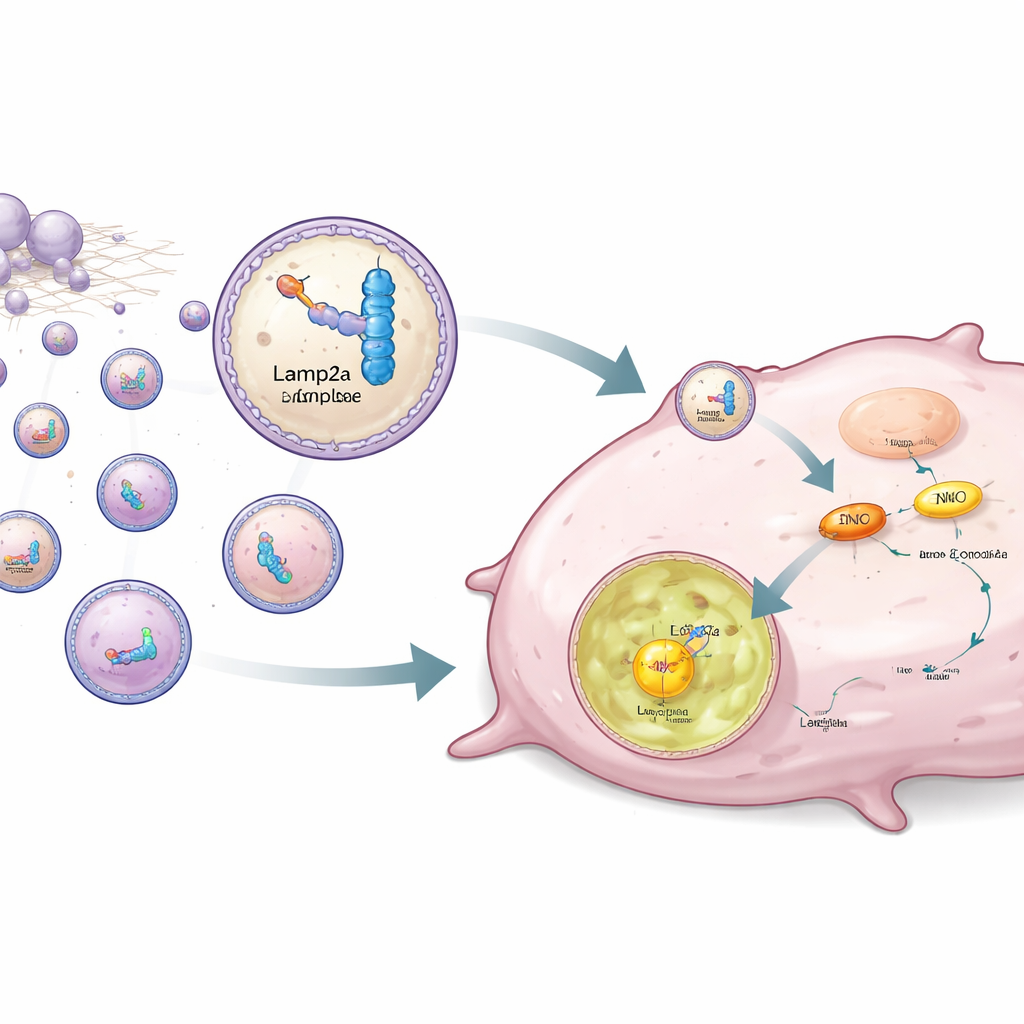
Vad detta kan betyda för framtida behandling
För en icke-specialist är huvudbudskapet att detta arbete avslöjar både en svaghet och en potentiell ny behandlingsvinkel för trippelnegativ bröstcancer. Svagheten är tumörens beroende av en självförstärkande energiloop byggd kring ENO1 och laktat, särskilt i lågsyreområden. Behandlingsidén är ett riktat system för proteinnedbrytning som använder skräddarsydd RNA och stamcells‑deriverade exosomer för att dra ENO1 in i cellens avfallshantering. Trots att metoden ligger långt från klinisk användning illustrerar den hur djup förståelse av cancerens metabola knep kan inspirera precisa terapier som syftar till att avväpna, snarare än enbart förgifta, maligna celler.
Citering: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
Nyckelord: trippelnegativ bröstcancer, cancermetabolism, laktatsignalering, riktad proteinnedbrytning, ENO1-enzymet