Clear Sky Science · sv
Fosfatasen Shp1 reglerar CXCR2-proteinstabilitet och IL8-medierad invasivitet vid bröstcancer
Varför denna forskning är viktig för bröstcancer
Bröstcancer är fortfarande en av de ledande orsakerna till cancerrelaterad dödlighet hos kvinnor, främst eftersom vissa tumörer blir invasiva och sprider sig till avlägsna organ. Denna studie förklarar hur en vanlig inflammatorisk signal i tumörer, kallad IL8, kommunicerar med bröstcancerceller och hur ett molekylärt "broms"-protein som heter Shp1 hjälper avgöra om dessa celler stannar kvar eller blir mer aggressiva. Att förstå detta molekylära dragkamp kan öppna nya vägar för att sakta eller stoppa spridningen av svårbehandlade bröstcancerformer, särskilt trippelnegativ sjukdom.
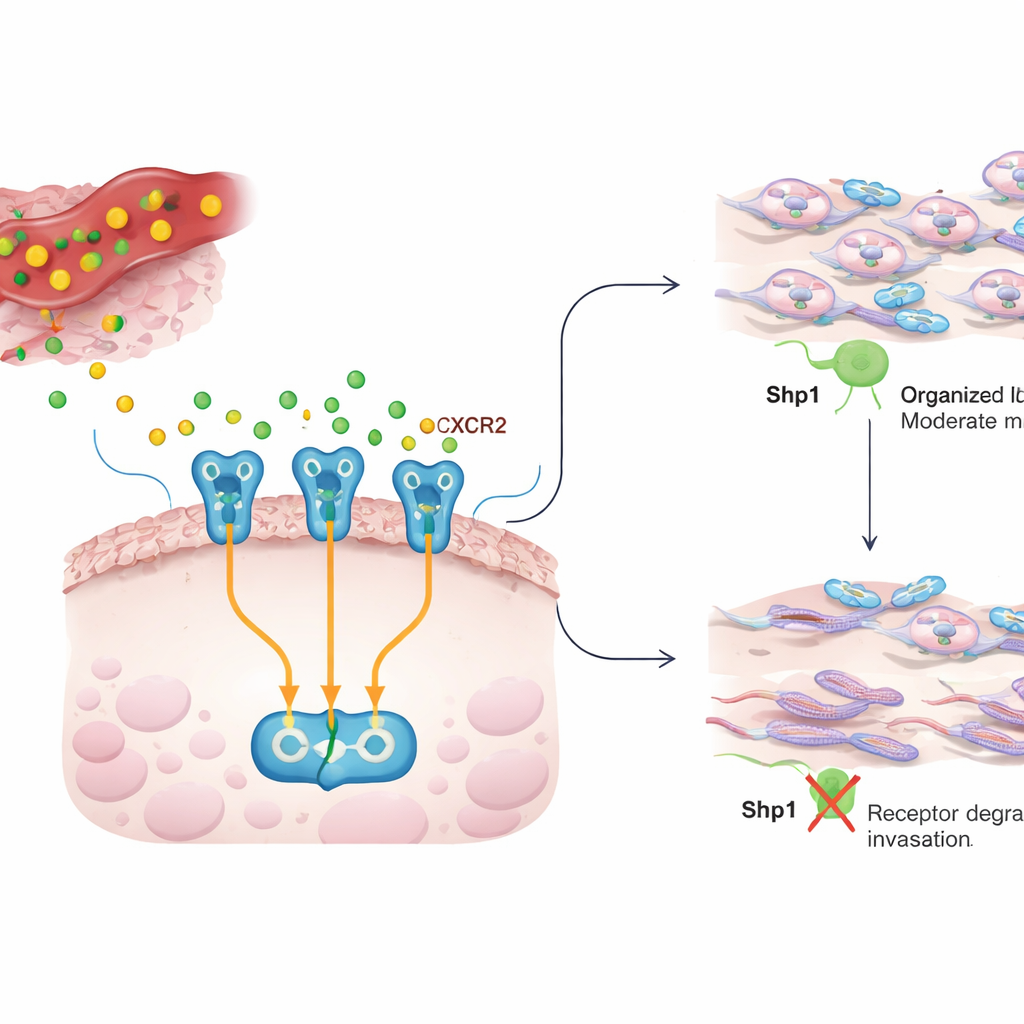
En konversation mellan inflammation och cancerceller
Inne i en tumör omges cancerceller av immunceller och stödjeceller som frigör kemiska budbärare, cytokiner. IL8 är en sådan budbärare och förekommer ofta i höga nivåer i många cancerformer, där den driver tillväxt, blodkärlsbildning och cancercellers förmåga att röra sig och invadera. IL8 signalerar via en receptor på cancercellens yta som kallas CXCR2. När IL8 binder CXCR2 aktiverar det flera interna kaskader som omorganiserar cellens skelett och gör det lättare för celler att krypa genom vävnad och spridas. Det aktuella arbetet frågar hur denna IL8–CXCR2-konversation hålls i schack, och om Shp1, ett enzym som vanligen ses som en tumörsuppressiv broms på tillväxtsignaler, också påverkar detta invasiva beteende.
Shp1s dolda roll i cellrörelse
Forskarna avlägsnade först eller kemiskt blockerade Shp1 i en vanligt använd luminal bröstcancellinje (MCF7) och mätte hur väl cellerna kunde migrera och invadera genom ett gel som efterliknar vävnad. Utan Shp1 slöt cancercellerna sår snabbare och pressade sig igenom gelen två till tre gånger effektivare, vilket visar att Shp1 normalt hämmar rörelse. Med hjälp av patientdata fann de också att kvinnor vars tumörer uttryckte mindre Shp1 hade sämre överlevnad och kortare tid till återfall. Tillsammans tyder dessa resultat på att Shp1 begränsar bröstcancercellers aggressiva beteende och att förlust av denna broms kopplas till sämre utfall.
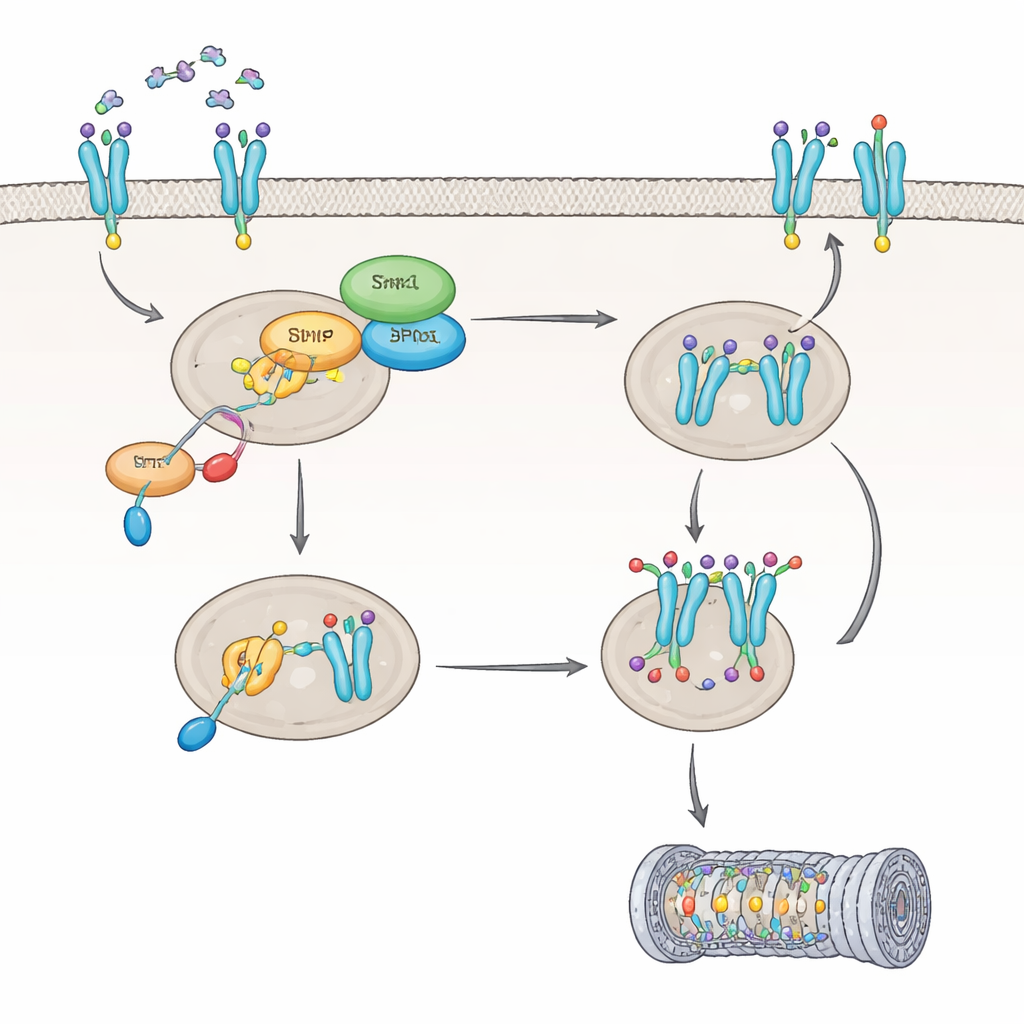
Hur IL8 slår av Shp1 och omprogrammerar en nyckelreceptor
Därefter undersökte gruppen hur IL8 påverkar Shp1 självt. De upptäckte att IL8 aktiverar ett protein kallat PKC, som märker Shp1 vid en specifik plats och sänker dess enzymatiska aktivitet med cirka 60 procent. När Shp1 dämpas på detta sätt blir ett annat enzym, PP2A, mindre aktivt, och CXCR2-receptorn förblir i ett kraftigt modifierat tillstånd som ändrar dess öde i cellen. Istället för att rensas upp och återanvändas till cellytan märks CXCR2 för nedbrytning, huvudsakligen via cellens proteinrivningsmaskineri, proteasomen. En specifik modifiering på CXCR2, vid aminosyran Ser347, visade sig vara avgörande för att fästa dessa nedbrytningsmärken. I celler som saknade Shp1 märktes och bröts CXCR2 ner snabbare, vilket ledde till färre receptorer på cellytan och en avtrubbad respons på IL8 över tid.
Olika bröstcancerformer, olika kopplingar
Bröstcancer är inte en enhetlig sjukdom; tumörer grupperas i luminala, HER2-positiva och trippelnegativa subtyper baserat på deras receptormönster. Forskarna testade IL8–CXCR2–Shp1-kretsen i flera cellinjer som representerar varje subtyp. I luminala och trippelnegativa celler aktiverade IL8 kaskaden Shp1–PP2A–CXCR2, och att blockera Shp1 ökade både den basala invasiviteten och utsläckte IL8:s sedvanliga pro-invasiva effekt. I kontrast svarade HER2-positiva celler fortfarande på IL8, men Shp1-blockad förändrade knappt deras beteende, vilket antyder att i dessa tumörer är Shp1 bundet till andra signaler, såsom HER2, och mindre tillgängligt för att reglera CXCR2. Storskaliga genuttrycksanalyser stödde denna bild: trippelnegativa linjer tenderade att ha lägre nivåer av Shp1, förändrad GPCR-relaterad signalering och högre IL8, i linje med en mer aggressiv, inflammationsdriven profil.
Vad detta innebär för framtida behandlingar
För en icke-specialist är huvudbudskapet att enzymet Shp1 fungerar som en trafikreglerare för IL8-receptorn CXCR2 och avgör om receptorn återanvänds eller förs till nedbrytning – och därigenom hur kraftigt bröstcancerceller kan svara på inflammatoriska signaler. I luminala och trippelnegativa bröstcancrar verkar denna kontrollpunkt vara särskilt viktig: när Shp1-nivåerna är låga eller dess aktivitet blockeras blir cellerna mer invasiva och patientutfallen försämras. Eftersom Shp1 kan förstärkas eller moduleras av vissa befintliga läkemedel kan riktade insatser mot Shp1–CXCR2-axeln, eventuellt tillsammans med IL8- eller CXCR2-hämmare, erbjuda en ny strategi för att begränsa invasion och metastasering i aggressiva bröstcancersubtyper.
Citering: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
Nyckelord: bröstcancerinvasion, IL8-signalering, CXCR2-receptor, Shp1-fosfatas, trippelnegativ bröstcancer