Clear Sky Science · sv
CRMP2 hämmar bildandet av metastaser genom att försvåra ILF3‑beroende stabilisering av CXCL10‑mRNA vid bröstcancer
Varför det är viktigt att stoppa cancer‑spridning
De flesta dödsfall i samband med bröstcancer beror inte på den ursprungliga tumören utan på att cancerceller tar sig till vitala organ, till exempel lungorna, och bildar nya tumörer. Denna studie avslöjar ett inbyggt skyddsprotein i bröstcancerceller som kan sakta ner eller till och med blockera denna spridning genom att förändra den ”välkomstmatta” som avlägsna organ lägger ut för vandrande cancerceller. Att förstå denna dolda säkerhetsbrytare kan öppna dörren för nya behandlingar som förhindrar att cancer etablerar sig på andra ställen i kroppen.
En tyst försvarare inne i cancercellerna
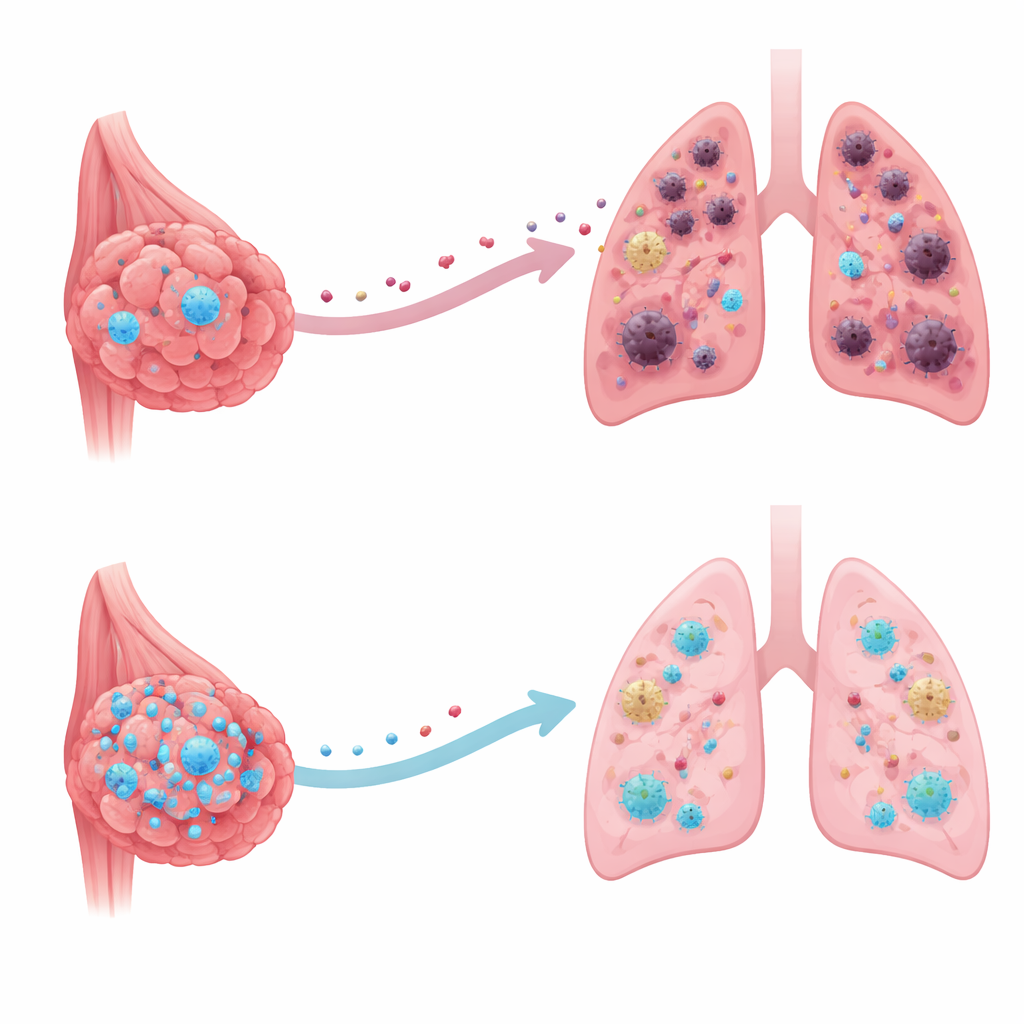
Forskarna fokuserade på ett protein kallat CRMP2, mest känt för att hjälpa nervceller att växa och bevara sitt interna skelett. När de undersökte stora offentliga cancerregister och patientprover fann de att CRMP2‑nivåerna var ovanligt låga i brösttumörer, särskilt i cancerformer som redan spridit sig. Patienter vars tumörer fortfarande hade högre mängder CRMP2 levde i genomsnitt längre och löpte mindre risk att utveckla avlägsna metastaser. Detta mönster antydde att CRMP2 beter sig mer som en broms än som en accelerator i bröstcancer — en intern försvarare snarare än en sjukdomsdrivare.
Hur lungorna förbereds för invasion
Cancerceller anländer sällan till ett avlägset organ som en överraskning. Långt innan de kommer dit frisätter den ursprungliga tumören molekyler som omformar det organet till vad forskare kallar en ”pre‑metastatisk nisch” — en mikromiljö som gynnar canceröverlevnad. Med en väletablerad musmodell som efterliknar mänsklig bröstcancer visade teamet att när brösttumörceller konstruerades för att producera extra CRMP2 växte primärtumörerna lika snabbt, men lungorna blev mycket mindre gästvänliga. Markörer för inflammation och vävnadsombyggnad i lungorna minskade, och färre av de immunceller som normalt dämpar anti‑tumörförsvar rekryterades. Som en följd bildades betydligt färre metastatiska knutor i lungorna efter att primärtumören avlägsnats.
En signalskedja som ställer till problem
För att förstå vilka tumörsekreterade signaler som låg bakom prepareringen av lungorna fokuserade forskarna på CXCL10, ett litet budbärarprotein (kemokin) känt för att locka vissa immunceller och förmå att väcka vilande cancerceller. I både odlade mänskliga och musbröstceller minskade en ökning av CRMP2 kraftigt mängden CXCL10 som producerades och frisattes. I möss visade lungor som exponerats för tumörmaterial rikt på CRMP2 mycket lägre CXCL10‑nivåer och färre inkommande immunceller som normalt dämpar skyddande T‑cellsaktivitet. När forskarna blockerade CXCL10 med en antikropp minskade kolonisationen av lungorna av cancerceller; när de tillsatte extra CXCL10 återställdes CRMP2:s skyddande effekt. Det placerade CXCL10 tydligt nedströms om CRMP2 som en nyckelaktör i skapandet av en metastasvänlig nisch.
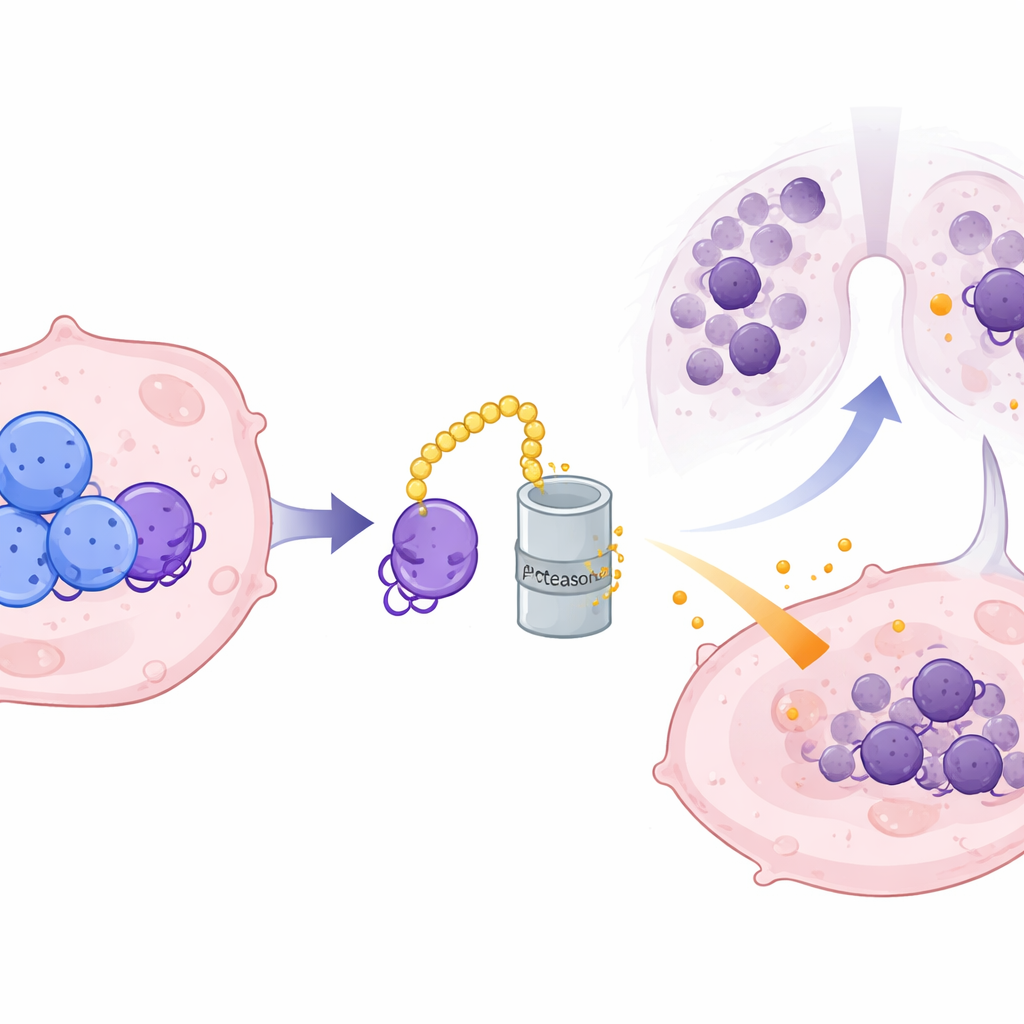
Den dolda mellanhanden som stabiliserar skadliga signaler
Eftersom CRMP2 finns inne i cellerna medan CXCL10 utsöndras misstänkte teamet en molekylär mellanhand. De identifierade ILF3, ett RNA‑bindande protein, som en direkt partner till CRMP2. ILF3 binder till RNA‑ritningen för CXCL10 och skyddar normalt detta från nedbrytning, vilket möjliggör produktion av mer CXCL10‑protein. CRMP2 binder ILF3 vid specifika kontaktpunkter och märker det för nedbrytning via cellens proteinåtervinningsmaskineri, vilket förkortar ILF3:s livslängd och bryter dess grepp om CXCL10‑RNA. När CRMP2‑nivåerna är höga degraderas ILF3 snabbare, CXCL10‑RNA blir instabilt och mindre av den inflammatoriska kemokinen utsöndras. När ILF3 konstgjort återställdes kunde det övervinna CRMP2:s hämning av CXCL10, vilket bekräftar dess roll som den avgörande länken i denna kedja.
Att förvandla en växtförening till en potentiell allierad
För att avgöra om denna väg kunde utnyttjas terapeutiskt screenade forskarna ett bibliotek av naturliga föreningar och fann att psoralen — en växt‑härledd molekyl som länge använts i hudbehandlingar — binder direkt till CRMP2 och gör det mer stabilt. I cellexperiment ökade psoralen CRMP2‑nivåerna, sänkte ILF3 och CXCL10 och minskade bröstcancercellers invasiva beteende utan att skada deras allmänna livsduglighet. I flera musmodeller krympte inte psoralen primärtumörerna, men det minskade kraftigt lungmetastaser och dämpade bildandet av den pre‑metastatiska nischen, återigen på ett sätt som var beroende av CRMP2. Även om psoralen i sig kan orsaka leverskada och behöver förfinas, visar resultaten att små molekyler kan förstärka CRMP2:s skyddande roll.
Vad detta betyder för patienter
Sammantaget visar detta arbete en skyddande axel inne i bröstcancerceller där CRMP2 destabiliserar ILF3, vilket i sin tur sänker CXCL10 och förhindrar att lungorna blir bördig mark för metastaser. Istället för att attackera cancerceller direkt syftar denna strategi till att avväpna de avlägsna nischer de är beroende av, och därmed gynna kroppens egna försvar. Mycket återstår innan en sådan metod når kliniken, men att rikta in sig på CRMP2–ILF3–CXCL10‑vägen — möjligen med säkrare psoralen‑lika läkemedel — erbjuder en lovande ny vinkel för att förhindra spridning av bröstcancer.
Citering: Lin, B., Luo, M., Zhou, Y. et al. CRMP2 inhibits metastasis formation by impairing ILF3-dependent stabilization of CXCL10 mRNA in breast cancer. Cell Death Dis 17, 255 (2026). https://doi.org/10.1038/s41419-026-08515-5
Nyckelord: metastaser vid bröstcancer, pre‑metastatisk nisch, kemokin‑signalering, RNA‑bindande proteiner, naturproduktterapier