Clear Sky Science · sv
Ubenimex samverkar med PD-L1-hämning vid magsäckscancer genom att konkurrera om bindning av LAP3 med UBE3A
Varför denna forskning är viktig
För många med avanserad magsäckscancer har moderna immunterapier som ”släpper på bromsarna” i immunsystemet gett nytt hopp — men de hjälper fortfarande bara en minoritet av patienterna. Denna studie ställer en praktisk fråga med verklig betydelse: kan ett äldre immunstimulerande läkemedel, Ubenimex, återanvändas för att öka effekten av dessa läkemedel, och varför skulle det fungera? Forskarna avslöjar ett dolt molekylärt knep som tumörer använder för att undkomma immunangrepp och visar hur Ubenimex kan åtgärda det, vilket öppnar för mer effektiva kombinationsbehandlingar.
En ny partner för cancerimmunterapi
Arbetet fokuserar på magsäckscancer, en sjukdom som fortfarande är vanlig och dödlig, särskilt i Kina. Läkemedel som blockerar PD-1 eller PD-L1 — proteiner som dämpar immunsvar — är nu en behandlingsgrundpelare. Ändå svarar de flesta patienter inte alls eller får så småningom återfall. Författarna vände sig till Ubenimex, ett långtidsgodkänt läkemedel som används som tillägg till cytostatika och strålbehandling och som är känt för att stimulera immunceller. De undersökte om en kombination av Ubenimex och PD-L1-blockerande antikroppar kunde göra tumörer mer sårbara för angrepp av CD8 T-celler, de immunceller som direkt förstör cancerceller.
Sätta läkemedelskombinationen på prov
Med en musmodell för magsäckscancer där tumörerna var konstruerade för att överproducera ett protein kallat LAP3 behandlade teamet djuren med Ubenimex, anti–PD-L1, båda eller inget av dem. Varje behandling ensam krympte tumörer, men kombinationen stack ut: tumörerna drog sig helt tillbaka hos alla behandlade möss och överlevnaden förbättrades mer än med enbart PD-L1-hämning. Immunanalyser visade att kombinationen kraftigt ökade antalet och aktiviteten hos CD8 ”mördande” T-celler, som släppte ut fler toxiska molekyler och inflammatoriska budbärare. Viktigt är att behandlingen inte orsakade tydliga leverskador eller viktnedgång, vilket tyder på att metoden kan vara kraftfull utan att vara alltför hård.
En dold switch som skyddar tumörer
För att förstå varför Ubenimex hjälpte fokuserade forskarna på LAP3, ett enzym det hämmar. De fann att LAP3-nivåerna var högre i mänskliga magsstumörer än i normalt magslemhinnvävnad och att patienter med mer LAP3 tenderade att få sämre överlevnad. I både patientprover och musstumörer gick hög LAP3-nivå hand i hand med färre CD8 T-celler inne i cancern, även om andra immuncellstyper var oförändrade. När LAP3 experimentellt minskades i tumörceller växte tumörerna långsammare, drog till sig fler CD8 T-celler och blev lättare för dessa celler att döda i laboratorietester. Sammantaget tyder data på att LAP3 inte bara är en åskådare utan en aktiv främjare av immunflykt.
Hur tumörer använder LAP3 för att hålla bromsarna i
När de grävde djupare avslöjade teamet hur LAP3 skyddar tumörceller från immunangrepp. De upptäckte att LAP3 hjälper till att stabilisera PD-L1, det centrala ”broms”-proteinet på cancerceller som släcker ner T-celler. Normalt kan PD-L1 märkas med små proteintaggar som skickar det till cellens nedbrytningsmaskineri. Ett enzym kallat UBE3A fäster dessa taggar, vilket leder till PD-L1-nedbrytning. LAP3 binder fysiskt till UBE3A och hindrar därigenom UBE3A från att märka PD-L1. Som ett resultat ansamlas PD-L1 på tumörytan och bildar en skyddande sköld mot CD8 T-celler. När LAP3-nivåerna sänks, eller när dess funktion blockeras, märks PD-L1 mer omfattande, bryts ner snabbare och dess ytuttryck minskar — vilket tillåter T-celler att närma sig och anfalla.
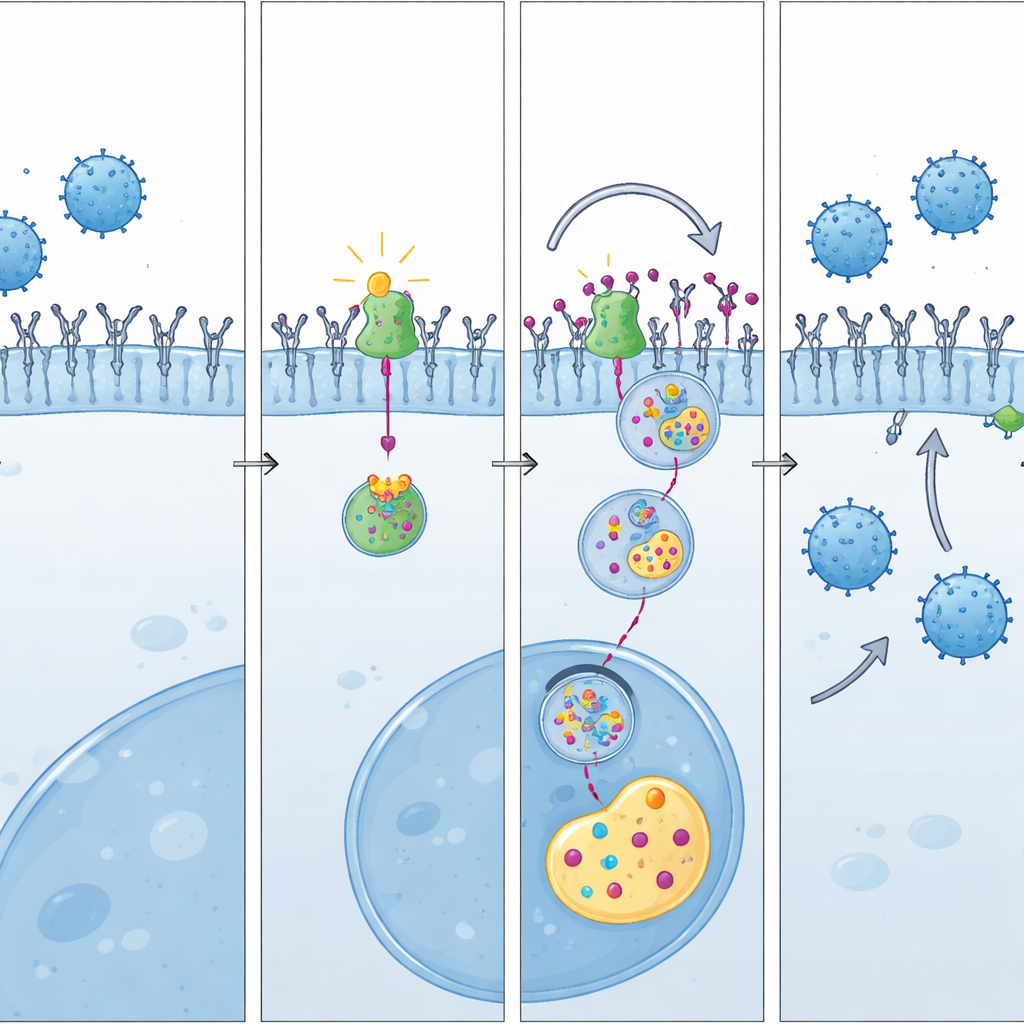
Hur Ubenimex tippar vågskålen
Studien visar sedan att Ubenimex verkar genom att störa LAP3–UBE3A-partnerskapet. Datormodellering och biokemiska experiment indikerar att Ubenimex tar plats i LAP3 vid samma region där LAP3 normalt interagerar med UBE3A. Denna konkurrerande bindning sliter UBE3A bort från LAP3, vilket frigör det att märka PD-L1 för nedbrytning. I cellexperiment minskade Ubenimex PD-L1 på tumörytan, ökade märkningen av PD-L1 för nedbrytning och vände de PD-L1-ökande effekterna av överskott av LAP3. I levande möss översattes detta molekylära skifte till fler aktiva CD8 T-celler och en påtaglig tumörkontroll när Ubenimex kombinerades med PD-L1-hämning.
Vad detta betyder för patienter
Sammantaget målar studien upp en tydlig bild: många magsäckstumörer överproducerar LAP3, vilket hjälper dem att upprätthålla höga nivåer av PD-L1 och därigenom gömma sig från immunsystemet. Ubenimex bryter detta skydd genom att blockera LAP3:s grepp om UBE3A, vilket gör att PD-L1 kan rensas bort. Med färre bromsar på cancercellernas yta kan PD-L1-blockerande läkemedel och mördande T-celler samverka mycket effektivare. Eftersom Ubenimex redan används kliniskt och LAP3 kan mätas i tumörprover ger denna forskning en konkret, prövbar strategi för att förbättra immunterapi vid magsäckscancer och potentiellt andra cancerformer med förhöjt LAP3.
Citering: Zhao, C., Li, J., Zheng, J. et al. Ubenimex synergizes with the PD-L1 blockade in gastric cancer by competitively binding LAP3 with UBE3A. Cell Death Dis 17, 241 (2026). https://doi.org/10.1038/s41419-026-08509-3
Nyckelord: magsäckscancer, immunterapi, PD-L1, Ubenimex, LAP3