Clear Sky Science · sv
Fibroblaster kopplade till cancer främjar osimertinib‑resistens i icke‑småcellig lungsjukdom via METTL1‑medierad NET1 m7G‑modifiering
Varför vissa lungcancerformer slutar svara på ett “smart” läkemedel
Målinriktade läkemedel som osimertinib har förändrat behandlingen för många med en vanlig form av lungcancer och ger längre överlevnad med färre biverkningar än traditionell cytostatika. För de flesta patienter är dock dessa fördelar tillfälliga: tumörer hittar så småningom sätt att kringgå läkemedlet. Denna studie ställer en bedrägligt enkel fråga med stora konsekvenser: är tumörens stödjande vävnad — specifikt celler som kallas cancerassocierade fibroblaster — tyst med och hjälper cancerceller att undkomma osimertinibs effekter?
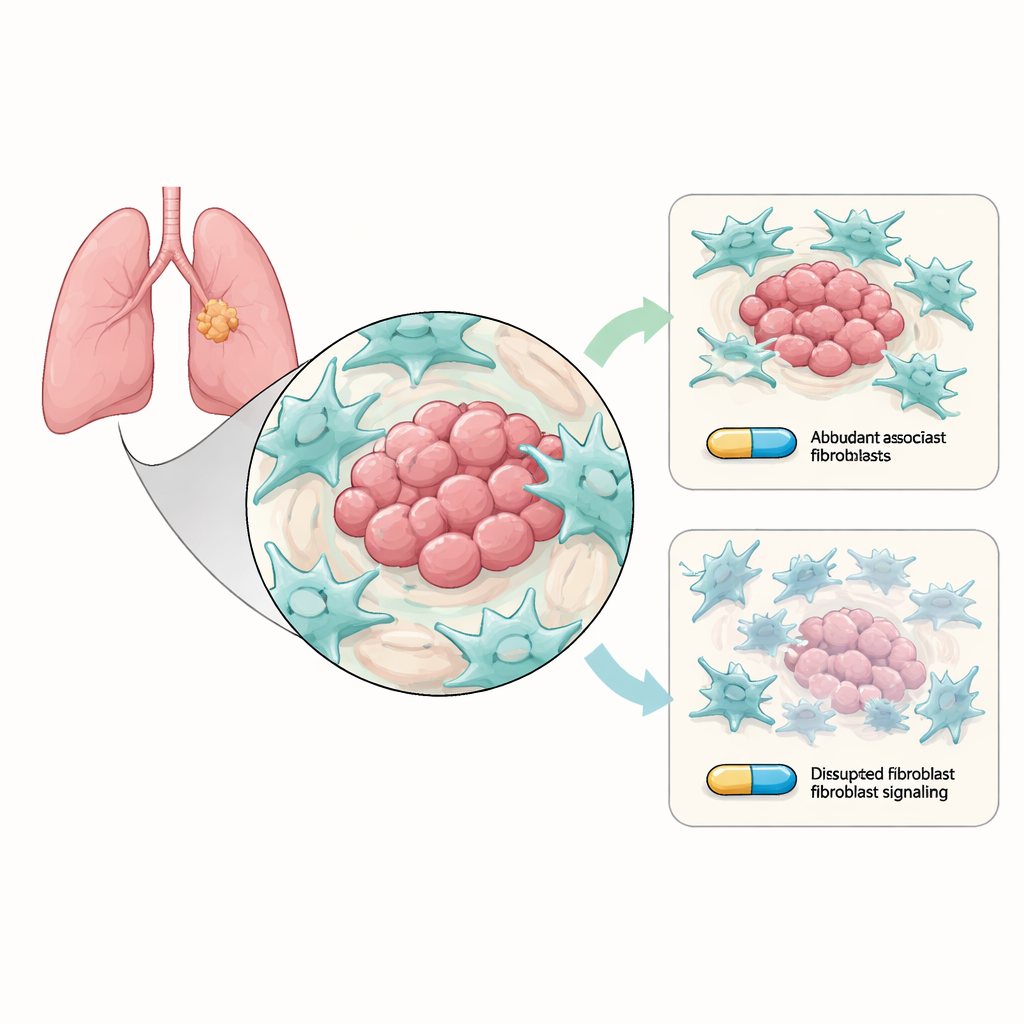
Hjälparceller som i smyg skyddar tumören
Icke‑småcellig lungcancer växer inom ett livligt kvarter av icke‑cancerceller som kallas tumörmikromiljön. Bland de mest talrika invånarna finns cancerassocierade fibroblaster (CAF), bindvävsceller som omformar området runt tumören. Forskarna odlade lungcancerceller med de vanliga osimertinib‑känsliga EGFR‑mutationerna tillsammans med CAFs i laboratoriet. De fann att när CAFs fanns närvarande var cancercellerna svårare att döda med osimertinib: de bildade fler kolonier, genomgick mindre apoptos och uppvisade starkare ”stamliknande” egenskaper kopplade till långsiktig överlevnad och återfall. Med andra ord, även om läkemedlet fortfarande riktade sig mot cancercellerna, hjälpte de omgivande fibroblasterna tyst dem att uthärda.
En kemisk märkning på RNA som ändrar spelreglerna
Teamet tittade sedan bortom generna själva till de kemiska märkningar som dekorerar RNA — de fungerande kopiorna av genetisk information i cellerna. En sådan märkning, kallad m7G, kan påverka hur stabilt ett RNA är och hur effektivt det översätts till protein. Genom biokemiska tester och genomsökningskartläggning visade forskarna att CAFs ökar den totala m7G‑märkningen på RNA i lungcancerceller. Denna ökning drevs främst av ett metylerande enzym kallat METTL1, som sätter m7G‑märken på messenger‑RNA. METTL1‑nivåerna var högre i lungtumörer än i omkringliggande normal vävnad och kopplades till mer avancerad sjukdom och sämre patientöverlevnad, vilket antyder att detta enzym gör mer än att bara finjustera rutinmässiga cellfunktioner.
En utsöndrad signal och en sårbar molekylär kedja
Hur får CAFs METTL1 att öka i cancerceller? Studien pekar på ett protein kallat HMGB1 som CAFs släpper ut i sin omgivning. Jämfört med cancerceller utsöndrade CAFs mycket större mängder HMGB1. När forskarna tillsatte HMGB1 till lungcancerceller steg METTL1‑nivåerna och m7G‑märkena; när de blockerade HMGB1 i CAF‑konditionerat medium avtog denna effekt. Vidare identifierade de ett nyckel‑RNA‑mål för METTL1: NET1, en gen som bidrar till celltillväxt och rörelse. CAFs ökade både m7G‑märkning och mängd NET1‑RNA och protein, och METTL1 bundet fysiskt till NET1‑RNA för att stabilisera det. Mindre METTL1 gav mindre modifierat NET1, svagare överlevnadssignaler i cancercellerna och större känslighet för osimertinib.
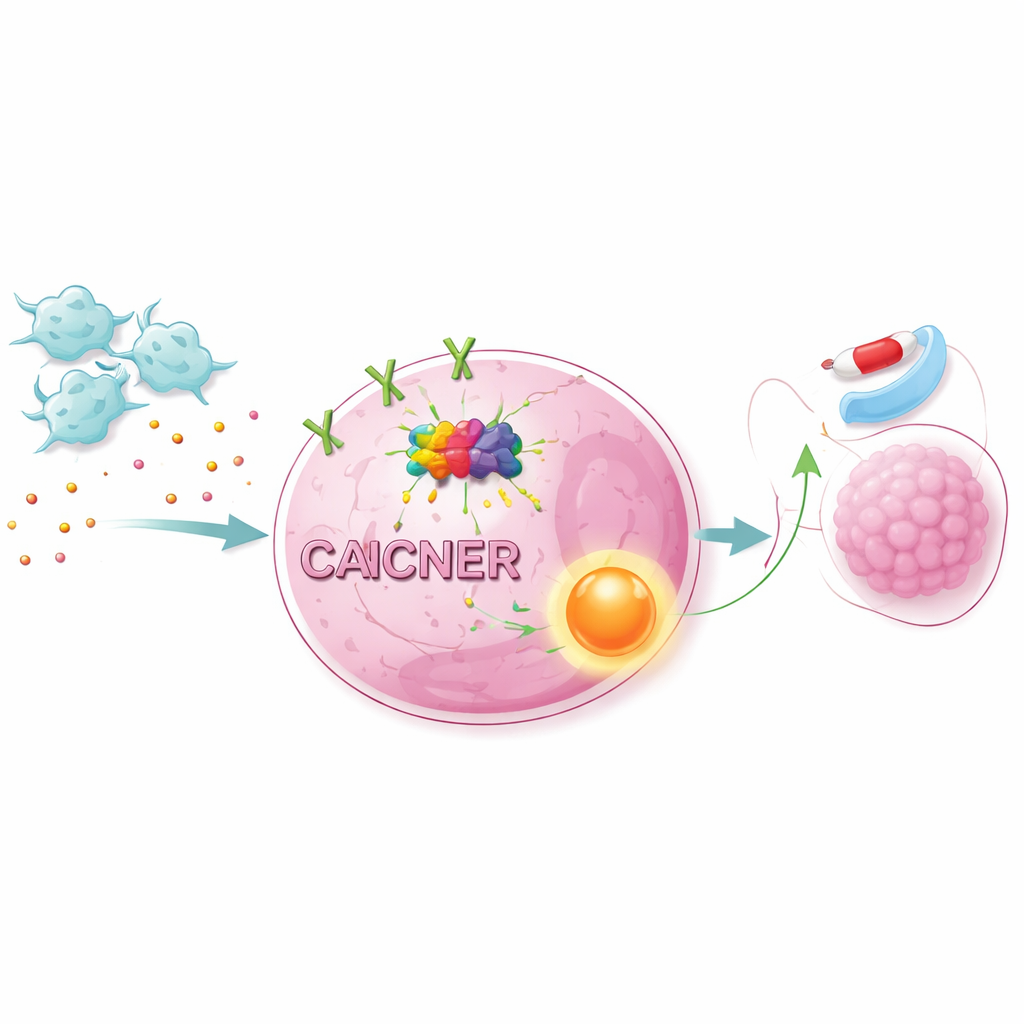
Att slå på överlevnadsvägar inuti cancerceller
Det försvagade NET1‑signalen agerade inte ensam. Genom att kombinera storskaliga RNA‑data med väg‑analys visade forskarna att CAFs aktiverar en huvudväg för tillväxt och överlevnad i cellerna känd som AKT/NF‑κB‑vägen. Blockering av AKT eller NF‑κB med specifika hämmare gjorde lungcancerceller mer sårbara för osimertinib, även i närvaro av CAFs. Att ändra NET1‑nivåer gav liknande effekter: minskning av NET1 försvagade CAF‑skyddet, medan ökning av NET1 stärkte resistensen. I möss inplanterade med humana lungcancerceller gjorde tillägg av CAFs att tumörer växte snabbare och blev mindre känsliga för osimertinib. Nedreglering av METTL1 i cancercellerna minskade m7G‑märken, sänkte NET1‑nivåer och väg‑aktivering, och reducerade kraftigt CAF‑driven tumörtillväxt.
Vad detta innebär för framtida behandling av lungcancer
För personer med EGFR‑muterad lungcancer erbjuder detta arbete ett nytt sätt att förstå varför kraftfulla läkemedel som osimertinib så småningom misslyckas. Istället för att enbart skylla på nya mutationer i cancerceller lyfter studien fram en molekylär kedja som börjar utanför tumörcellen — med CAFs som frigör HMGB1 — och går via METTL1, m7G‑märken på NET1 och aktivering av överlevnadsvägar som försvagar läkemedlets effekt. Att avbryta denna kedja i något led skulle i teorin kunna återställa eller förlänga känsligheten för behandlingen. Medan läkemedel som direkt riktar sig mot METTL1, HMGB1 eller specifika m7G‑markerade RNA fortfarande är i tidiga faser, tyder studien på att kombinationer av osimertinib med terapier riktade mot tumörens stödjeceller eller deras RNA‑modifierande signaler kan hjälpa till att hålla denna typ av lungcancer under kontroll längre.
Citering: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
Nyckelord: osimertinib‑resistens, icke‑småcellig lungcancer, cancerassocierade fibroblaster, RNA‑metylering, METTL1 NET1‑väg