Clear Sky Science · sv
miR-424(322)~503 hämmar koloncancerprogression driven av PTEN-brist
Varför denna studie är viktig för koloncancer
Koloncancer är fortfarande en av de vanligaste och mest dödliga cancerformerna globalt, och många patienter utvecklar avancerad sjukdom trots kirurgi, cytostatika och riktade läkemedel. Denna studie undersöker en liten uppsättning genetiska "dimmerbrytare" kallade microRNA som kan bromsa eller påskynda tumörtillväxt. Genom att klarlägga hur en specifik microRNA-kluster interagerar med den välkända tumörsuppressorgenen PTEN bidrar arbetet till att förklara varför vissa koloncancer blir mer aggressiva och pekar på nya sätt att förutsäga risk och utforma behandlingar.
Små RNA-brytare med stor effekt
MicroRNA är korta RNA-molekyler som inte kodar för proteiner men finjusterar hur hundratals gener används i en cell. miR-424(322)~503-klustret, som består av två besläktade microRNA, har förbryllat forskare eftersom det kan fungera både som broms och som gas i olika cancerformer. I koloncancer var dess roll oklar. Författarna fokuserade på cancer som drivs av förlust av PTEN, en gen som normalt håller tillväxtsignaler under kontroll och som ofta förändras i kolontumörer. De ställde en enkel men kraftfull fråga: vad händer med koloncancerutvecklingen när både PTEN och detta microRNA-kluster saknas?
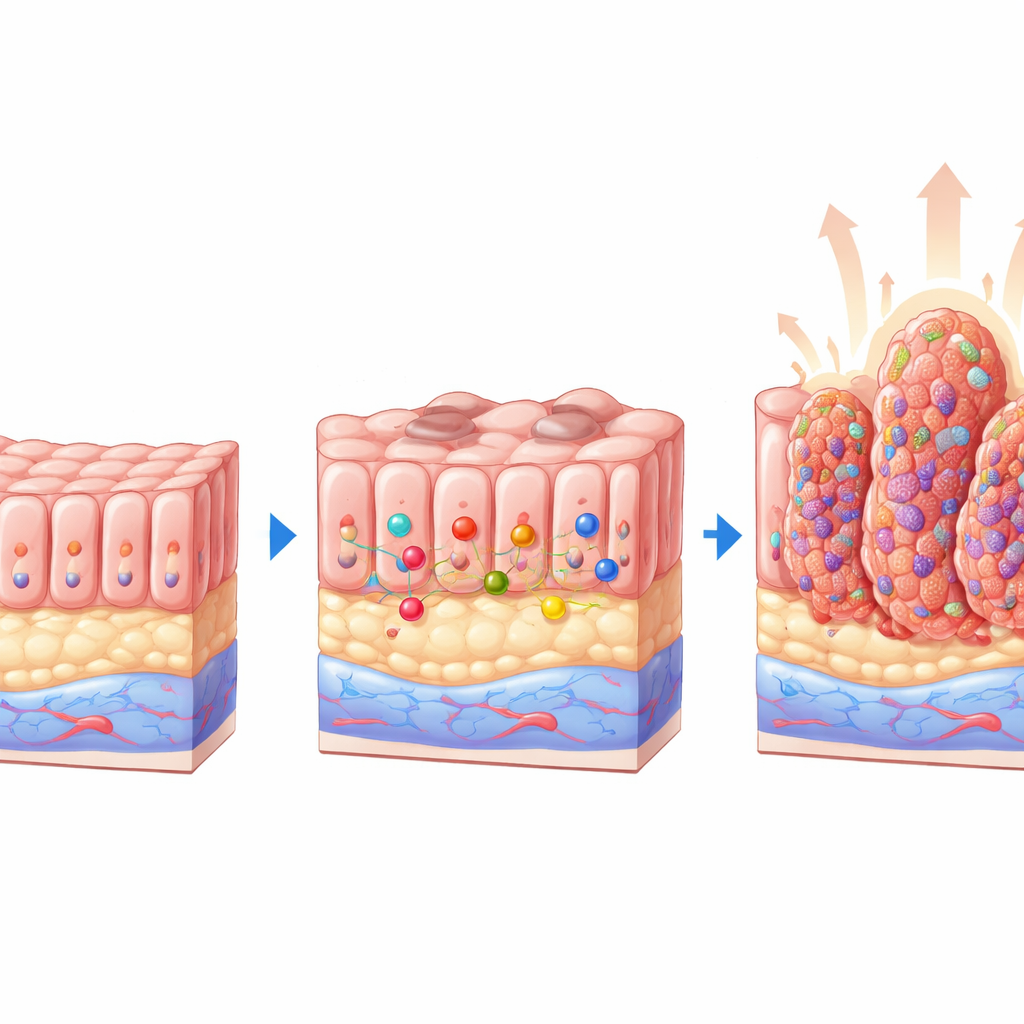
Musmodeller visar ett skyddande samband
För att besvara detta använde forskarlaget genetiskt modifierade möss där PTEN kan stängas av i tarmepitelet, och korsade dem med möss som saknar miR-424(322)~503-klustret. Det skapade fyra grupper: normala djur, möss som bara saknade microRNA, möss som bara saknade PTEN och dubbla utstötare som saknade båda. Efter att PTEN förlorats undersökte de noggrant kolon. Djur som bara saknade PTEN utvecklade flera små polyper, många med tidiga tecken på onormalt vävnad. I stark kontrast hade möss som saknade både PTEN och microRNA-klustret många fler lesioner, större polyper och en högre andel avancerade förändringar, inklusive höggradig dysplasi och tydlig adenokarcinom. MicroRNA-klustret i sig orsakade alltså inte sjukdom, vilket visar att dess förlust är särskilt skadlig när PTEN redan saknas.
Oförändrad klassisk väg, skift mot nya syndare
Koloncancer drivs ofta av överaktivering av Wnt/β-catenin-vägen, en central bana som kontrollerar stamceller i tarmen. Eftersom detta microRNA-kluster kan påverka den vägen i bröstvävnad testade författarna om samma gällde här. Överraskande nog förändrades varken nivåer eller lokalisation av β-catenin och dess koreceptor LRP6 i kolon när microRNA-klustret togs bort, inte ens i de dubbla knockout-djuren. Istället pekade storskalig genuttrycksprofilering åt annat håll: tumörer som saknade både PTEN och microRNA visade starka signaturer av vävnadsombyggnad, sårläkningsrespons och epitel-till-mesenkym-övergång, ett program kopplat till invasion och metastas. Signalvägar drivna av MAP-kinaser (ERK1/2 och p38) och av tillväxtfaktorn TGFβ var särskilt förhöjda.
Hur tillväxtsignalerna spårar ur
Genom att gå djupare undersökte forskarna proteiner i kolonvävnaden. De fann att medan förlust av PTEN ensam ökade PI3K/AKT-vägen, gav den ytterligare förlusten av microRNA-klustret en fortsatt topp i MAPK-aktivitet: mer aktiverat JNK, p38, MKK4 och särskilt ERK1/2. Dessa starkt aktiva signaler sammanföll med högre nivåer av cyklin D1, en nyckelregulator av celldelning. Samtidigt steg komponenter i TGFβ-vägen som främjar dess aktivitet (SMAD3 och SMAD4), medan en intern broms (SMAD7) föll, och cancerceller visade starkare nukleär SMAD2/3-färgning, vilket är förenligt med vägens aktivering. Genom att jämföra mössens tumörgener med förutsagda microRNA-mål identifierade teamet IGF1, en potent tillväxtfaktor som matar in i MAPK-kaskader, som ett direkt mål för miR-424(322)~503-klustret. När microRNA saknades undgick IGF1 repression och drev MAPK-signaleringen ännu högre. Analys av mänskliga koloncancer-dataset speglade dessa fynd: IGF1 var högre i tumörer med låga nivåer av miR-424 eller miR-503, och det långa icke-kodande RNA som är värd för dessa microRNA, MIR503HG, liksom microRNAen själva, var samordnat förändrade i patienttumörer.
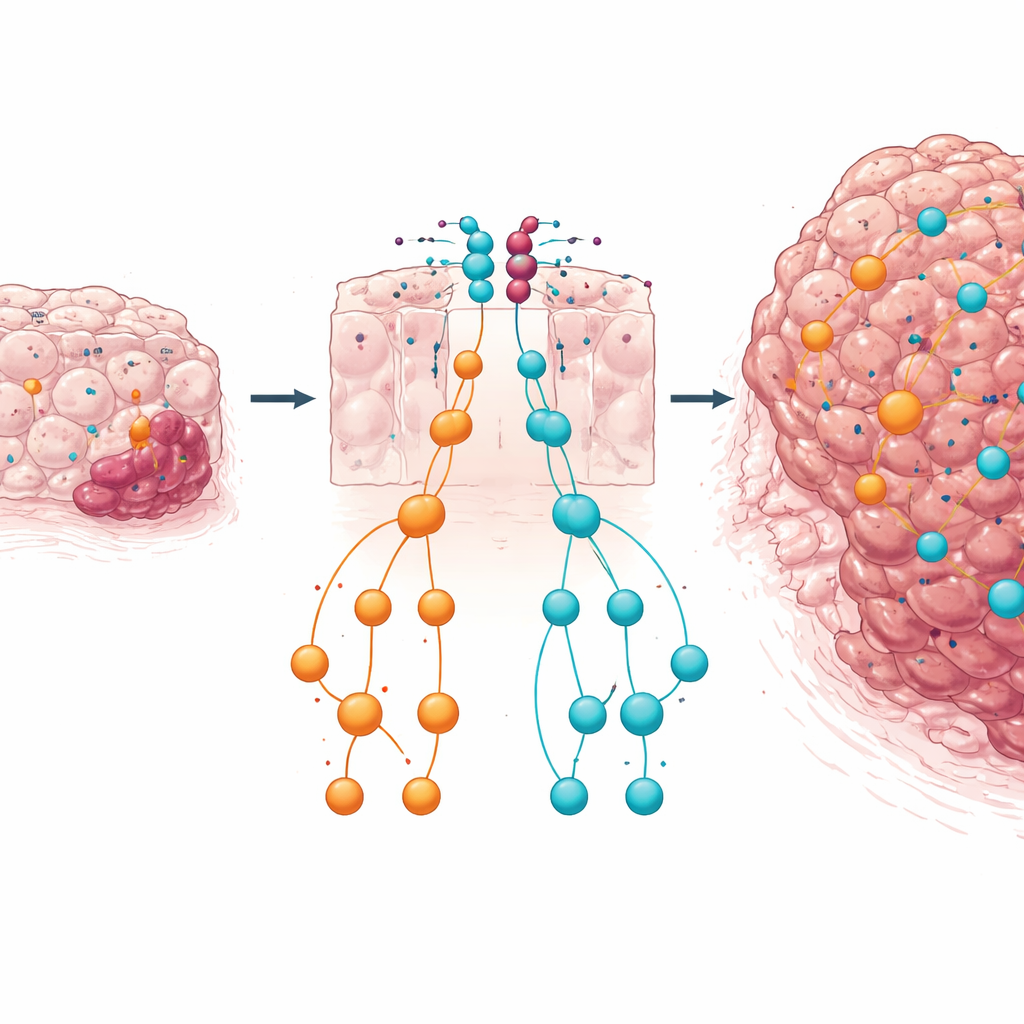
Ett dubbelt säkerhetsnät och vad det betyder för patienter
Sammantaget tyder resultaten på att i PTEN-bristfällig kolonvävnad fungerar miR-424(322)~503-klustret som ett andra säkerhetsnät. När PTEN förloras ökas dessa microRNA delvis genom signaler som TGFβ och arbetar för att dämpa kraftfulla tillväxtvägar som IGF1–MAPK och TGFβ–SMAD. Om denna microRNA-broms tas bort får tillväxt- och ombyggnadssignaler fritt spelrum, vilket påskyndar övergången från godartade polyper till invasiv cancer. För en lekmannaläsare är huvudbudskapet att inte alla genetiska förändringar i en tumör drar åt samma håll: vissa är inbyggda försvar. Att förstå hur PTEN och detta microRNA-kluster samverkar för att hålla celltillväxt i balans kan hjälpa till att identifiera högriskpatienter och inspirera till kombinationsbehandlingar som riktar både PI3K/AKT- och MAPK/TGFβ-axlarna vid kolorektal cancer.
Citering: Vidal-Sabanés, M., Bonifaci, N., Navaridas, R. et al. miR-424(322)~503 impairs colon cancer progression driven by PTEN deficiency. Cell Death Dis 17, 254 (2026). https://doi.org/10.1038/s41419-026-08504-8
Nyckelord: kolorektal cancer, PTEN, microRNA, MAPK-signalering, TGF-beta