Clear Sky Science · sv
mTOR-drivet hämmande av autophagi definierar metabolisk sårbarhet i CDK4/6-hämmarresistent HR+/HER2− bröstcancer
Varför detta är viktigt för bröstcancerpatienter
Många kvinnor med avancerad bröstcancer lever numera längre tack vare läkemedel som kallas CDK4/6-hämmare, vilka saktar ner hur snabbt tumörceller delar sig. Tyvärr lär sig de flesta tumörer så småningom att undkomma dessa mediciner. Denna studie ställer en hoppfull fråga: när bröstcancer blir resistent mot CDK4/6-läkemedel, får den då en ny svaghet som läkare skulle kunna utnyttja med befintliga, relativt enkla metaboliska läkemedel såsom metformin eller dikloroättiksyra (DCA)?
När cellcykelhämmare slutar fungera
Läkare behandlar ofta den vanligaste typen av bröstcancer — hormonreceptorpositiv, HER2-negativ sjukdom — med hormonterapi tillsammans med CDK4/6-hämmare som palbociklib eller ribociklib. Dessa läkemedel riktar in sig på proteiner som driver cellerna genom delningscykeln. Med tiden anpassar sig dock vissa cancerceller och blir starkt resistenta, fortsätter att växa även i närvaro av höga doser läkemedel. Forskarna återskapade detta problem i laboratoriet genom att utsätta bröstcancercellinjer (T47D och MCF7) för gradvis ökande mängder CDK4/6-hämmare. De fick fram två typer av överlevare: delvis resistenta celler och en mindre grupp av starkt resistenta kloner som inte längre svarade väl på behandlingen.
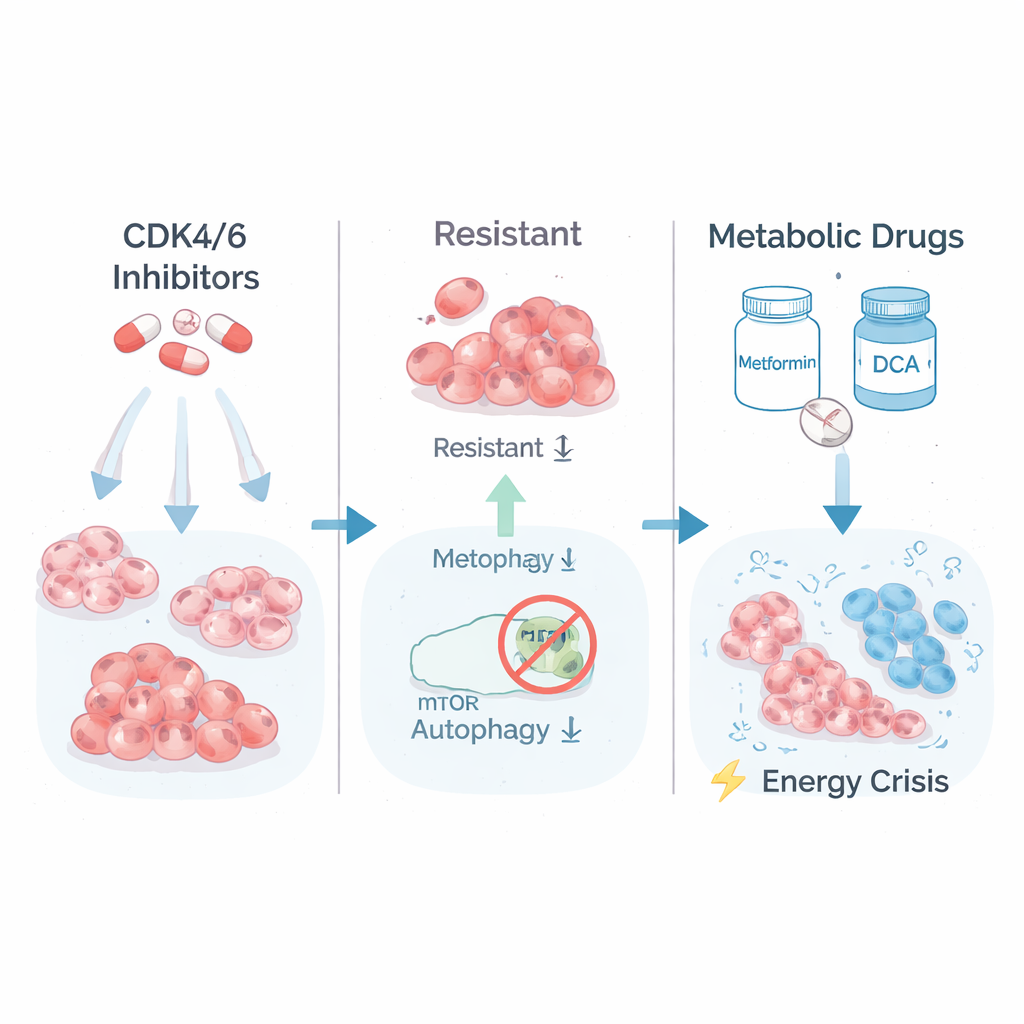
En dold svaghet i tumörens energianvändning
För att förstå vad som gjorde de starkt resistenta cellerna annorlunda undersökte teamet vilka gener som var på- eller avskrivna. De fann att de mest resistenta cellerna hade skruvat upp vägar involverade i sockernedbrytning (glykolys) och i tillväxtsignalering som styrs av ett proteinkomplex kallat mTORC1. Med andra ord levde dessa celler i hög växel och förbrukade bränsle i hög takt för att fortsätta växa. Forskarna testade sedan om denna ”högväxlande” metabolism kunde vändas mot cellerna. De behandlade de resistenta och föräldra‑cellerna med metformin, ett vanligt diabetesläkemedel som stressar cellens energifabriker, och DCA, som tvingar celler att bearbeta bränsle mer effektivt. Slående nog var de mest läkemedelsresistenta klonerna nu de mest sårbara: deras långsiktiga tillväxt i odlingsskålar kollapsade under metabolisk behandling, medan föräldra‑ och endast delvis resistenta celler påverkades mycket mindre.
Blockerad självstädning och en energikrasch
Varför skulle dessa flyktade cancerceller vara så känsliga för energistress? Svaret låg i en annan grundläggande överlevnadsprocess: autophagi, cellens inbyggda ”återvinnings- och rengörings”system. Normalt, när energi blir knapp, bryter celler ner och återanvänder sina egna komponenter för att hålla sig vid liv. Forskarna visade att i de starkt resistenta klonerna var mTORC1 överaktivt och satte en kemisk broms på ULK1, en nyckelaktiverare av autophagi. Med en känslig reporter‑analys demonstrerade de att dessa celler inte längre kunde korrekt slå på eller uppreglera autophagi, även när de pressades med metabola läkemedel. Som en följd skapade metformin och DCA en svår energikris: sensorer för låg energi aktiverades, fettproduktion stängdes av och markörer för irreversibel celldöd uppträdde, specifikt i de starkt resistenta cellerna.
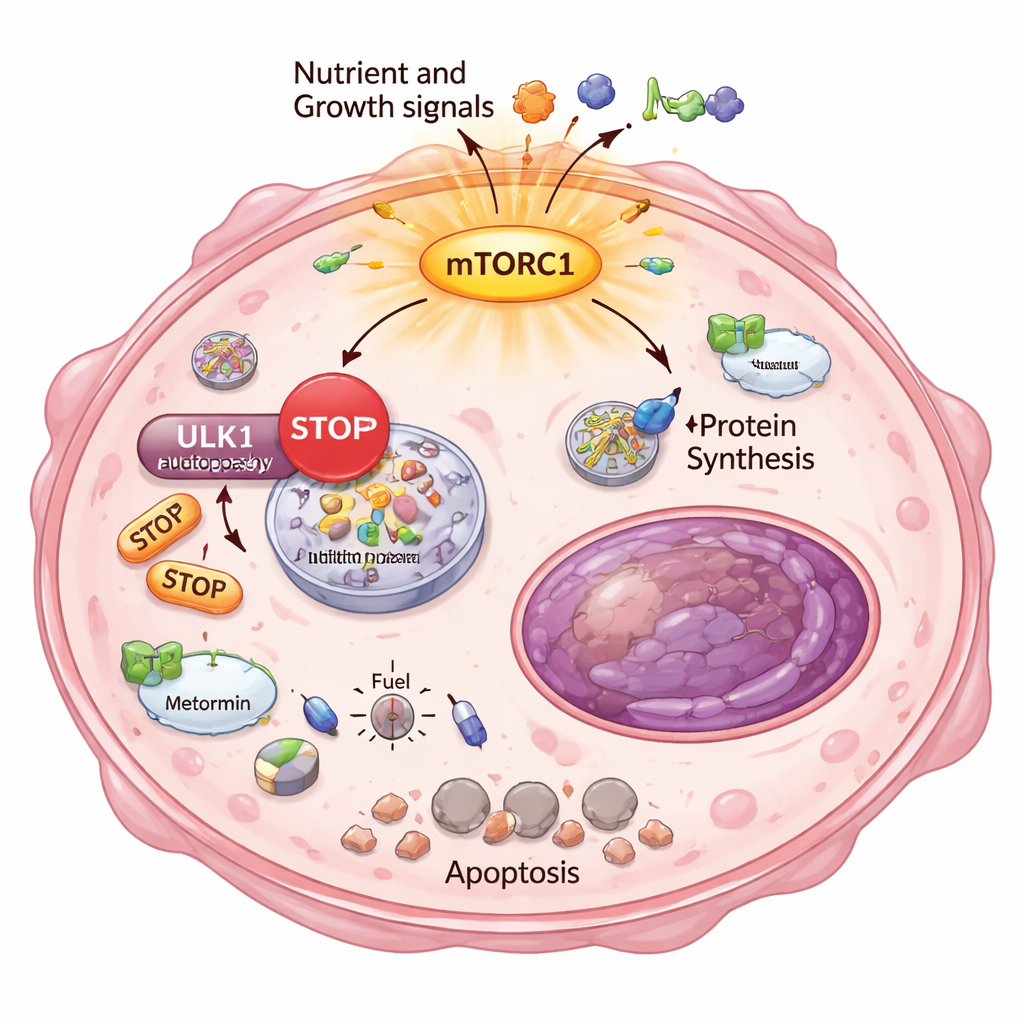
Bevis från verkliga patienttumörer
Laboratoriemodeller speglar inte alltid vad som händer hos patienter, så teamet vände sig till mänskliga brösttumörprover. De färgade in över hundra cancer för en markör för mTORC1‑aktivitet (fosforylerad 4E‑BP1) och för p62, ett protein som ansamlas när autophagi blockeras. Tumörer med hög mTORC1‑aktivitet tenderade att ha mer p62, vilket stöder idén att ett mönster av ”överdriven tillväxtsignal plus dålig återvinning” finns i verkliga bröstcancerfall, inte bara i cellinjer. Detta tyder på att en undergrupp av patienter kan bära tumörer med samma metabola svaghet som sågs i labbet.
Vad detta kan innebära för framtida behandlingar
För en lekmannapublik är kärnbudskapet att när bröstcancer utvecklas för att undkomma kraftfulla CDK4/6‑läkemedel kan den samtidigt måla in sig i ett metaboliskt hörn. Genom att permanent slå på tillväxtsignaler och stänga av cellens återvinningssystem blir dessa tumörer starkt beroende av ett konstant energitillflöde. Studien visar att denna konfiguration kan utnyttjas med metabola läkemedel som metformin och DCA, vilka redan är välkända i andra sjukdomar. Viktigt är att författarna föreslår att enkla vävnadstester för mTORC1‑aktivitet och autophagimarkörer skulle kunna hjälpa till att identifiera patienter vars resistenta tumörer är förberedda för denna typ av metaboliskt angrepp, vilket öppnar dörren för mer personligt anpassade räddningsbehandlingar efter att CDK4/6‑hämmare misslyckats.
Citering: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
Nyckelord: bröstcancer, resistens mot CDK4/6-hämmare, mTOR, autophagi, metabolisk behandling