Clear Sky Science · sv
Splice-växling av den onkogena BCS1L-isoformen undertrycker äggstockscancerutveckling genom att störa mitokondriell funktion
Kraftverk inne i cancerceller
Varje cell i vår kropp är beroende av små kraftverk som kallas mitokondrier. Cancerceller, som växer och sprider sig snabbt, är särskilt energikrävande. Denna studie avslöjar hur äggstockscancer omprogrammerar en av sina centrala mitokondriella medhjälpare, och visar att man genom att varsamt slå om en molekylär ”strömbrytare” på denna medhjälpare kan svälta tumörer samtidigt som frisk vävnad i stort sett sparas.
Varför tumörer lutar sig mot sina motorer
Äggstocksceller, liksom många andra cancerformer, kan flexibelt utnyttja olika energikällor. Genom att gå igenom stora patientdatabaser och enstaka cellprofiler fann forskarna att många äggstockstumörer kör sina mitokondrier i ett högvarvsläge känt som oxidativ fosforylering, eller OXPHOS. Tumörer med denna upptrappade mitokondriella aktivitet var mer aggressiva och vanligare i avancerad sjukdom. Bland de många proteiner som bygger upp mitokondriens kraftmaskineri stack ett ut: BCS1L, en chaperon som hjälper till att montera Komplex III, en central nod i cellens energipipeline. Tumörer med hög OXPHOS och vissa tumörcellstyper visade särskilt stark BCS1L-aktivitet, vilket antyder att cancerceller i hög grad förlitar sig på denna medhjälpare för att hålla sina motorer igång.
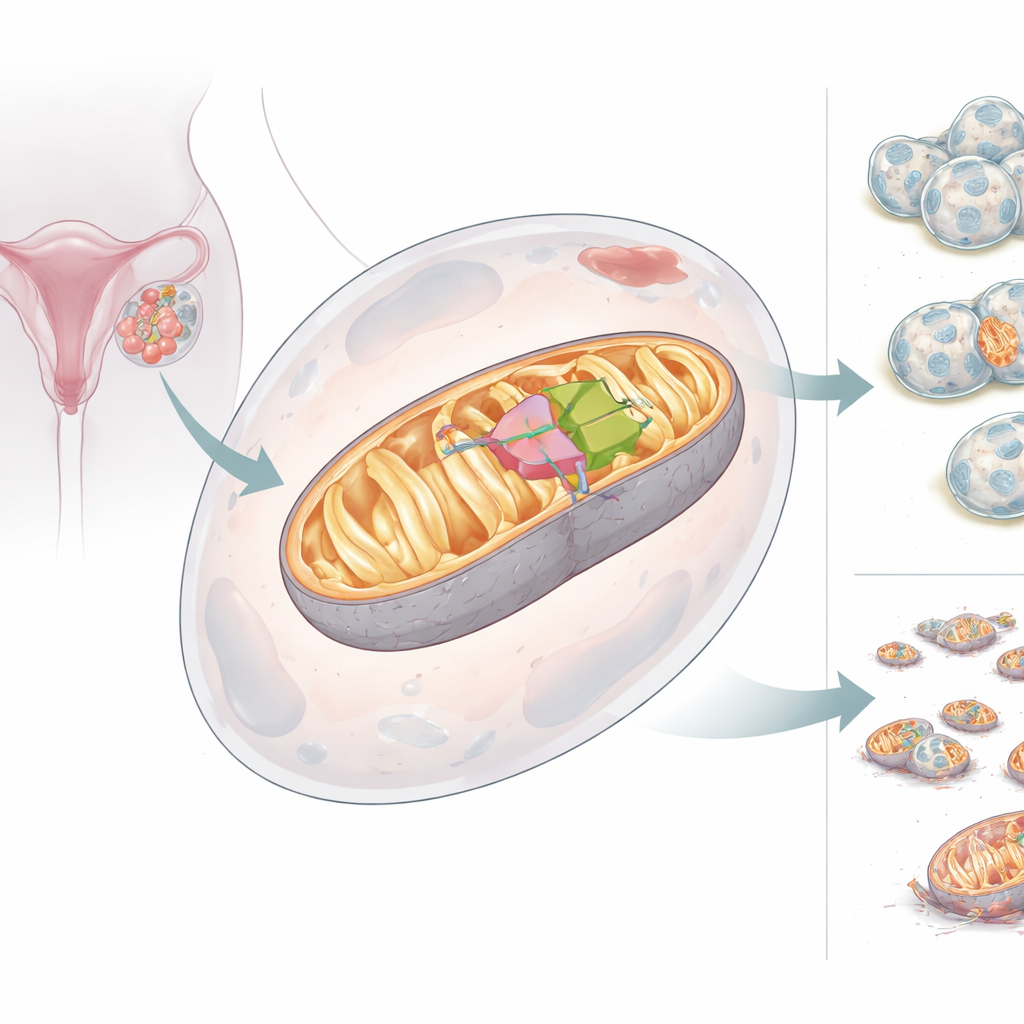
Två ansikten hos en mitokondriell medhjälpare
Teamet upptäckte att BCS1L-genen kan ge upphov till två versioner, eller isoformer, av sitt protein. Den fullängdsform, BCS1L-L, bär en inbyggd adresstag som skickar den in i mitokondrierna, där den stöder korrekt montering av Komplex III och hög energiproduktion. Den kortare formen, BCS1L-S, saknar ett avgörande segment och når inte mitokondrierna; istället sitter den i cellens vätska och kärna och stöder inte energiproduktion. I frisk vävnad är den korta versionen vanlig, men i äggstockscancer förändras balansen: den långa, mitokondriebundna formen dominerar. När celler tvingades producera mer BCS1L-L genererade deras mitokondrier mer energi, upprätthöll starkare membranpotential, producerade färre skadliga syreprodukter och motstod celldöd. När BCS1L minskades fragmenterades mitokondrierna, energiproduktionen föll, skadliga syremolekyler ökade och cancerceller var mer benägna att dö.
Hur cancern omkopplar budskapet
Att producera antingen den långa eller korta BCS1L-versionen beror på hur cellen redigerar sitt RNA-meddelande, en process som kallas splitsning. Forskarna sökte efter proteiner som binder BCS1L-RNA och påverkar detta val. De fokuserade på USP39, en splitsningsfaktor som redan kopplats till flera cancerformer. I äggstocksceller binder USP39 nära den RNA-sekvens som blir BCS1L:s exon 2 och uppmuntrar dess inkludering, vilket främjar den långa, mitokondrieinriktade formen. När USP39 tystades hoppade cellerna över detta segment oftare och skiftade mot den korta BCS1L-S-formen. Detta skifte försvagade Komplex III, minskade mitokondriell respiration och ATP-produktion, ökade oxidativ stress och utlöste cancercelldöd. Återställande av BCS1L-L i dessa celler räddade mycket av deras mitokondriella funktion och överlevnad, vilket visar att USP39 driver en kritisk mitokondriell strömbrytare till stor del genom BCS1L.
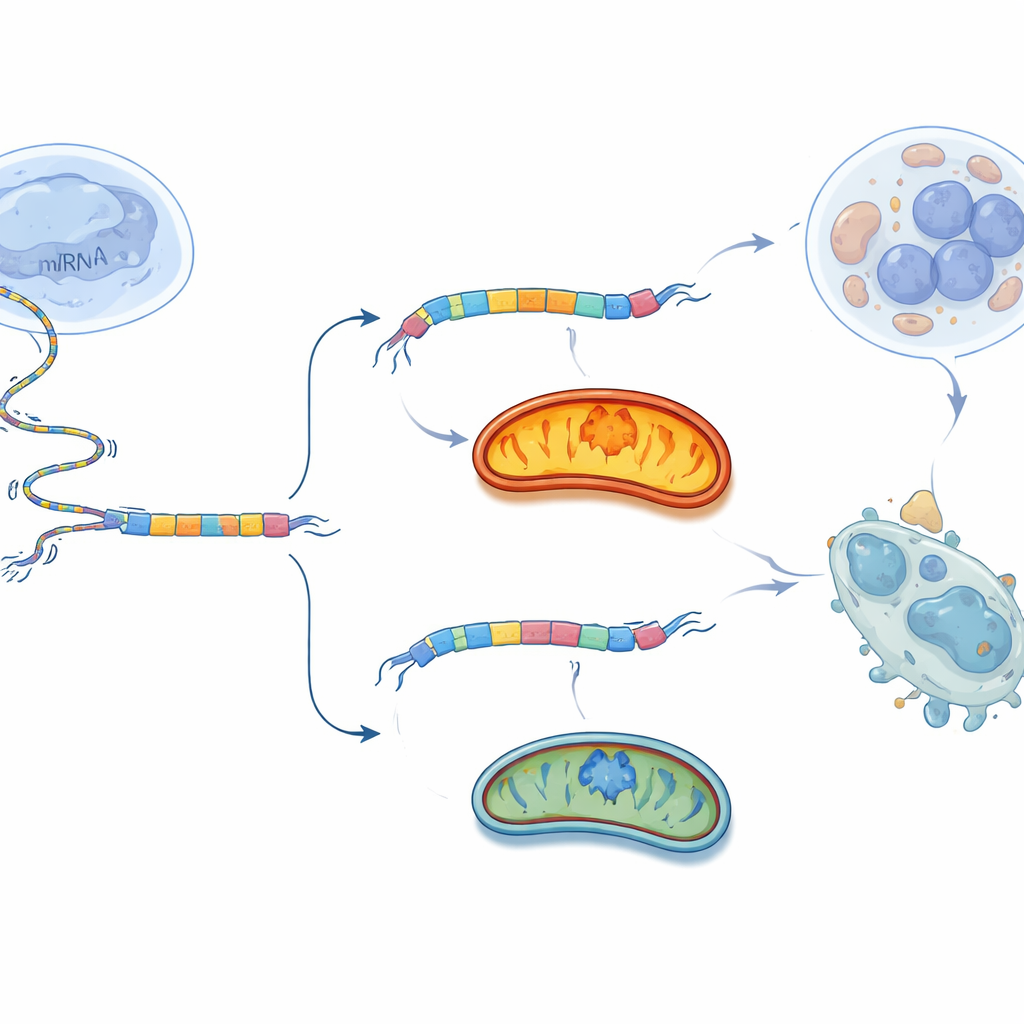
Vända strömbrytaren mot tumören
I stället för att blockera mitokondrier brett, vilket kan skada många vävnader, prövade teamet en mer kirurgisk taktik: att påverka själva splitsningsvalet av BCS1L. De designade korta stycken genetiskt material kallade antisense-oligonukleotider (ASO) som binder precis runt exon 2 i BCS1L-RNA:t. Dessa ASO fungerar som små klädnypor och förändrar hur splitsningsmaskineriet läser budskapet och uppmuntrar cellen att hoppa över exon 2. I äggstocksceller odlade i skålar minskade den bästa ASO kraftigt den långa BCS1L-L-formen och ökade den korta BCS1L-S-formen. Som ett resultat sjönk mitokondriell respiration och ATP-produktion, nivåerna av skadliga syreradikaler ökade och betydligt fler celler genomgick programmerad död. När samma ASO injicerades i äggstockstumörer hos möss bromsades tumörtillväxten och tumörerna vägde mindre, med en mycket starkare effekt på cancerceller än på normala fibroblaster.
Vad detta kan innebära för patienter
Enkelt uttryckt visar detta arbete att många äggstockstumörer förlitar sig på en ”turbo”-version av ett mitokondriellt hjälpprotein för att driva sin tillväxt. En splitsningsfaktor, USP39, tippar cellens RNA-redigeringsmaskineri så att mer av denna turboversion bildas och håller tumörens kraftverk i toppskick. Genom att använda noggrant designade ASO för att slå tillbaka splitsningsvalet mot den svagare versionen kan forskare selektivt försvaga cancercellernas mitokondrier, utlösa deras död samtidigt som de lämnar de flesta normala celler mindre påverkade. Även om leverans av sådana ASO-läkemedel till tumörer fortfarande är en stor utmaning, pekar denna studie på BCS1L:s splitsningsströmbrytare som ett lovande och mycket specifikt nytt angreppssätt för behandling av äggstockscancer.
Citering: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
Nyckelord: äggstockscancer, mitokondrier, RNA-splitsning, BCS1L, antisense-oligonukleotider