Clear Sky Science · sv
NSD2 hämmar uttrycket av PD-L1 via oxidativ fosforylering för att kontrollera immunövervakning vid hepatocellulärt karcinom
Varför denna levercancerberättelse är viktig
Hepatocellulärt karcinom, den vanligaste formen av levercancer, upptäcks ofta sent och är motståndskraftigt mot många behandlingar. Immunoterapier som blockerar PD-L1:s ”osynlighetsmantel” på tumörceller hjälper vissa patienter, men inte de flesta. Denna studie avslöjar en oväntad aktör, ett protein kallat NSD2, som kopplar samman hur levercancerceller producerar energi med hur synliga de är för immunsystemet. Att förstå denna koppling kan peka mot nya sätt att förstärka nuvarande terapier och identifiera vilka patienter som troligen har nytta av dem.
En överraskande roll för ett känt cancerprotein
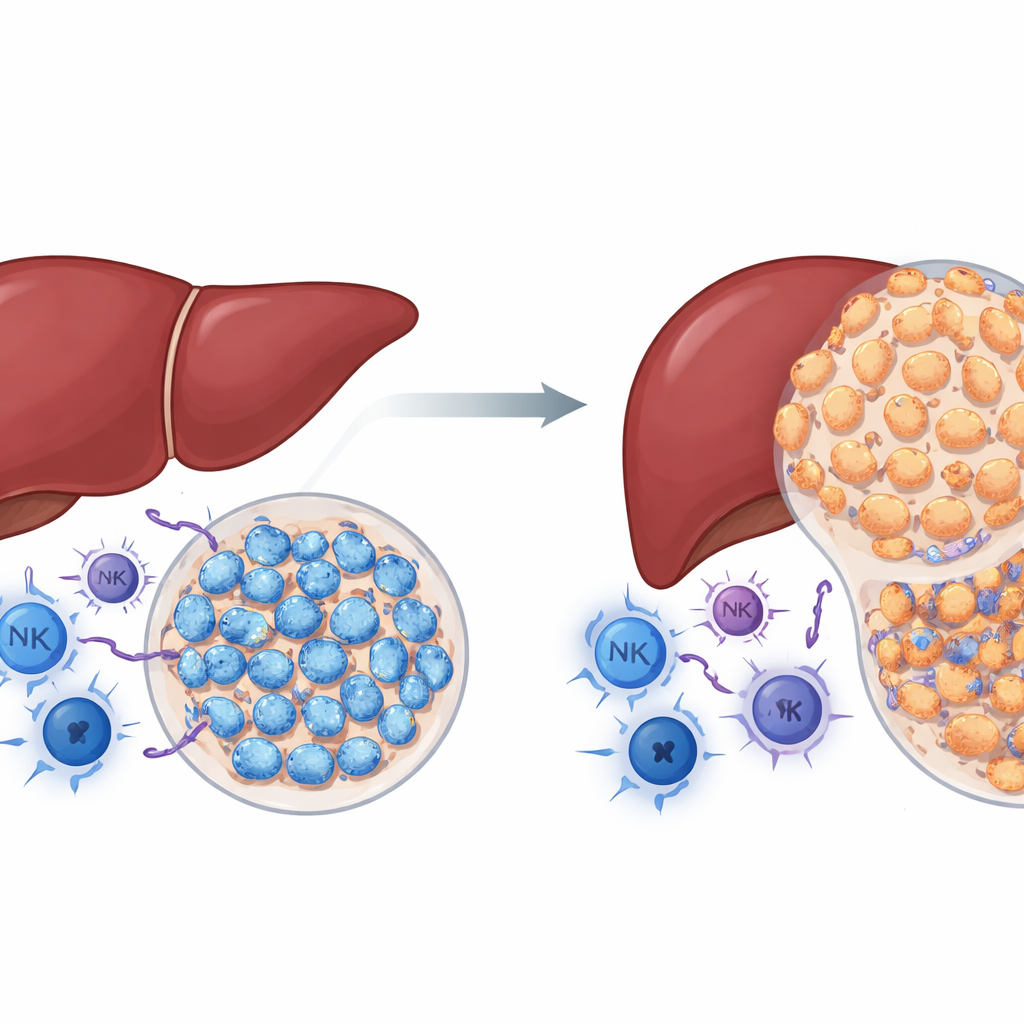
NSD2 är ett enzym som modifierar histoner, proteinerna runt vilka DNA är lindat. I många cancerformer har NSD2 betraktats som en drivkraft för tumörtillväxt. Författarna undrade om detsamma gäller i levercancer. Genom att använda genetiskt modifierade möss där NSD2 är aktiverat specifikt i leverceller behandlade de djuren med en kemikalie som på ett tillförlitligt sätt inducerar levertumörer. Motsatt förväntan utvecklade möss med extra NSD2 betydligt färre och mindre tumörer än normala möss, och deras lever visade mindre skada, ärrbildning och cellproliferation. Samtidigt innehöll tumörer från levervävnad som överuttryckte NSD2 fler cancerbekämpande immunceller, inklusive hjälpar- och mördande T‑celler samt naturliga mördarceller. Dessa fynd antyder att NSD2, i ett intakt immunsystem, beter sig mindre som en accelerator och mer som en broms för levercancer.
Energifabriker och bränsleanvändning i tumörceller
För att förstå hur NSD2 begränsar tumörer kartlade teamet genaktivitet i levervävnad. De fann att NSD2‑överuttryck kraftigt dämpade gener som är involverade i oxidativ fosforylering, processen där mitokondrier — cellens ”kraftverk” — genererar energi med hjälp av syre. Uppföljande experiment i mus- och humana levercancercellinjer visade att ökat NSD2 sänkte uttrycket av många gener för oxidativ fosforylering, minskade syreförbrukning och ATP‑produktion samt sänkte mitokondriemembranpotentialen, ett tecken på svagare mitokondrieaktivitet. Samtidigt konsumerade dessa celler mindre glukos men skiftade inte mot ökad glykolys, vilket indikerar en netto‑minskning i energiproduktion. Förlust av NSD2 gav motsatta effekter, med starkare mitokondriell kraft och bränsleanvändning.
Hur NSD2 omkopplar energi och immun‐synlighet
Genom att gå djupare kombinerade forskarna genomskädlig kromatinmappning med genuttrycksdata och identifierade en uppsättning gener som direkt aktiveras när NSD2 är närvarande. Två av dessa, Camk2d och Prkce, är kända för att dämpa mitokondrieaktivitet. NSD2 ökade en särskild histonmarkör (H3K36me2) vid deras promotorer och förstärkte därigenom deras uttryck. Återinsättning av dessa gener i NSD2‑defekta levercancerceller minskade mitokondriell syreförbrukning och ATP‑produktion, vilket bekräftar att de fungerar som NSD2:s nedströmsbromsar på oxidativ fosforylering. Tidigare arbete har visat att mycket aktiva mitokondrier tenderar att främja höga nivåer av PD‑L1 på tumörceller. I linje med detta fann författarna att NSD2‑överuttryck minskade PD‑L1‑nivåer, medan förlust av NSD2 ökade PD‑L1 på levercancerceller och i tumörvävnad.
Sänkning av skölden och väckande av immunangrepp
Den funktionella effekten av dessa molekylära skiften testades i möss som fick leverinjektioner av cancerceller konstruerade för att få eller förlora NSD2. Celler utan NSD2 bildade snabbt större tumörer, uttryckte mer PD‑L1 och infiltrerades av färre T‑celler och naturliga mördarceller, särskilt aktiverade mördande T‑celler. När forskarna kemiskt blockerade mitokondriens komplex V, en nyckelkomponent i oxidativ fosforylering, sjönk PD‑L1‑nivåerna i NSD2‑defekta celler tillbaka mot normala nivåer och immunceller kunde i högre grad inducera tumörcellsdöd. På liknande sätt minskade överuttryck av Camk2d eller Prkce i NSD2‑bristande celler, eller behandling av tumörer med en PD‑L1‑blockerande antikropp, tumörstorleken och återställde immuncellsinfiltration. I patientdataset kopplades lågt NSD2‑uttryck till sämre överlevnad men, intressant nog, till bättre respons på PD‑L1‑riktad terapi, vilket tyder på att NSD2‑status kan hjälpa till att förutsäga vem som har nytta av sådana läkemedel.
Vad detta betyder för framtida vård av levercancer
För en allmän läsare är huvudbudskapet att denna studie omdefinierar NSD2 som en tumörundertryckande faktor i levercancer, åtminstone i närvaro av ett fungerande immunsystem. Genom att dämpa cellens syreberoende energiproduktion sänker NSD2 indirekt PD‑L1 på tumörceller, tar bort en del av deras osynlighetsmantel och tillåter immunceller att känna igen och attackera dem. Denna nyupptäckta kedja NSD2–energi–PD‑L1 ger två praktiska idéer: för det första kan patienter vars tumörer saknar NSD2 vara särskilt lämpliga kandidater för PD‑L1‑blockerande läkemedel; och för det andra kan kombinationer av läkemedel som hämmar mitokondriell energiproduktion och immunoterapi erbjuda en kraftfull kombination mot levercancer.
Citering: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
Nyckelord: hepatocellulärt karcinom, NSD2, oxidativ fosforylering, PD-L1, tumörimmunoterapi