Clear Sky Science · sv
SNRPD2-medierad reglering av DDX39B-splitsning främjar endometriecancerprogression genom att undertrycka aktiveringen av CTSC-kryptiska exoner
Varför dolda budskap i cancergener är viktiga
Endometriecancer, en vanlig cancer i livmodern, ökar världen över, men många patienter med avancerad sjukdom har fortfarande få effektiva alternativ. Denna studie avslöjar hur en subtil process inne i cellerna — hur de klipper och klistrar i genetiska budskap — kan driva endometriala tumörer att växa och sprida sig. Genom att blottlägga ett sårbart "kopplingsschema" som cancerceller förlitar sig på pekar arbetet på nya sätt att stänga ner tumörer med precisa genetiska läkemedel.
En växande cancer i behov av nya svar
Endometriecancer är nu den vanligaste gynekologiska cancern i många västerländska länder, med fall och dödsfall som stadigt ökar både i väst och i Kina. Kirurgi, strålning, kemoterapi, hormonbehandling och immunterapi används alla, men de är långt ifrån perfekta. Att avlägsna livmodern slutar fertiliteten, hormonbehandlingar misslyckas ofta, och aggressiva tumörer återkommer ofta. Dessa utmaningar har fått forskare att söka djupare inne i cancercellerna efter molekylära svagheter som kan riktas med mer precisa terapier.
Cellens splitsningsmaskineri som en svag länk
För att fungera kopieras våra gener först till långa RNA-molekyler som måste trimmas och sys ihop i en process kallad splitsning. Specialiserade proteinmaskiner kallade spliceosomer avgör vilka bitar som behålls och vilka som kastas bort, och redigerar i praktiken det manus cellerna använder för att tillverka proteiner. Teamet fokuserade på en spliceosomkomponent kallad SNRPD2, en del av en familj av "Sm"-proteiner som hjälper till att sätta ihop splitsningsmaskineriet. Genom att gräva i stora databaser över cancer-gener och proteiner och undersöka patientprover fann de att nivåerna av SNRPD2 är markant högre i endometriala tumörer än i normal livmoderslemhinna, och att patienter vars tumörer har mer SNRPD2 tenderar att få sämre prognos.
Att stänga av en huvudredigerare bromsar tumörer
För att testa om SNRPD2 bara är en åskådare eller en aktiv drivkraft stängde forskarna ner den i endometriecancer-cellinjer odlade i labbet. När SNRPD2 tystades delade sig cellerna långsammare, bildade färre kolonier och var mindre kapabla att röra sig och invadera genom membran — beteenden kopplade till metastas. När dessa förändrade celler implanterades i möss var de resulterande tumörerna mycket mindre och visade färre celler i aktiv delning. Viktigt är att teamet utformade antisens-oligonukleotider — korta, läkemedelslika bitar av syntetisk DNA — som specifikt riktar in sig på SNRPD2:s RNA. I en patient-deriverad xenograftmodell, där mänskliga tumörfragment växer i immundefekta möss, minskade dessa antisensläkemedel kraftigt SNRPD2-nivåerna och tumörstorleken, vilket tyder på att SNRPD2 kan vara läkemedelsmål i kliniskt meningsfull utsträckning.
En trestegs-kedja från splitsningsfel till cancertillväxt
Genom att fördjupa sig i de genetiska data frågade forskarna hur förlust av SNRPD2 omkopplar RNA-budskap över genomet. De upptäckte att när SNRPD2 minskas börjar ett centralt RNA‑bearbetande enzym kallat DDX39B att fungera felaktigt. Normalt hjälper DDX39B till att avlägsna en särskild intron — ett RNA-segment som ska klippas bort — från sitt eget budskap. Utan tillräckligt med SNRPD2 lämnas denna intron kvar, vilket skapar en felaktig version av DDX39B-RNA som cellen snabbt förstör. Lägre DDX39B får sedan en kaskadeffekt på en annan gen, CTSC, som kodar för ett protein‑klyvande enzym känt för att understödja tumörtillväxt och spridning. Under friska förhållanden ignoreras en dold "kryptisk" exon i CTSC:s RNA, vilket tillåter celler att tillverka fullängds, aktiv CTSC-protein. Med reducerad DDX39B inkluderas denna kryptiska exon av misstag, vilket inför förtida stopp‑signaler i RNAt. Det missbildade CTSC-budskapet degraderas innan det kan producera mycket protein, och cancercellerna förlorar en del av sin aggressivitet.
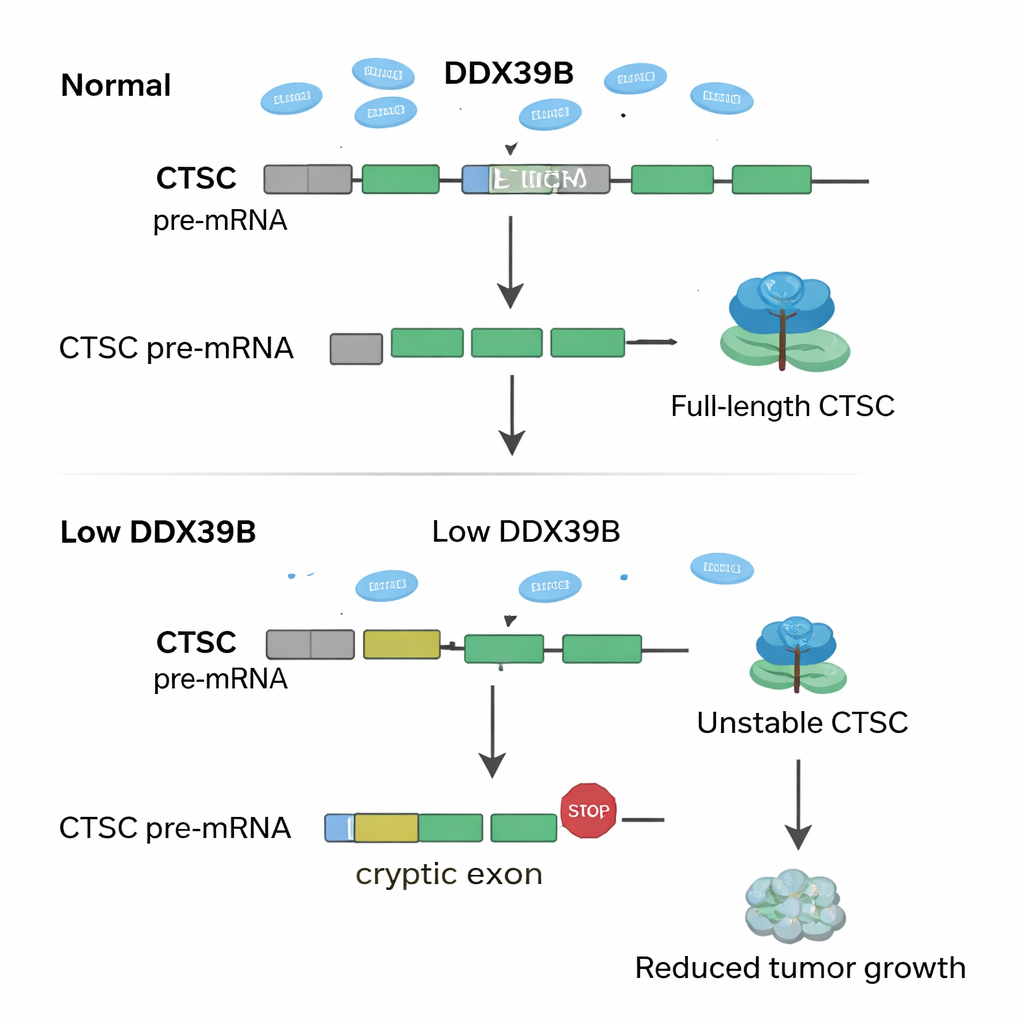
Vad detta betyder för framtida behandlingar
Enkelt uttryckt avslöjar författarna ett reläsystem — SNRPD2 → DDX39B → CTSC — som endometriecancerceller utnyttjar för att frodas. Hög SNRPD2 håller DDX39B rikligt; DDX39B förhindrar i sin tur att CTSC använder skadliga kryptiska exoner, vilket bevarar ett fullstarkt CTSC‑protein som hjälper tumörer att växa och sprida sig. När SNRPD2 blockeras kollapsar denna kedja, CTSC-nivåerna sjunker och tumörer försvagas. För icke‑specialister är huvudidén att cancerceller är beroende av mycket precis RNA‑redigering, och att även små påtvingade "misstag" kan selektivt förgifta deras tillväxt. Att rikta SNRPD2 med antisensläkemedel, eller att direkt tvinga användning av kryptiska exoner i CTSC, kan erbjuda nya, mer skräddarsydda terapier för patienter med endometriecancer.
Citering: Li, Y., Chen, Z., Liu, Y. et al. SNRPD2-mediated regulation of DDX39B splicing promotes endometrial cancer progression by suppressing the activation of CTSC cryptic exons. Cell Death Dis 17, 239 (2026). https://doi.org/10.1038/s41419-026-08489-4
Nyckelord: endometriecancer, RNA-splitsning, SNRPD2, DDX39B, CTSC