Clear Sky Science · sv
DNMT2 hämmar progressionen av anaplastisk thyroideacancer genom att nedreglera produktionen av 5’tiRNAGly-GCC
Varför denna dolda RNA-kemi spelar roll
Anaplastisk thyroideacancer är en av de mest dödliga cancerformerna hos människa och dödar ofta patienter inom månader trots operation, strålning och kemoterapi. Denna studie avslöjar en överraskande bov djupt inne i cancercellerna: små kemiska märken på transfer-RNA, molekylerna som hjälper till att bygga proteiner. Författarna visar att när ett visst enzym, DNMT2, går förlorat eller minskar, växer tyroideatumörer snabbare, sprider sig lättare och blir motståndskraftiga mot det vanliga cytostatikan doxorubicin. Ännu mer intrigant identifierar de en kort RNA-fragment som uppstår när DNMT2 är lågt och visar att blockering av detta fragment kan bli en ny behandlingsstrategi.
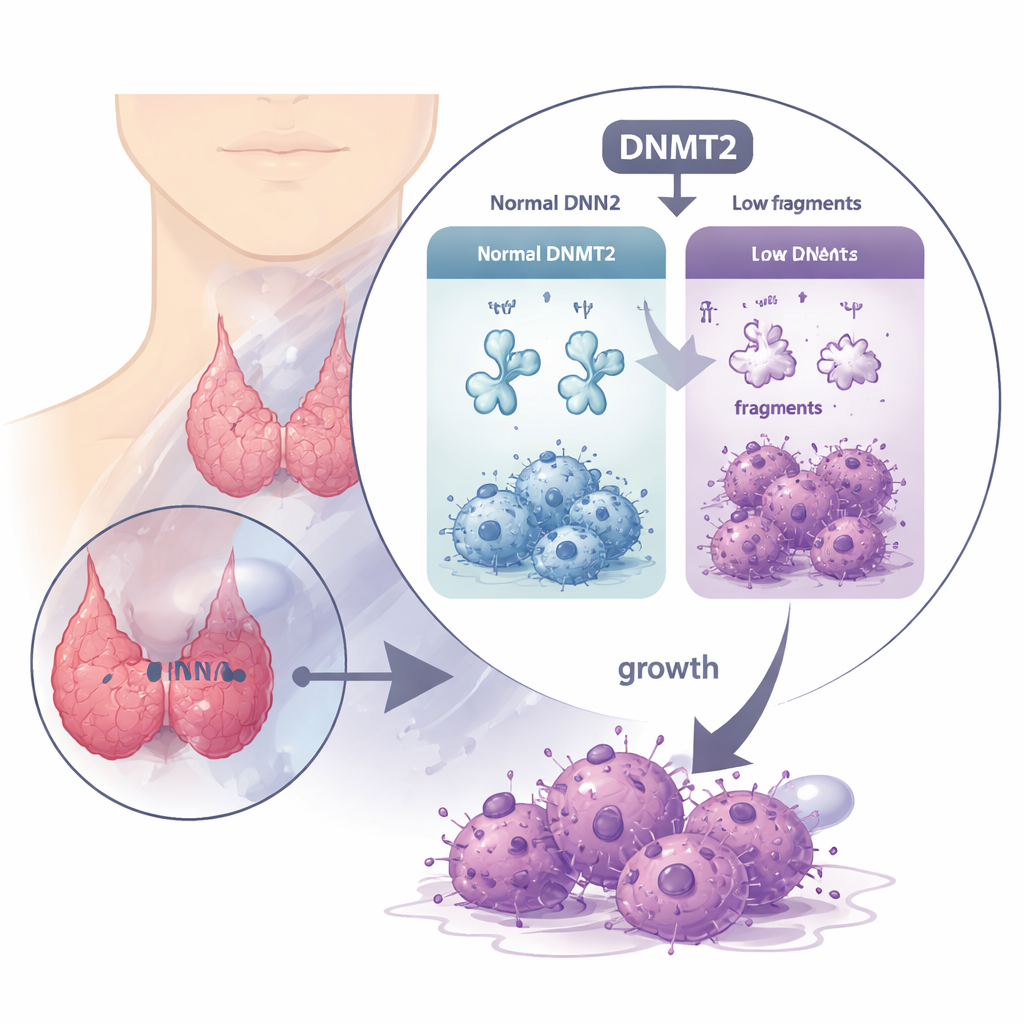
Ett skyddande enzym som försvinner
Transfer-RNA (tRNA) förmedlar normalt aminosyror till cellens proteintillverkning, och deras stabilitet beror på känsliga kemiska dekorationer. DNMT2 är ett enzym som lägger till ett sådant märke, en metylgrupp, på specifika platser på tRNA. I många cancerformer är DNMT2 förhöjt och anses stötta tumörer, men här är berättelsen den motsatta. Genom att analysera stora patientdatamängder och tumörprover fann forskarna att DNMT2-nivåerna är signifikant lägre i vävnad från anaplastisk thyroideacancer än i normal sköldkörtel. Patienter vars tumörer hade mer DNMT2 tenderade att leva längre utan att deras cancer förvärrades, vilket tyder på att DNMT2 i denna sjukdom fungerar mer som en broms än som en accelerator.
Hur låg DNMT2 driver aggressivt beteende
För att se vad DNMT2 faktiskt gör i cancerceller manipulerade teamet dess nivåer i cellinjer från anaplastisk thyroideacancer odlade i petriskålar och i musmodeller. När DNMT2 minskades delade cellerna snabbare, invaderade membraner lättare och bildade fler kolonier — alla kännetecken för en aggressiv tumör. Dessa celler blev också mindre känsliga för doxorubicin, ett standardläkemedel för denna cancer. I möss växte tumörer med reducerad DNMT2 större och spred sig lättare till lungorna, medan ökad DNMT2-uttryck gav motsatt effekt. Forskarna spårade delvis dessa förändringar till aktivering av ett cellulärt program som kallas epitel–mesenkymal transition, vilket gör cancerceller mer rörliga och invasiva.
Från skadat tRNA till skadliga små fragment
Vid djupare analys visar studien att DNMT2 sätter en metylmarkering vid en specifik position (kallad C38) på bara tre typer av tRNA. Utan detta skydd blir tRNA mer sårbara för klövning av ett annat enzym, angiogenin. Denna klyvning ger en kort RNA-bit härledd från tRNA-Gly-GCC, benämnd 5’tiRNAGly-GCC. Med hjälp av sekvensering och biokemiska tester fann författarna att när DNMT2 är låg så ansamlas detta fragment, särskilt från glycin-bärande tRNA. I provrörsexperiment skyddade tillsatsen av metylmarkeringen starkt tRNA mot att bli skuret, vilket bekräftar att DNMT2 normalt skyddar dessa molekyler från att hakas upp i mindre, potentiellt skadliga delar.
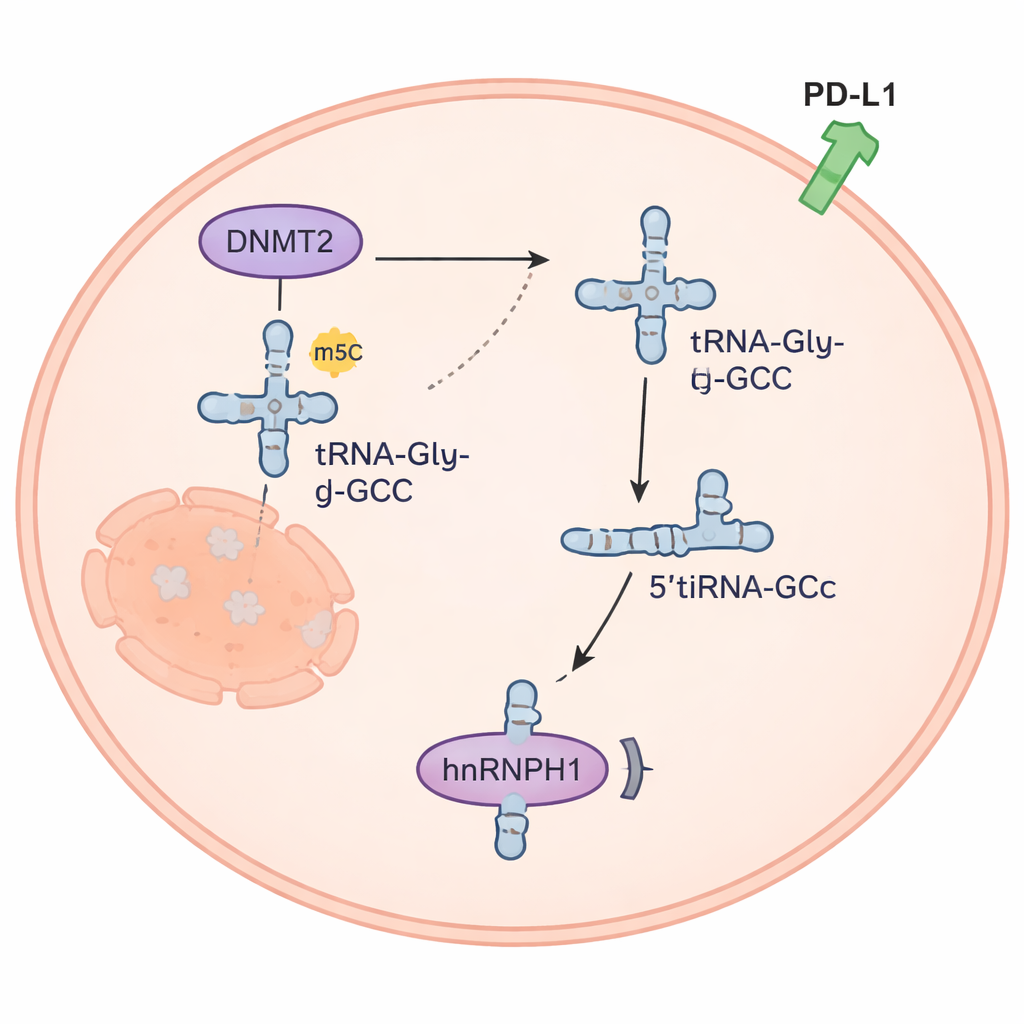
Ett litet RNA-fragment omkopplar cancersignaler
5’tiRNAGly-GCC-fragmentet visade sig vara mer än molekylärt skräp. Det var rikligt i celler från anaplastisk thyroideacancer men sällsynt i normala thyroideaceller. När forskarna artificiellt höjde dess nivåer prolifererade cancerceller snabbare, invaderade mer och blev mer resistenta mot doxorubicin; att sänka fragmentet hade motsatt effekt. I möss bromsade en kemiskt designad hämmare av 5’tiRNAGly-GCC tumörtillväxten, och kombinationen av denna hämmare med doxorubicin fungerade ännu bättre än någon av behandlingarna ensam. Teamet upptäckte att 5’tiRNAGly-GCC binder till ett protein kallat hnRNPH1 och minskar dess mängd inne i cellerna. Eftersom hnRNPH1 normalt hjälper till att hålla nivåerna av det immungerelaterade proteinet PD-L1 i schack, tillåter förlust av hnRNPH1 att PD-L1 ökar — en förändring som kan hjälpa tumörer att undkomma immunangrepp och är kopplad till ackumulering av regulatoriska T‑celler runt tumörer.
Vad detta betyder för framtida behandlingar
Kort sagt avslöjar studien en kedjereaktion: när DNMT2 är låg förlorar vissa tRNA ett skyddande märke, klipps till små fragment, och ett av dessa fragment (5’tiRNAGly-GCC) inaktiverar ett protein som begränsar PD-L1. Resultatet är en mer aggressiv, läkemedelsresistent och immunundvikande cancer. Istället för att försöka öka DNMT2 direkt — vilket kan vara riskabelt i andra vävnader — föreslår författarna att rikta in sig på det skadliga RNA-fragmentet självt. Deras musförsök med en 5’tiRNAGly-GCC-hämmare, särskilt i kombination med doxorubicin, ger tidigt bevis på att avbrott i denna mikroskopiska RNA-kretsgång skulle kunna hjälpa till att tygla en av de mest dödliga formerna av thyroideacancer.
Citering: Zhou, R., Li, B., Cao, M. et al. DNMT2 inhibits anaplastic thyroid cancer progression by downregulating 5’tiRNAGly-GCC production. Cell Death Dis 17, 240 (2026). https://doi.org/10.1038/s41419-026-08488-5
Nyckelord: anaplastisk thyroideacancer, DNMT2, tRNA-fragment, kemoresistens, PD-L1