Clear Sky Science · sv
Riktad påverkan på mitokondriell fosfatas PGAM5 lindrar ferroptos och akut pankreatit genom uppreglering av NRF2-medierad FSP1‑uttryck
Varför stressade celler och smärtsamma bukspottkörtlar spelar roll
När celler pressas för hårt kan de dö på sätt som skadar hela kroppen. En sådan form av celldöd, kallad ferroptos, drivs av järn och okontrollerade kemiska reaktioner som får fetterna i cellmembran att ”rosta”. Denna process har kopplats till organskador, inklusive ett smärtsamt och ibland livshotande tillstånd som kallas akut pankreatit. Studien bakom denna artikel avslöjar en viktig kontrollpunkt inne i mitokondrierna — cellens kraftverk — som kan skruva upp eller ner ferroptos, och visar hur blockering av denna brytare kan skydda pankreas i en musemodell.
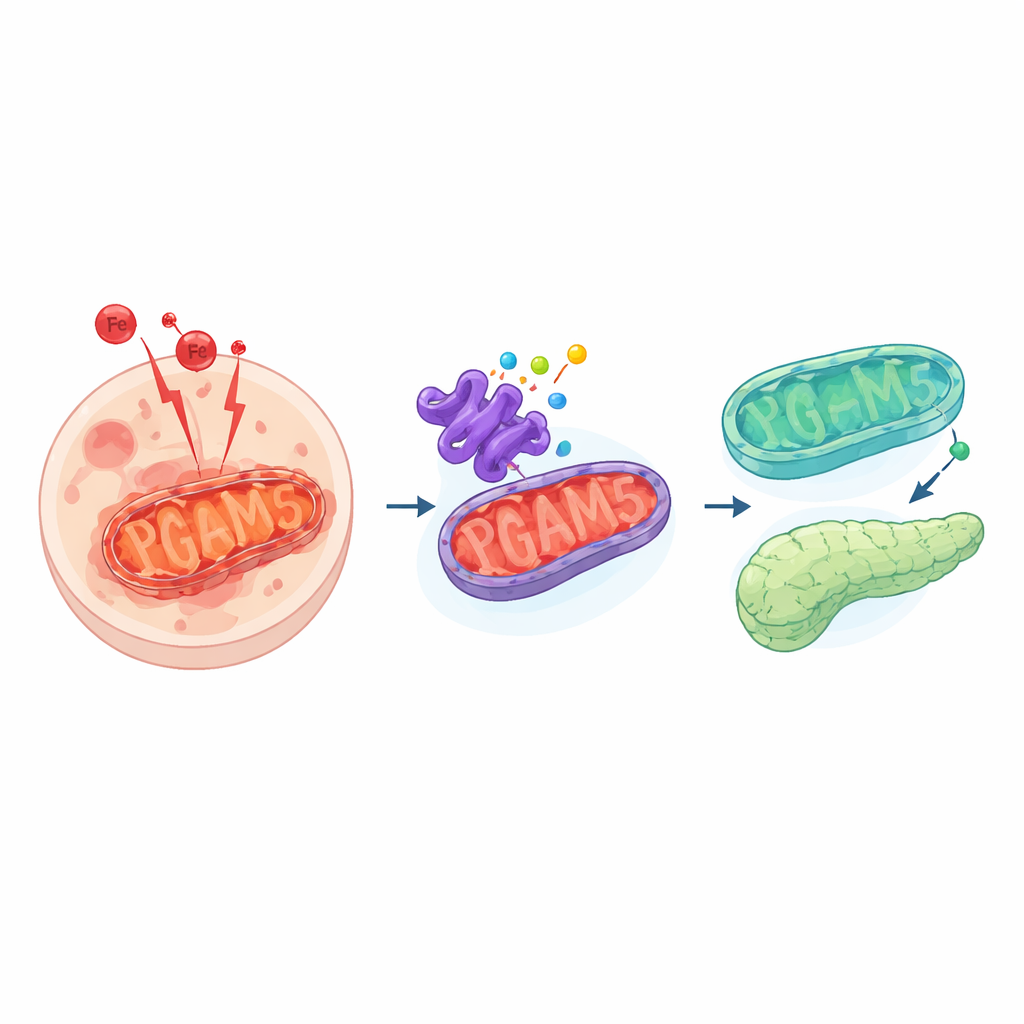
En farlig form av celldöd
Ferroptos skiljer sig från mer bekanta former av celldöd som apoptos. Istället för ordnad självdestruktion drabbas celler under ferroptos av en storm av järndrivna reaktioner som gör de känsliga fetterna i deras membran härskna. Detta skapar giftiga biprodukter och hål i membranen som slutligen dödar cellen. Vanligtvis håller cellerna detta i schack med skyddssystem som avgiftar dessa reaktiva molekyler. När dessa system fallerar eller överväldigas kan ferroptos sprida skada genom vävnader och bidra till sjukdomar från cancer till organsvikt.
En mitokondriell brytare i sikte
Forskarnas fokus låg på ett protein kallat PGAM5, som sitter på mitokondriens inre yta och fungerar som ett signalnav. PGAM5 hjälper till att kontrollera mitokondriernas form, svarar på stress och påverkar hur celler hanterar oxidation. Överraskande nog gjorde både minskad PGAM5-nivå och tvångsmässig överproduktion av proteinet cellerna svårare att döda genom ferroptos. Kemisk hämning av PGAM5, genetisk nedreglering och överuttryck minskade alla uppbyggnaden av skadliga lipidbiprodukter och reducerade celldöd som inducerades av ett ferroptosframkallande läkemedel. Detta visar att systemet är fininställt: både för lite och för mycket PGAM5 skjuter cellerna mot ett mer skyddat tillstånd.
Att slå på ett internt skydd
Vidare upptäckte författarna att PGAM5:s påverkan går via en skyddande axel som involverar två andra aktörer: NRF2 och FSP1. NRF2 är en huvudregulator som, när den är aktiv i kärnan, slår på ett brett spektrum av antioxidativa försvar. FSP1 är en av dess nedströmsförsvarare som hjälper till att regenerera en fettlöslig antioxidant och därigenom blockerar lipidskador vid cellmembranet. När PGAM5‑nivåerna ändrades ökade cellerna både budbärar-RNA och proteinnivåer för NRF2, och NRF2 förflyttades lättare från cytoplasman till kärnan. Där ökade den produktionen av FSP1. Blockering av FSP1 eller NRF2 utplånade skyddet och återställde känsligheten för ferroptos, vilket visar att denna PGAM5–NRF2–FSP1‑kedja är avgörande för den observerade motståndskraften.
Energistress som den dolda budbäraren
Studien avslöjade också hur mitokondriell stress omvandlas till detta skyddssvar. Störningar i PGAM5 rubbade mitokondriernas balans och försköt cellens energivaluta: förhållandet mellan lågenergimolekyler (AMP och ADP) och högenergi‑ATP ökade, vilket signalerade energistress. Detta aktiverade enzymet AMPK, som är känsligt för energistatus. Aktivt AMPK modifierade direkt NRF2 på ett sätt som främjade dess inträde i kärnan och ytterligare ökade FSP1‑produktionen. När AMPK togs bort ur systemet ackumulerades inte längre NRF2 i kärnan, FSP1‑nivåerna sjönk och cellerna gav åter vika för ferroptos. Således kopplar PGAM5 mitokondriellt tillstånd till ett bredare energi‑ och antioxidantprogram som skyddar celler från järndriven död.
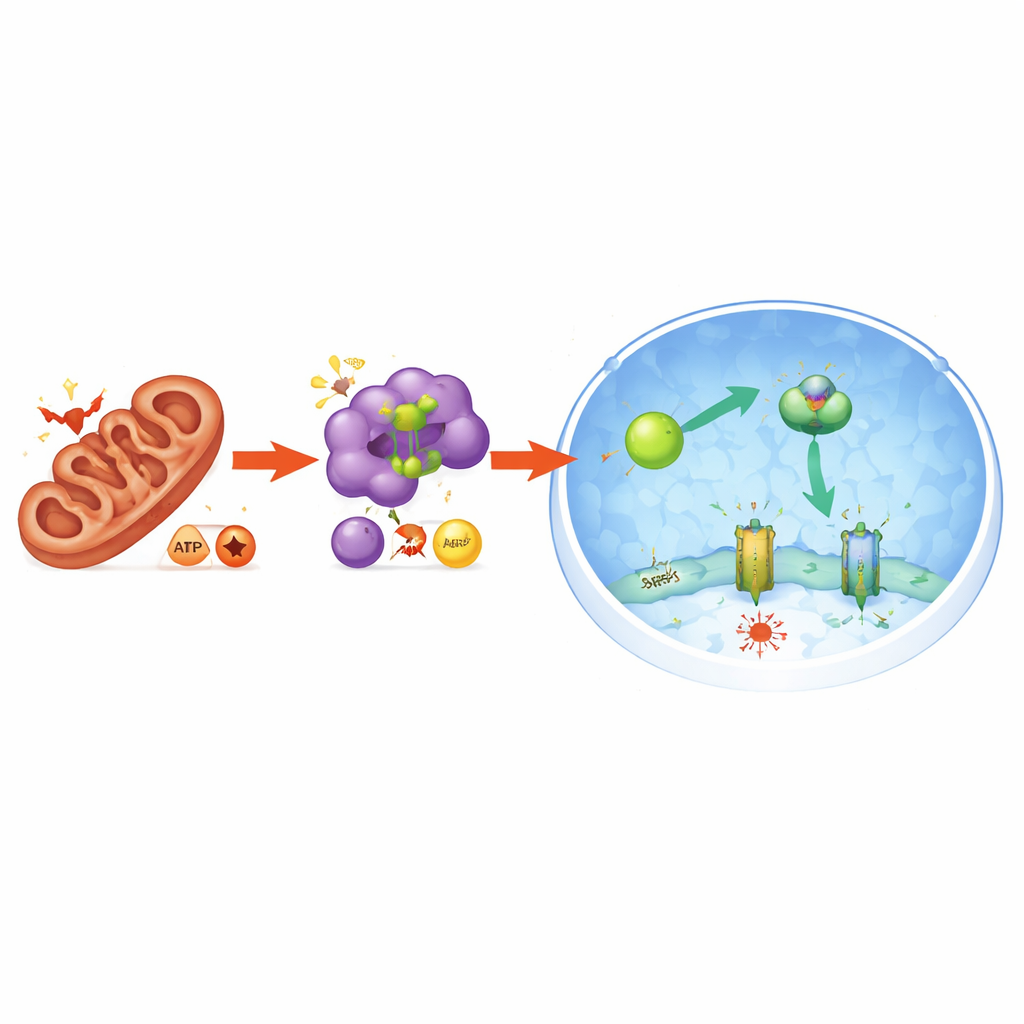
Att skydda pankreas i levande djur
För att pröva om denna mekanism är betydelsefull i ett helt organ använde forskarna en musemodell för akut pankreatit utlöstad av höga doser av aminosyran arginin. I denna modell uppvisar pankreas omfattande skador, förhöjda nivåer av blodenzymer som signalerar vävnadsskada och en våg av inflammatoriska molekyler. Markörer för lipidperoxidation — ett kännetecken för ferroptos — ökade också kraftigt i pankreas. Behandling av möss med en PGAM5‑hämmande förening mildrade dessa symtom: blodets skademarkörer sjönk, pankreasvävnaden såg friskare ut i mikroskopet och inflammatoriska signaler minskade. Samtidigt föll ferroptosmarkörerna, medan AMPK‑aktivitet samt NRF2‑ och FSP1‑nivåer ökade i pankreas, i linje med den skyddande väg som sågs i cellodling.
Vad detta betyder för framtida behandlingar
Sammantaget identifierar arbetet PGAM5 som en central kontrollpunkt som länkar mitokondriell stress, cellens energitillstånd och ett kraftfullt antioxidativt program som blockerar ferroptos. Genom att dämpa PGAM5‑aktivitet aktiverar celler AMPK och NRF2, ökar FSP1 och står bättre emot järndrivna lipidskador. I möss minskar denna strategi pankreasskada vid akut pankreatit. För en lekmannaläsare är budskapet att forskare funnit en ny intern ”strömställare” som kan förhindra en destruktiv form av celldöd. Även om mycket återstår innan klinisk användning, kan riktning mot PGAM5 eller dess nedströmsaktörer öppna nya vägar för behandling av tillstånd där ferroptos och mitokondriellt haveri spelar en skadlig roll.
Citering: Ma, S., Qin, J., Luan, J. et al. Targeting mitochondrial phosphatase PGAM5 alleviates ferroptosis and acute pancreatitis by upregulating NRF2-mediated FSP1 expression. Cell Death Dis 17, 252 (2026). https://doi.org/10.1038/s41419-026-08484-9
Nyckelord: ferroptos, mitokondrier, akut pankreatit, oxidativ stress, celldöd