Clear Sky Science · sv
Målinriktning av fettsyresyntas hämmar tumörutveckling i NF2/CDKN2A-bristfällig pleural mesoteliom
Varför detta är viktigt för personer som exponerats för asbest
Pleural mesoteliom är en sällsynt men nästan alltid dödlig cancer som växer på lungsäckens beklädnad, oftast efter asbestexponering flera decennier tidigare. När sjukdomen väl konstaterats är den svår att behandla och svarar ofta dåligt på standardkemoterapi. Denna studie undersöker en annan infallsvinkel: istället för att angripa tumören med traditionella cytostatika försöker forskarna svälta ut cancercellerna genom att stänga av en viktig källa till byggstenar och energi, vilket pekar mot en mer skräddarsydd behandling för en stor genetisk undergrupp av mesoteliom.
Hur tumörceller missbrukar fettbildande mekanismer
Många cancerformer ökar aktiviteten hos ett enzym kallat fettsyresyntas, som sätter ihop långkedjiga fetter som celler använder för att bygga membran, lagra energi och reglera signalering. Teamet fokuserade på mesoteliomceller som saknar två tumörskyddande gener, NF2 och CDKN2A (även känd som p16), förändringar som är vanliga i denna sjukdom. Genom att screena 364 antitumörsubstanser fann de att en molekyl, cerulenin, som blockerar fettsyresyntas, var särskilt effektiv på att bromsa tillväxten av NF2/p16-bristfälliga mesoteliomceller. I kontrast var andra läkemedel, inklusive en annan fettsyresyntas-hämmare kallad C75 och standardmedlen cisplatin och pemetrexed, mycket mindre effektiva vid jämförbara doser.
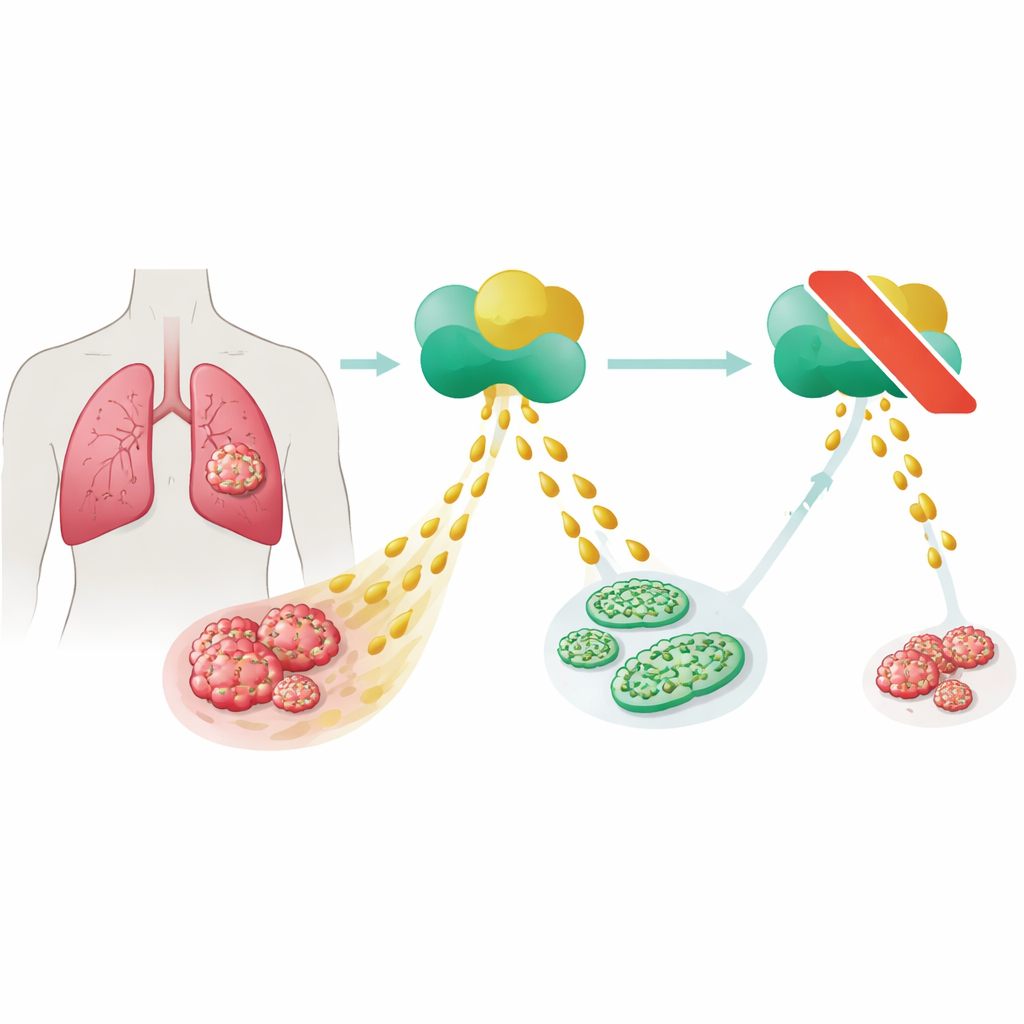
Koppling mellan ett fettbildande enzym och patienttumörer
För att avgöra om detta enzym verkligen spelar roll vid mänsklig sjukdom undersökte forskarna vävnadsprover från 45 personer med pleural mesoteliom och jämförde dem med normal pleuraveck. De fann fettsyresyntasprotein i varje tumör som förlorat både NF2 och p16, men bara i ungefär en tredjedel av tumörerna där dessa gener var intakta, och inte alls i normal vävnad. När de vände sig till en stor publik cancer-databas hade patienter vars mesoteliom uttryckte högre nivåer av fettsyresyntasgenen kortare överlevnad totalt än de med lägre nivåer. Tillsammans tyder dessa fynd på att enzymet inte bara är en åskådare utan är nära kopplat till aggressivt tumörbeteende i denna cancermetastas.
Test av ett målinriktat läkemedel i djur
Nästa steg var att undersöka om blockad av fettsyresyntas kunde krympa tumörer i levande organismer. Forskarna implanterade mänskliga NF2/p16-bristfälliga mesoteliomceller under huden på immundefekta möss och behandlade dem med antingen cerulenin eller en ofarlig saltlösning. Cerulenin bromsade dramatiskt tumörtillväxten utan att orsaka viktnedgång eller synlig skada på hjärta, lever eller njurar. Blodprover för lever- och njurfunktion, elektrolyter, fetter och socker höll sig också inom normala intervall. Dessa resultat visar att cerulenin, åtminstone i detta experimentella sammanhang, kan dämpa tumörtillväxt samtidigt som det verkar relativt säkert.
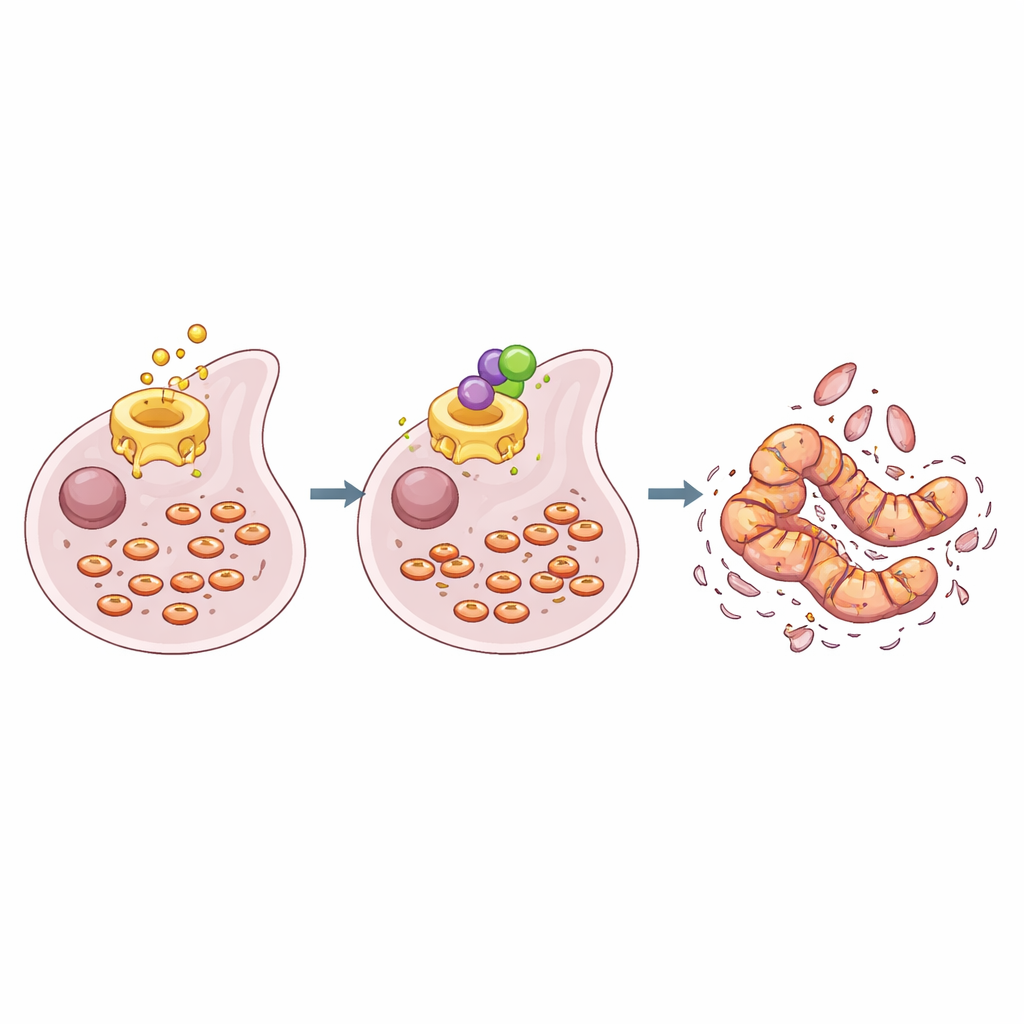
Hur omkoppling av cellernas kraftverk driver cancerceller mot död
Cancerceller är starkt beroende av sina mitokondrier, de små strukturer som producerar det mesta av cellens energi. Dessa mitokondrier delar sig och fusionerar ständigt, och denna balans förändras vid sjukdom. I NF2/p16-bristfälliga mesoteliomceller stödde fettsyresyntasaktivitet ett mönster av många små, fragmenterade mitokondrier och aktiva signaler som främjar cellsurvival. När forskarna tillsatte cerulenin smälte mitokondrierna i dessa celler samman till långa, tubulära nätverk och aktiviteten hos DRP1, ett protein som driver mitokondriell delning, minskade. Signalering genom en större tillväxtväg (PI3K–AKT–mTOR) och ett tillväxtkontrollsystem känt som Hippo–YAP dämpades också. Flödescytometri och proteinanalyser visade att fler behandlade celler genomgick programmerad celldöd, markerad av ökade nivåer av klyvt PARP och klyvd caspas-3.
Genetiskt bevis att fettsyresyntas är ett sårbart mål
För att bekräfta att dessa effekter verkligen orsakades av blockad av fettsyresyntas och inte av off-target-effekter av cerulenin använde teamet CRISPR-genteknik för att ta bort fettsyresyntasgenen i NF2/p16-bristfälliga mesoteliala celler och skapade så kallade ”trippel knockout”-celler. Dessa redigerade celler växte långsammare, hade mer sammansmälta, förlängda mitokondrier och visade minskade DRP1-nivåer men ökade nivåer av proteiner som främjar mitokondriell fusion. De genererade också mer reaktiva syreradikaler, ett tecken på stressade mitokondrier, och uppvisade fler markörer för apoptos. Ytterligare experiment föreslog att utan fettsyresyntas blir DRP1 mer märkt med ubiquitin och bryts ner, vilket ytterligare tippar balansen mot mitokondriell fusion och celldöd.
Vad detta kan betyda för framtida behandling
Sammantaget visar studien att mesoteliomceller som saknar NF2 och p16 är beroende av fettsyresyntas för att hålla sina energifabriker i ett pro-tillväxttillstånd och för att upprätthålla starka överlevnadssignaler. Att blockera detta enzym med cerulenin försvagar selektivt dessa tumörer i celler, i mänskliga vävnadsprover och i möss, samtidigt som normal vävnad i det korta perspektivet skonas. För patienter antyder detta arbete att läkemedel som riktar sig mot fettsyresyntas, särskilt i tumörer som testats för förlust av NF2 och CDKN2A, skulle kunna bli en del av en precisionmedicinsk strategi som utnyttjar en specifik metabolisk sårbarhet hos deras cancer.
Citering: Karnan, S., Ota, A., Hasan, M.N. et al. Targeting fatty acid synthase suppresses tumor development in NF2/CDKN2A-deficient pleural mesothelioma. Cell Death Dis 17, 287 (2026). https://doi.org/10.1038/s41419-026-08481-y
Nyckelord: pleural mesoteliom, fettsyresyntas, cerulenin, mitokondriell dynamik, precision-onkologi