Clear Sky Science · sv
UBE3A-medierad ubiquitinering av mH2A1 aktiverar TERT-transkription för att främja resistens mot senescens i bukspottkörtelcancer
Varför denna forskning är viktig för patienter
Bukspottkörtelcancer är en av de dödligaste cancerformerna, delvis eftersom tumörceller är ovanligt skickliga på att undvika kroppens inbyggda åldringsbroms. Denna studie avslöjar en dold molekylär ”sabotagekrets” som hjälper bukspottkörtelcancerceller att förbli unga, fortsätta dela sig och motstå behandling. Genom att förstå denna krets pekar forskarna på ett nytt sätt att tvinga dessa celler in i åldrande och därefter selektivt rensa ut dem, vilket öppnar dörren för smartare kombinationsbehandlingar.
Åldrande som kroppens naturliga tumörbroms
Alla celler bär på en intern klocka som så småningom får dem att sluta dela sig, en process som kallas senescens. I tidiga förändringar i bukspottkörteln kan denna klocka sakta tumörutvecklingen genom att sätta precancerösa celler i permanent pensionering. Många anticancerbehandlingar fungerar också delvis genom att tvinga tumörceller i detta åldrade tillstånd. Om dessa senescenta celler inte rensas bort kan de däremot driva inflammation och bidra till att cancern återkommer. Det har lett till en ny behandlingsidé: först tvinga cancerceller i senescens, och sedan eliminera dessa åldrade celler med ”senolytiska” läkemedel som är särskilt giftiga för dem.
En cancerfrämjande enzym i strålkastarljuset
För att hitta gener som hjälper bukspottkörtelcancerceller att trotsa senescens grävde gruppen i stora patientdatamängder och validerade sina fynd i tumörprover och cellinjer. De fastnade för ett protein kallat UBE3A, ett enzym som märker andra proteiner för nedbrytning. UBE3A-nivåerna var mycket högre i bukspottkörteltumörer än i omgivande normalt vävnad, och patienter med mer UBE3A tenderade att ha större, mer avancerade tumörer och sämre överlevnad. I odlingsceller påskyndade ökat UBE3A tillväxten, minskade klassiska markörer för cellulärt åldrande och reducerade de inflammatoriska sekret som är typiska för senescenta celler. Tystande av UBE3A gav motsatt effekt och i musmodeller minskade tumörtillväxt och levermetastaser kraftigt. 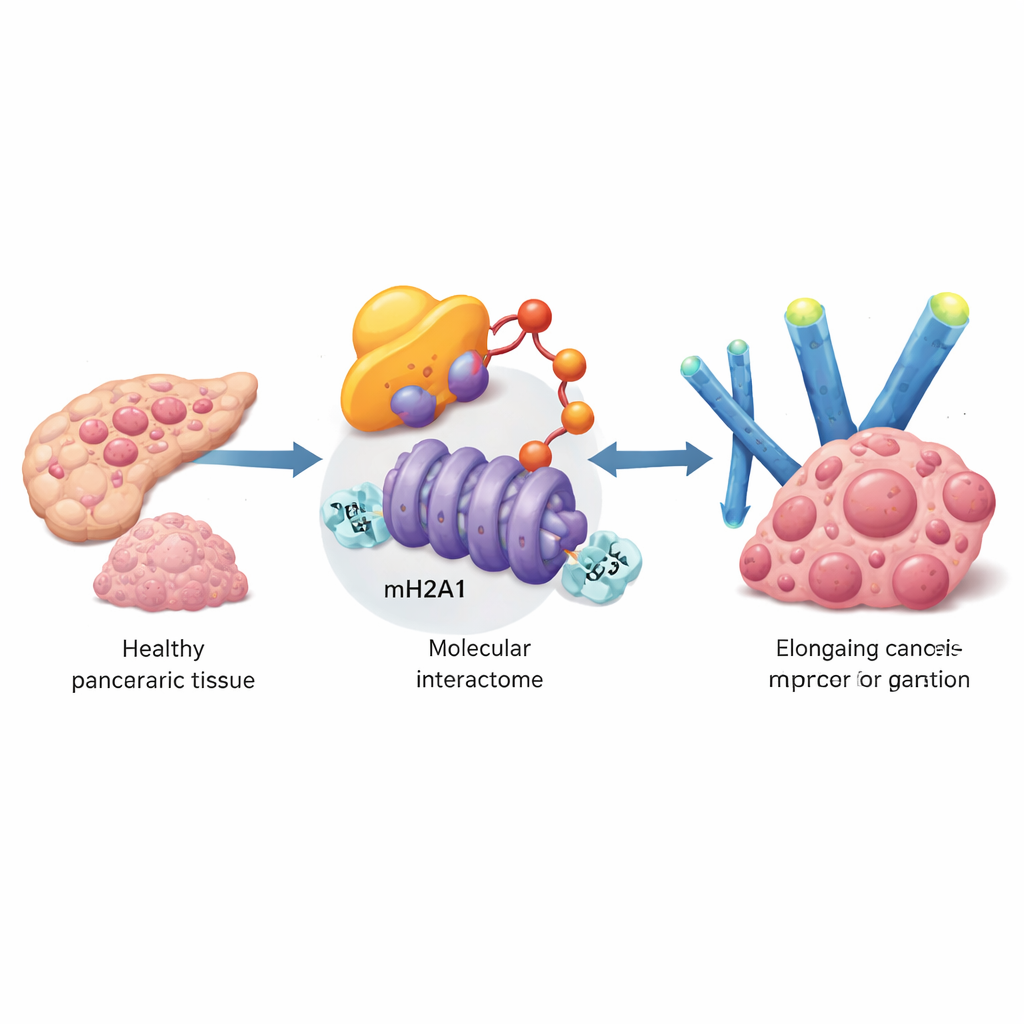
Hur cancerceller suddar ut en kromatinbroms
Genom att gå djupare undersökte forskarna vilka molekyler UBE3A verkar på. Med avancerade masspektrometriscreeningar fann de att UBE3A binder till och kemiskt märker en speciell histonvariant kallad macroH2A1 (mH2A1), som hjälper till att kompakta DNA och vanligtvis fungerar som en broms på genaktivitet. UBE3A fäster en kedja av ”förstör mig”-märken på mH2A1 vid en specifik position, vilket gör att det bryts ner av cellens proteinröjningsmaskineri. I bukspottkörteltumörer var mH2A1-nivåerna lägre där UBE3A var hög, och återställande av mH2A1 motverkade UBE3A:s förmåga att blockera senescens och driva tumörtillväxt. Detta avslöjar ett nyckelsteg: bukspottkörtelcancerceller avlägsnar en skyddande kromatinmarkör genom att använda UBE3A för att eliminera mH2A1.
Att låsa upp telomeras för att hålla celler unga
Nästa fråga var vilka gener som frigörs när mH2A1 tas bort. Genom att kombinera RNA-sekvensering och kartor över DNA-bindning identifierade gruppen telomerasgenen TERT som ett centralt mål. Telomeras upprätthåller de skyddande hättorna på kromosomändar, vilket gör att celler kan fortsätta dela sig istället för att gå in i senescens. Studien visar att mH2A1 normalt sitter vid en enhancerregion inom TERT-genen, där den rekryterar ett annat enzym, EZH2, för att lägga på en repressiv kemisk mark på närliggande histoner. Denna kombination håller TERT nedreglerad och tillåter telomererna att förkortas. När UBE3A förstör mH2A1 upplöses den repressiva komplexet, enhancern blir aktiv, TERT slås på, telomererna bibehålls och bukspottkörtelcancerceller får ökad resistens mot åldrande. Mutanta former av UBE3A som inte kan märka proteiner, eller mutant mH2A1 som inte kan märkas, bryter denna krets och återställer senescensbromsen.
Att kombinera induktion av senescens med senolytisk rensning
Slutligen testade forskarna om denna väg kunde utnyttjas terapeutiskt. Att slå ner UBE3A tvingade bukspottkörtelcancerceller mot senescens och ökade deras beroende av anti-död-proteiner i BCL-2-familjen — en känd sårbarhet hos senescenta celler. Gruppen kombinerade sedan UBE3A-hämning med ABT-263, ett senolytiskt läkemedel som riktar sig mot dessa överlevnadsproteiner. I kultiverade celler orsakat kombinationsbehandlingen att många fler cancerceller gick in i programmerad celldöd än vid någon av behandlingarna för sig. I musmodeller krympte tumörer med reducerat UBE3A ännu mer när djuren gavs ABT-263, och markörer för cellproliferation inuti tumörerna föll kraftigt. 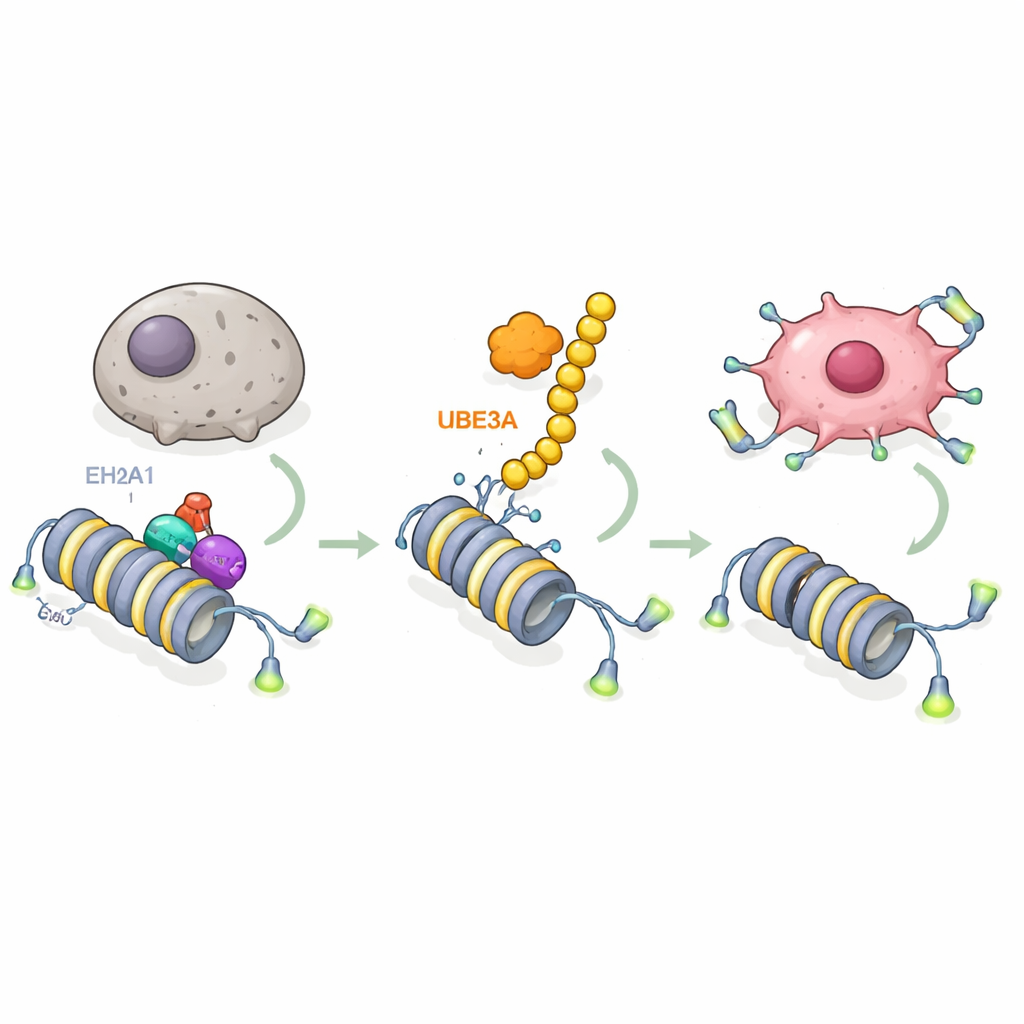
Vad detta betyder för framtida behandling
Detta arbete avslöjar en detaljerad händelsekedja genom vilken bukspottkörtelcancerceller undviker att bli gamla: UBE3A förstör kromatinbromsen mH2A1, vilket i sin tur lyfter repressionen av telomerasgenen TERT och hjälper till att upprätthålla telomererna så att cellerna kan fortsätta dela sig. Genom att rikta in sig på UBE3A kan man möjligen återaktivera cellens naturliga åldringsprogram och sedan använda senolytiska läkemedel som ABT-263 för att selektivt eliminera dessa sårbara, åldrade cancerceller. Även om fler studier behövs för att översätta denna mekanism till patientbehandlingar erbjuder UBE3A–mH2A1–TERT-axeln ett lovande nytt grepp om en av de mest behandlingsresistenta cancerformerna.
Citering: Ren, L., Lu, R., Fei, X. et al. UBE3A-mediated mH2A1 Ubiquitination activates TERT transcription to promote senescence resistance in pancreatic cancer. Cell Death Dis 17, 274 (2026). https://doi.org/10.1038/s41419-026-08480-z
Nyckelord: bukspottkörtelcancer, cellulär senescens, telomeras, ubiquitin-ligas, senolytisk terapi