Clear Sky Science · sv
En liten molekylär hämmare av ARF GTPase-protein 1 begränsar lever- och koloncansertillväxt samt metastasering
Varför denna forskning är viktig
Lever- och koloncancer hör till de dödligaste tumörtyperna, och nuvarande behandlingar krymper ofta tumörer men ger svåra biverkningar. Denna studie undersöker en ny typ av läkemedel som inte enbart förgiftar snabbt delande celler, utan istället tar sig in i cancercellen och sliter isär ett proteinmässigt "kontrollnav" som cellerna förlitar sig på för att växa och sprida sig. Genom att rikta in sig på detta nav strävar den experimentella föreningen efter att bromsa tumörtillväxten samtidigt som frisk vävnad skonas.
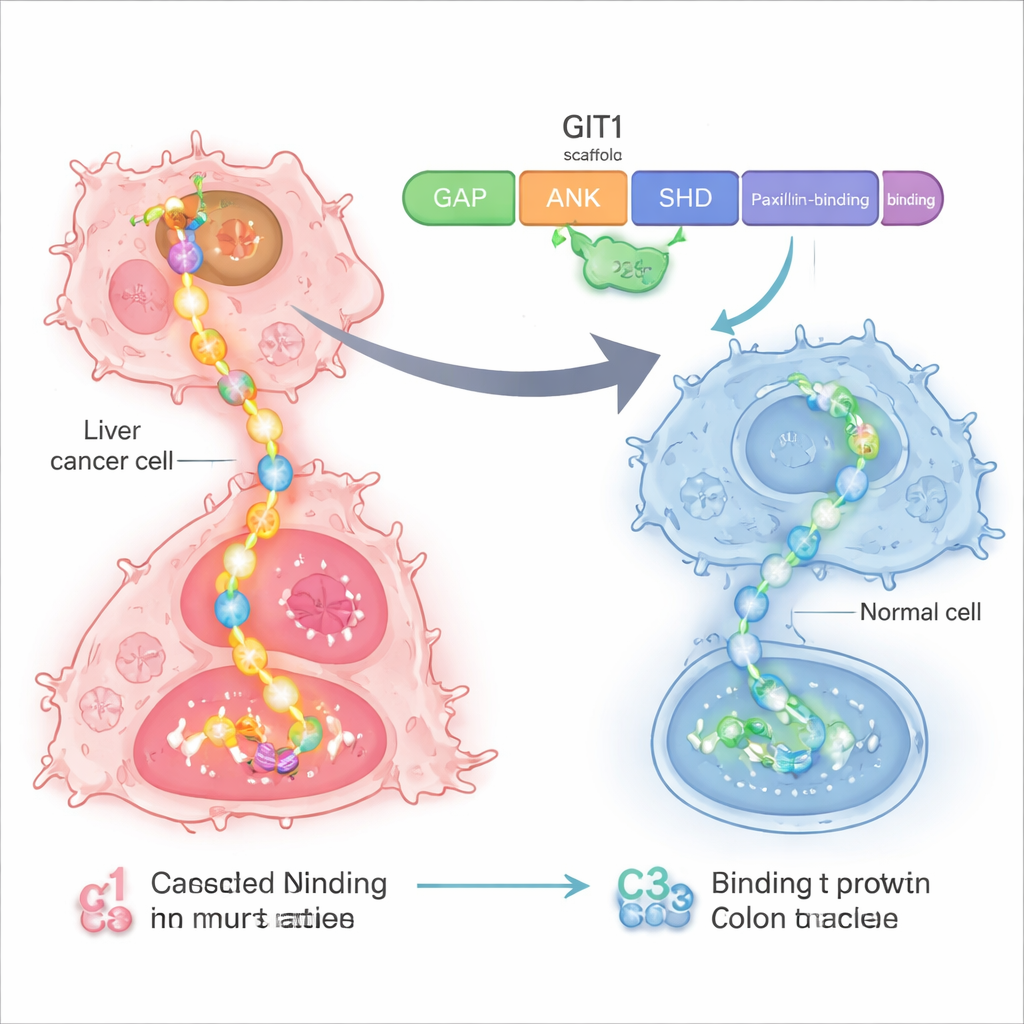
Ett sårbart kontrollnav inne i cancerceller
Forskarna fokuserade på ett protein kallat GIT1, som fungerar som ett stommeprotein eller ett grenuttag inne i cellen. I lever- och koloncancer överproduceras GIT1 och dess partnerprotein MAT2B. Tillsammans monterar de flera komponenter i en viktig tillväxtväg känd som RAS–RAF–MEK–ERK, en signalkedja som uppmanar celler att dela sig och migrera. Tidigare arbete visade att när GIT1 och MAT2B är rikliga växer lever- och kolonstumörer snabbare och sprider sig lättare, och när dessa proteiner minskas avtar cancerns tillväxt. Det gjorde GIT1–MAT2B-stommen till ett attraktivt mål för en mer precis terapi.
Att designa en liten molekyl utan ritning
En viktig utmaning var att GIT1:s tredimensionella kristallstruktur inte finns tillgänglig, så teamet kunde inte bara "titta upp" proteinets form. Istället använde de datorbaserad modellering för att förutsäga strukturen hos en region av GIT1 bestående av ankyrinupprepningar, belägen nära där MAT2B och andra signalproteiner binder. De genomförde därefter virtuell screening av ett stort bibliotek av små molekyler mot denna modell för att se vilka som kunde binda in till området. Av nio kandidater som testades i celler framstod en molekyl — kallad förening 3 (C3) — som särskilt intressant. C3 band specifikt till GIT1, men inte till dess nära släkting GIT2, och reducerade aktiviteten i ERK-tillväxtsignalen i flera cancercellinjer.
Att stoppa cancerceller från att dela sig och sprida sig
När lever- och koloncancerceller behandlades med C3 avstannade deras tillväxt, och vid högre doser dog många celler, medan icke-cancerogena lever- och njurceller förblev stort sett opåverkade. C3 fick cancerceller att stanna vid gränsen mellan G2- och M-faserna i cellcykeln, kontrollpunkten precis före och under mitos när en cell delar sig i två. Föreningen minskade också kraftigt cancercellernas förmåga att bilda kolonier och att migrera över en yta — två laboratoriemått kopplade till tumöråterväxt och metastasering. På molekylär nivå försvagade C3 interaktionerna mellan GIT1, MAT2B och RAF–MEK–ERK-signalproteinerna, vilket ledde till lägre MEK- och ERK-aktivitet och mindre av cellcykeldrivaren cyklin D1.
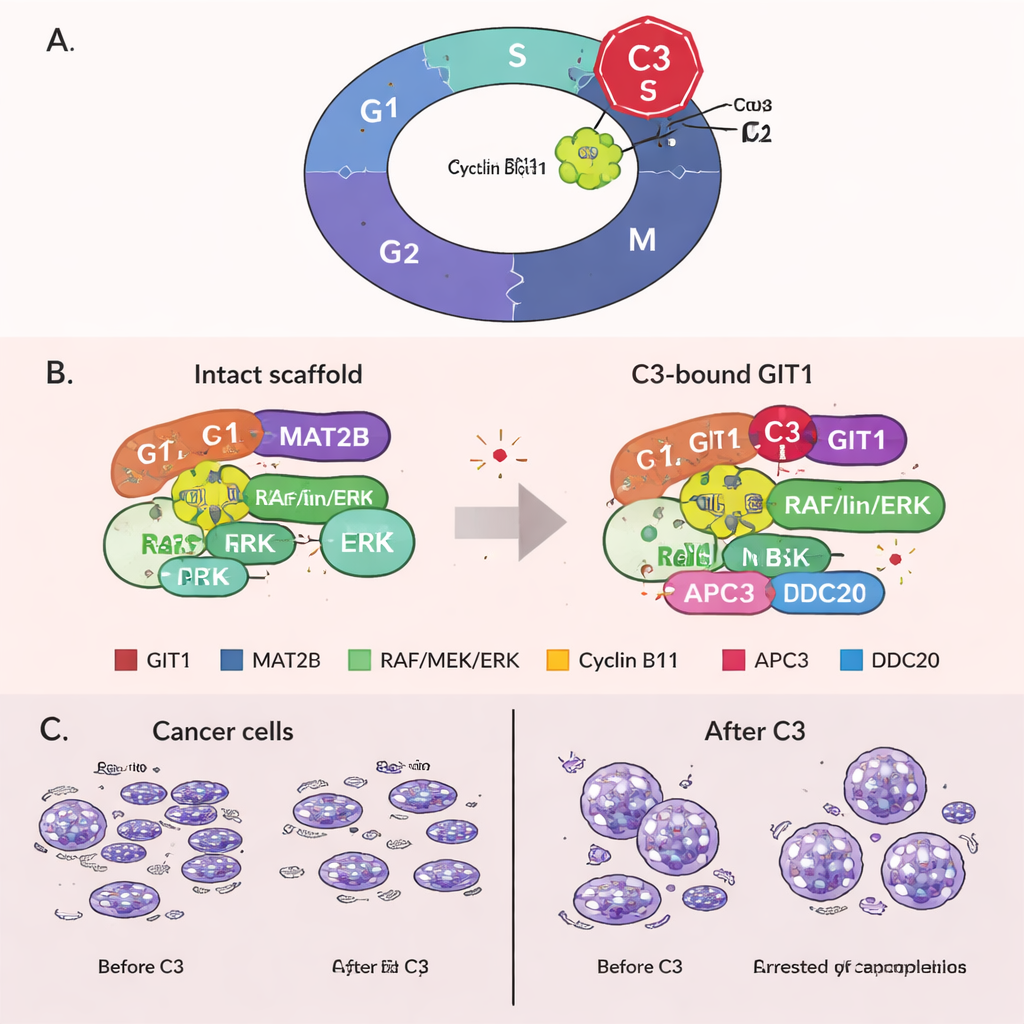
Att låsa celler i mitos genom en nyligen upptäckt funktion hos GIT1
Överraskande nog upptäckte teamet en ny roll för GIT1 i de sista stegen av celldelningen. De fann att GIT1 binder till cyklin B1, ett protein som hjälper celler att gå in i mitos, och även till delar av ett proteinkomplex kallat anaphase-promoting complex (APC/C), som normalt märker cyklin B1 för nedbrytning så att celler kan lämna mitosen. C3-behandling stärkte bindningen mellan GIT1 och cyklin B1 men försvagade kopplingarna mellan GIT1, cyklin B1 och APC/C-komponenterna. Som ett resultat bröts inte cyklin B1 effektivt ned, dess nivåer förblev höga och cellerna fastnade i mitos. Denna förlängda arrest är känd för att utlösa celldöd, vilket ger ett andra sätt för C3 att döda cancerceller. Viktigt är att när GIT1 experimentellt sänktes förlorade C3 mycket av sin förmåga att öka cyklin B1, blockera cellcykeln och hämma tillväxt, vilket visar att dess effekter verkligen är GIT1-beroende.
Lovande resultat i djurmodeller
Forskarna gick sedan vidare till musmodeller för att se om C3 kunde fungera i levande organismer. I immunkompetenta möss med inplanterade kolorektala tumörer bromsade injektioner av C3 direkt i tumörerna deras tillväxt kraftigt utan uppenbar toxicitet mot större organ. I två ytterligare modeller — mänskliga koloncancerceller som växte i levern hos immundefekta möss, och muskoloncancerceller som spridit sig till levern hos immunkompetenta möss — minskade C3 givet intraperitonealt tumörbörda och tecken på spridning. Blodprov och vävnadsundersökningar antydde att behandlingarna tolererades väl, och farmakokinetiska studier visade att läkemedelsnivåerna i blodomloppet förblev tillräckligt höga under flera timmar efter dosering.
Vad detta kan innebära för framtida cancerbehandlingar
För en icke-specialist är huvudbudskapet att forskarna funnit ett sätt att angripa cancer inte genom att rikta in sig på ett enskilt muterat enzym, utan genom att störa en multiproteinansamling som cancerceller är beroende av för både tillväxtsignaler och korrekt celldelning. Deras små molekyl, C3, binder specifikt till GIT1, omformar dess nätverk av partnerproteiner, dämpar en viktig tillväxtväg och fångar cancerceller i en dödlig trafikkö under mitos. Även om C3 fortfarande är ett experimentellt verktyg och ännu inte ett läkemedel för patienter, visar arbetet att inriktning mot stommeproteiner som GIT1 kan öppna en ny väg för behandling av lever- och koloncancer med större precision och potentiellt färre biverkningar.
Citering: Peng, H., Chhimwal, J., Fan, W. et al. A small molecule inhibitor of ARF GTPase protein 1 limits liver and colon cancer cell growth and metastasis. Cell Death Dis 17, 238 (2026). https://doi.org/10.1038/s41419-026-08477-8
Nyckelord: levercancer, koloncancer, målinriktad terapi, cellcykelstopp, stommeprotein