Clear Sky Science · sv
Omkoppling av melanomcellers öde: TRPM8-modulatorer utlöser apoptos och ökar NK-cellers cytotoxicitet
Varför det är viktigt att vända en “kallsensor” mot hudcancer
Melanom är en farlig form av hudcancer som ofta lär sig undvika både läkemedel och immunsystemet. Denna studie undersöker en oväntad sårbarhet i melanomceller: ett protein kallat TRPM8, mest känt som sensorn som låter nervceller uppfatta kyla eller mentol. Forskarna visar att noggrant designade läkemedel som blockerar TRPM8 kan få melanomceller att självdestruera samtidigt som de blir lättare för naturliga mördarceller (NK-celler) i immunsystemet att attackera. Denna dubbla verkan pekar på en ny strategi för att behandla envisa, avancerade melanom.
En dold strömbrytare på melanomceller
Genom att analysera stora cancer-databaser och studera patienthärledda melanomceller i laboratoriet fann teamet att TRPM8 är mycket mer uttryckt i metastatiskt melanom än i normal hud, inklusive friska melanocyter och dermala fibroblaster. Med hjälp av bildtekniker visade de att TRPM8 finns både på cellytan och på interna membran, vilket placerar kanalen i strategiska lägen för att påverka cellbeteende. När de testade en panel nya TRPM8-riktade molekyler utmärkte sig två föreningar (benämnda 4 och 9): de minskade markant melanomcellernas överlevnad över tid samtidigt som normala hudceller i stort sett lämnades oskadda. Genetiska tester bekräftade att när TRPM8 togs bort förlorade dessa läkemedel sin dödande effekt, och när TRPM8 ökades blev melanomcellerna ännu mer känsliga, vilket bevisar att effekten beror på denna specifika kanal. 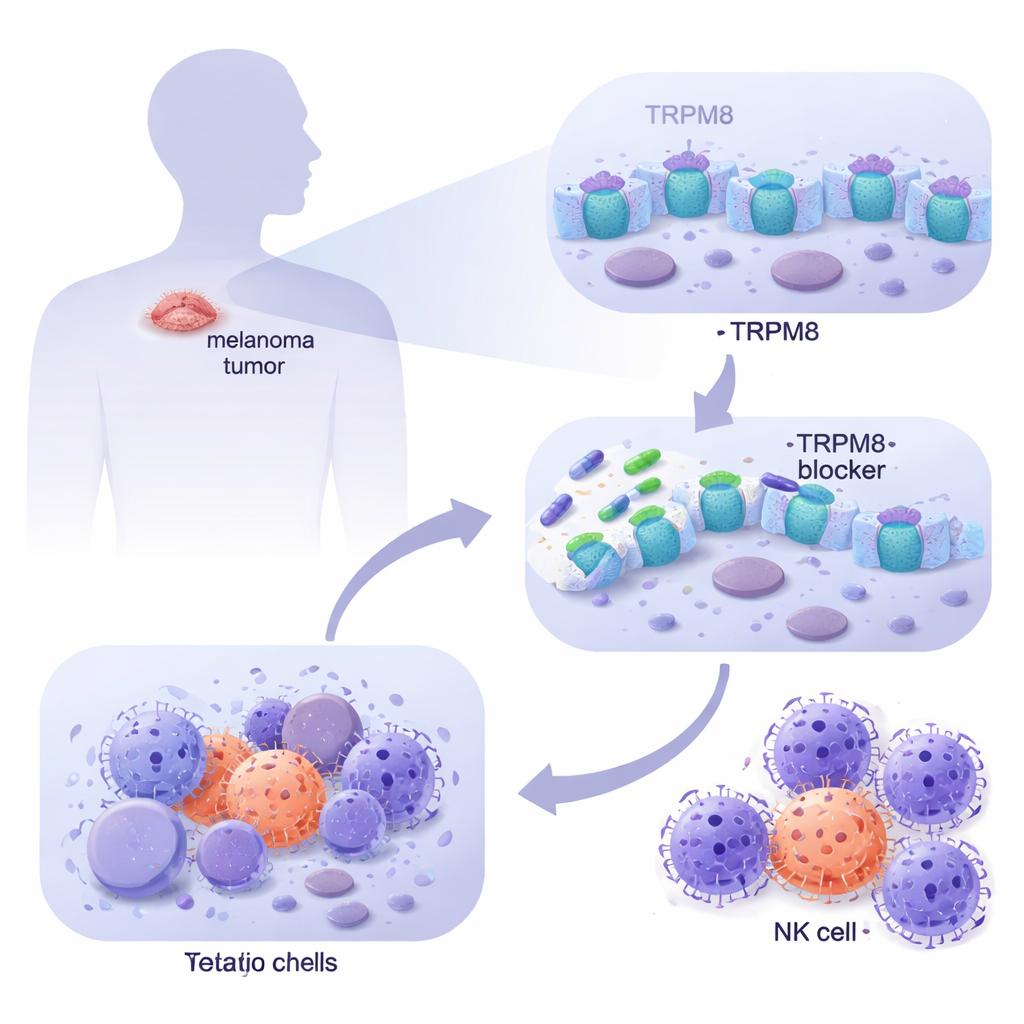
Att tvinga cancerceller in i en energikris
Till skillnad från klassiska TRPM8-aktivatorer som mentol, vilka driver ett kalciumflöde in i cellerna, utlöste dessa nya hämmare inga kalciumsignaler. Istället startade de en våg av oxidativ stress inne i melanomcellerna. Föreningarna ökade snabbt bildningen av reaktiva syreföreningar, särskilt i mitokondrierna, cellens energifabriker. Denna oxidativa stöt fick mitokondrierna att tappa sin elektriska potential, fragmentera och läcka ut cytokrom c, ett viktigt steg i att slå på cellens inre “självmords”program. Antioxidanter som tillfälligt neutraliserade dessa reaktiva molekyler räddade i stor utsträckning cellerna, vilket visar att redoxobalans inte är en sidoeffekt utan motorn bakom celldöden. Nedströms bekräftade klassiska dödsmarkörer, såsom aktivering av caspas-3 och klyvning av PARP, att cellerna genomgick programmerad apoptos snarare än ospecifikt skador.
Att avväpna överlevnadssignaler och väcka en väktare
Den oxidativa chocken satte igång ett bredare stressvar. Läkemedlen aktiverade ATM, en sensor för DNA-skada, och ledde till uppbyggnad och aktivering av p53, ett välkänt tumörsuppressorprotein som avgör om en skadad cell ska reparera sig eller dö. Samtidigt försvagade föreningarna en av melanomets huvudsakliga överlevnadsleder: PI3K–AKT-vägen. Normalt interagerar TRPM8 fysiskt med PI3K-komponenter för att hjälpa till att hålla AKT i sin aktiva, tillväxtfrämjande form. Efter behandling bröts detta partnerskap och AKT-aktiviteten sjönk, vilket ytterligare tippar balansen mot celldöd. Viktigt är att dessa förändringar var uttalade i melanomceller men inte i icke-cancerösa celler, vilket tyder på ett terapeutiskt fönster där tumören träffas hårt medan frisk vävnad skonas.
Att göra tumörer mer synliga för immuna “insatsstyrkor”
En del av melanomets fara ligger i dess förmåga att undkomma immunövervakning. Forskarna frågade därför vad som händer med tumörceller som överlever låga doser av TRPM8-hämmare under längre tid. De upptäckte att dessa kvarvarande celler började visa mer av en ytmärkning kallad ULBP1, som fungerar som en nödsignal igenkänd av NKG2D-receptorer på NK-celler. Andra relaterade signaler förändrades inte, vilket indikerar en selektiv effekt. I tredimensionella melanomsfärer som bättre efterliknar verkliga tumörer gjorde förbehandling med TRPM8-hämmare inte bara strukturerna mindre och ökade celldöd, utan gjorde dem också mycket mer sårbara för NK-cellernas angrepp. När ULBP1 eller NKG2D blockerades med antikroppar försvann denna ökade dödlighet i stor utsträckning, vilket visar att den förbättrade immunrensningen förmedlas av denna specifika kontakt mellan tumör och NK-celler. 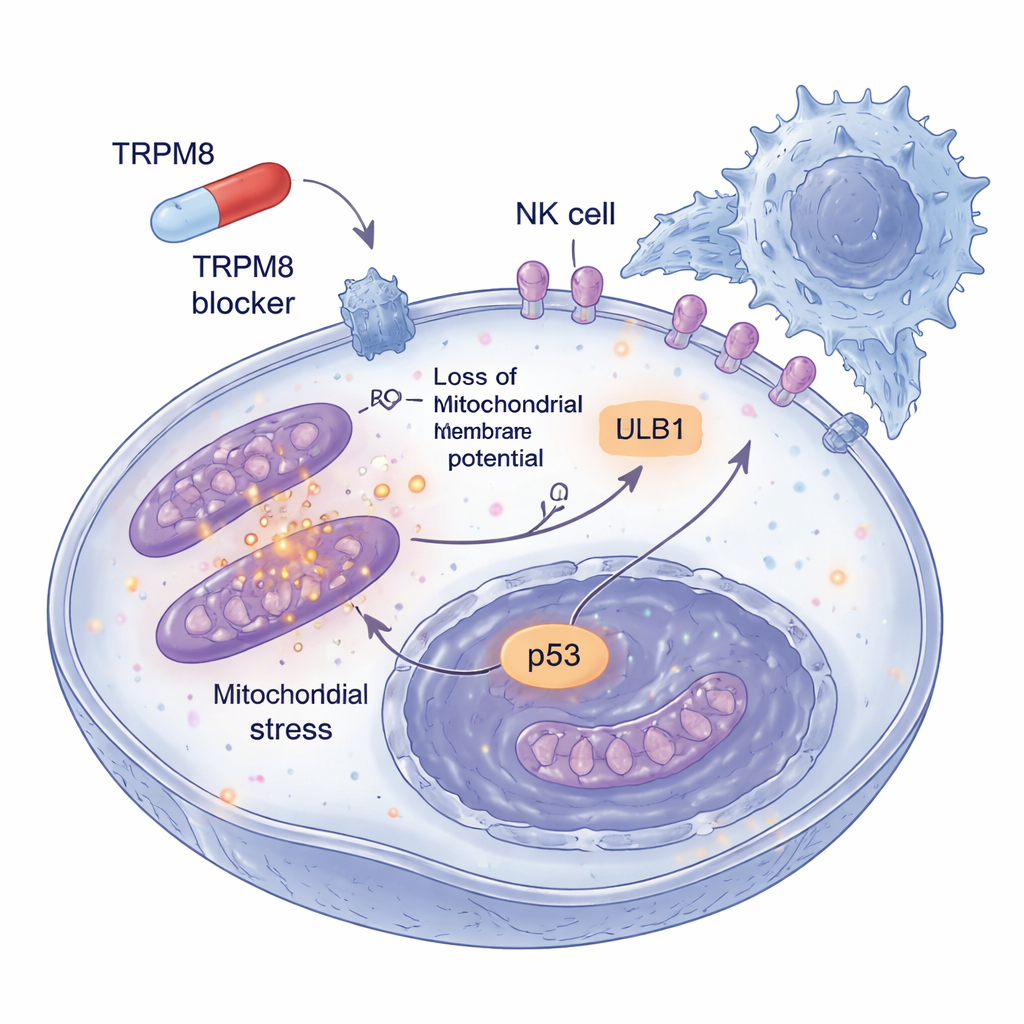
Vad detta kan innebära för framtida melanombehandling
Enkelt uttryckt förvandlar blockering av TRPM8 “kallsensorn” till en terapeutisk spak: den driver melanomceller in i en dödlig mitokondriell och DNA-relaterad kris samtidigt som den flaggar dem för destruktion av NK-celler. Eftersom läkemedlen skonar normala hudceller och inte skadar NK-cellerna själva, erbjuder de en lovande grund för nya behandlingar. Författarna föreslår att TRPM8-hämmare skulle kunna kombineras med befintliga immunoterapier för att attackera avancerat, läkemedelsresistent melanom på två fronter: genom att direkt döda tumörceller och genom att göra de överlevande lättare för immunsystemet att hitta och eliminera.
Citering: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
Nyckelord: melanom, TRPM8, mitokondrier, oxidativ stress, naturliga mördarceller