Clear Sky Science · sv
Laktayleringsdriven TRIM29 inducerar invasivt beteende och lymfnodmetastasering vid magsäckscancer via hnRNPA1‑medierad Wnt/β‑catenin‑signalering
Varför denna forskning är viktig
Magsäckscancer är en av världens mest dödliga cancerformer, till stor del eftersom den sprider sig tidigt till närliggande lymfkörtlar, vilket gör kirurgisk bot svår att uppnå. Denna studie avslöjar hur en kemisk förändring kopplad till tumörens ämnesomsättning överaktiverar ett protein kallat TRIM29, vilket hjälper cancerceller att invadera omgivande vävnad, bygga nya lymfkärl och stå emot cellgifter. Att förstå denna händelsekedja pekar mot nya sätt att bromsa eller blockera spridningen av magsäckscancer.
En farlig allians i magsårstumörer
Forskarna började med att jämföra prover från magsäckscancer med intilliggande frisk vävnad från 100 patienter, samt stora offentliga genbanker. De fann att TRIM29, ett protein som tidigare kopplats till immunreglering och andra cancerformer, konsekvent var högre i tumörceller. Patienter vars tumörer uppvisade högre TRIM29 hade större sannolikhet att ha cancer i lymf- och blodkärl och hade sämre total överlevnad. Dessa mönster tyder på att TRIM29 inte bara är närvarande utan aktivt bidrar till att göra magsäckscancer mer aggressiv.
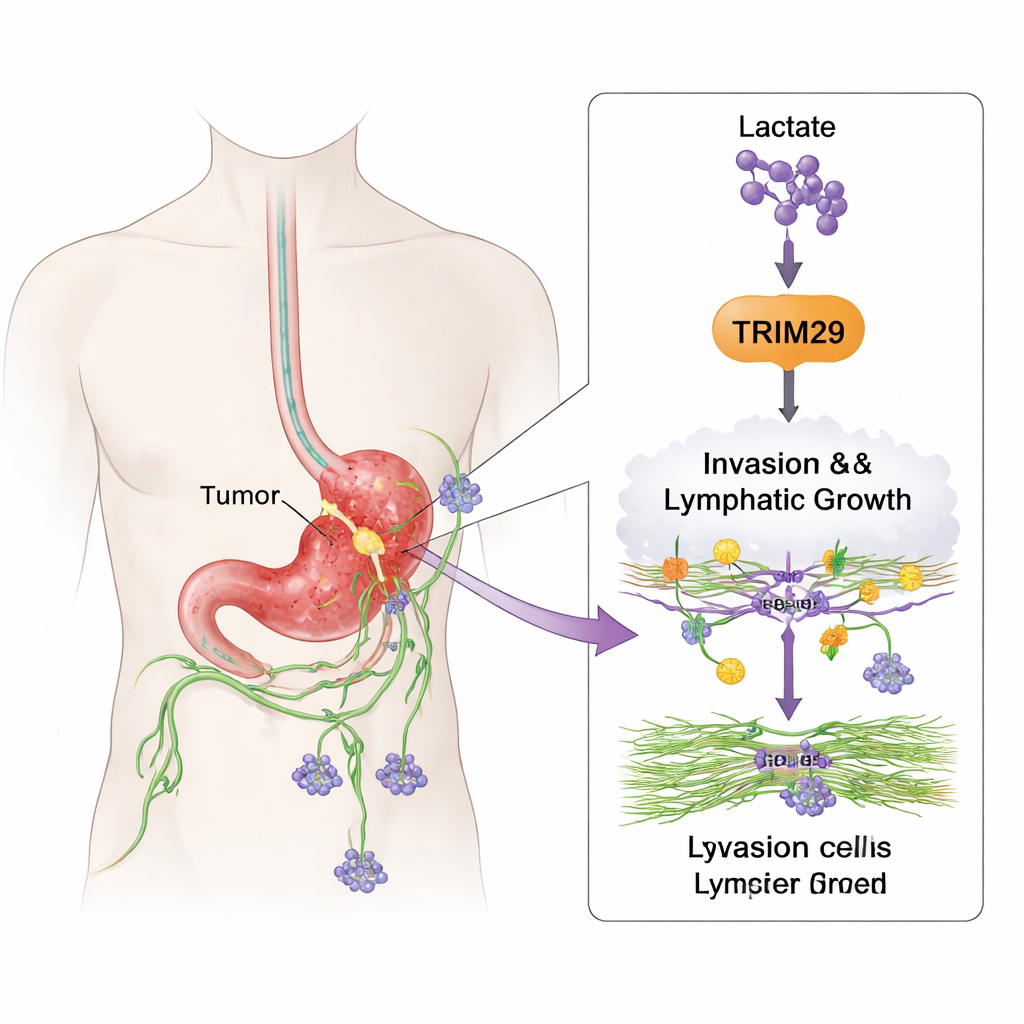
Hur cancerceller lär sig att förflytta sig
För att se vad TRIM29 faktiskt gör ändrade teamet dess nivåer i magsäckscellinjer. När de minskade TRIM29 blev cellerna märkbart mindre rörliga och mindre kapabla att tränga igenom tredimensionella geler som efterliknar kroppsvävnad. Att öka TRIM29 gav motsatt effekt och gjorde cellerna mer invasiva. Forskarna undersökte också lymfatiska endotelceller, de celler som bekläder lymfkärlen. TRIM29‑rika cancerceller uppmuntrade dessa kärlceller att spruta ut och bilda rörlika strukturer, ett tecken på ny lymfkärlsbildning (lymfangiogenes). I musmodeller gav tumörer med högt TRIM29 fler lever‑ och lymfnodmetastaser, medan tumörer med nedsatt TRIM29 spred sig mindre och bildade färre lymfkärl.
Molekylärt stafett: skyddar en nyckelregulator
Vid en djupare genomgång upptäckte forskarna att TRIM29 fysiskt binder till ett annat protein, hnRNPA1, som är känt för att påverka genbearbetning och kopplats till cancerns spridning. Normalt kan hnRNPA1 märkas för nedbrytning av ett annat protein, ett enzym kallat ZFP91, genom cellens avfallshanteringssystem. TRIM29 stör denna process genom att konkurrera med ZFP91 om bindningen till hnRNPA1. När TRIM29 är rikligt förekommande skyddar det hnRNPA1 från att märkas och brytas ned. Som ett resultat blir hnRNPA1 mer stabilt och ackumuleras i cancerceller, vilket sätter igång en kedja av signaler som slutligen aktiverar Wnt/β‑catenin‑vägen, en välkänd drivare av tumörtillväxt och migration. Detta ökar i sin tur produktionen av VEGF‑C, ett molekylärt signalämne som stimulerar ny lymfkärlsbildning och ger cancerceller fler ”vägar” att fly.
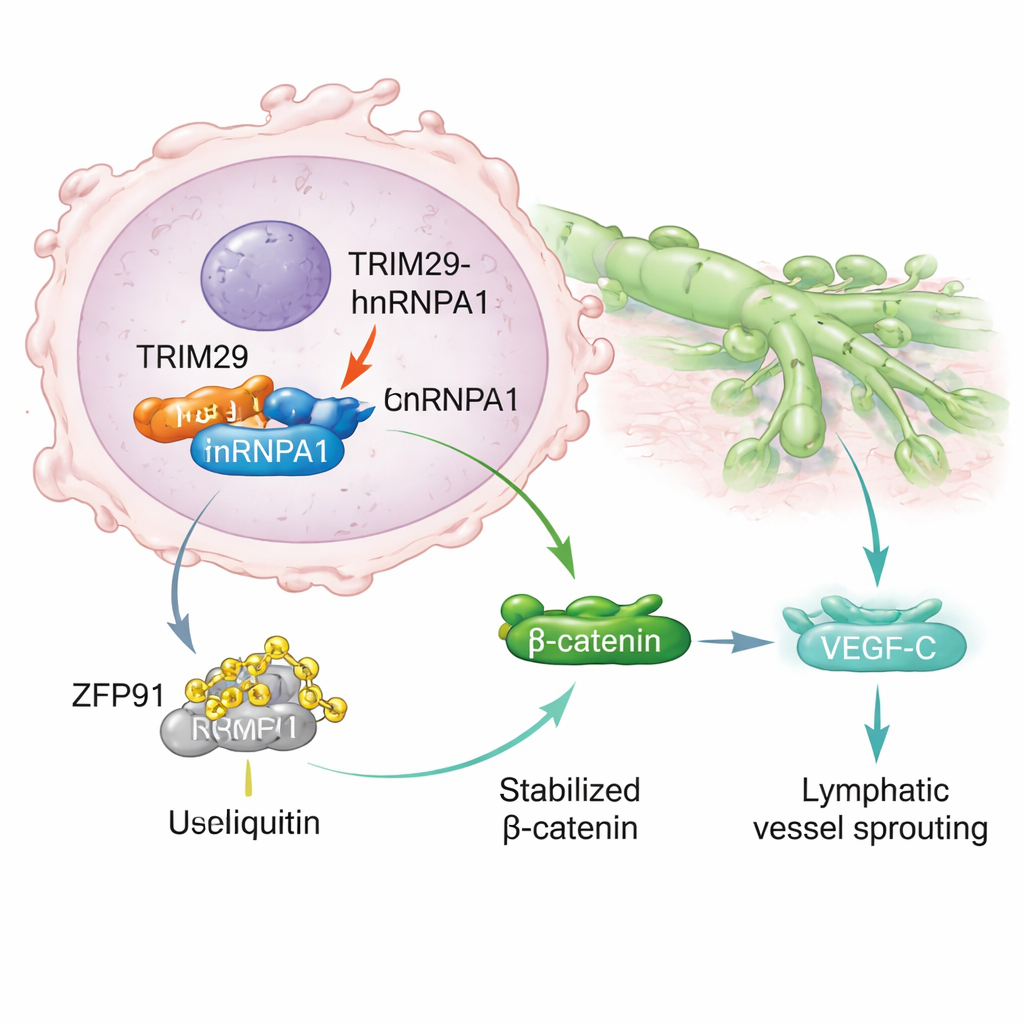
Att driva cancer med laktat
Studien kopplar också detta invasiva beteende till hur tumörer bearbetar socker. Snabbväxande tumörer förlitar sig ofta på en form av ämnesomsättning som producerar stora mängder laktat, en biprodukt som tidigare betraktats som skräp. Här visar författarna att laktat kan kemiskt modifiera histonproteiner som paketerar DNA, specifikt på en plats kallad H3K9. Denna ”laktaylering” fungerar som en på‑knapp för genen TRIM29 och ökar dess aktivitet. När de sänkte laktatproduktionen med metabola läkemedel föll TRIM29‑nivåerna; när de ökade laktat steg TRIM29. Magsäcksvävnader från patienter visade högre nivåer av H3K9‑laktaylering, vilket korrelerade med högre TRIM29, mer spridning till lymfkörtlar och sämre överlevnad. I praktiken hjälper tumörens förändrade ämnesomsättning till att skriva ett mer aggressivt genetiskt program.
Nya sätt att förbättra cellgiftsbehandling
Lymfkärl gör mer än att bära cancerceller; de kan också dränera cytostatika bort från tumörer. Med patient‑härledda tumörtransplantat odlade i möss testade forskarna om blockering av TRIM29 och lymfkärlsbildning kunde förbättra effekten av 5‑fluorouracil (5‑FU), ett standardläkemedel mot magsäckscancer. Hämning av TRIM29 eller blockering av lymfangiogenes gjorde vardera 5‑FU mer effektivt för att krympa tumörer och reducera celldelning. Kombinationen av båda strategierna gav starkast respons, vilket tyder på ett potentiellt sätt att övervinna vissa former av läkemedelsresistens vid avancerad sjukdom.
Vad detta betyder för patienter
Denne forskning målar upp en steg‑för‑steg‑bild: magskörtumörer producerar överskott av laktat, vilket slår på TRIM29; TRIM29 skyddar därefter hnRNPA1, stabiliserar en tillväxtsignal och ökar lymfkärlsbildning och spridning till lymfkörtlar. Kliniskt identifierar höga TRIM29‑nivåer och relaterade laktayleringsmarkörer patienter med högre risk för aggressiv sjukdom. Framöver kan läkemedel som dämpar laktatsignalering, blockerar TRIM29 eller förhindrar lymfkärlsbildning kombineras med befintlig kemoterapi för att hindra spridning av magsäckscancer och förbättra behandlingseffekten.
Citering: Hua, R., Yu, J., Niu, Y. et al. Lactylation-drived TRIM29 induces invasive behavior and lymph node metastasis in gastric cancer via hnRNPA1-mediated Wnt/β-catenin pathway. Cell Death Dis 17, 222 (2026). https://doi.org/10.1038/s41419-026-08468-9
Nyckelord: metastasering vid magsäckscancer, TRIM29, laktat och laktaylering, lymfangiogenes, Wnt beta‑catenin‑väg