Clear Sky Science · sv
Selenometionin som en dubbelverkande ferroptoshämmare: selenförsörjningsdriven GPX4-biosyntes bortom transsulfuration och reduktionskapacitetsmedierad ROS-avskiljning oberoende av GPX4-aktivitet
Varför det är viktigt att skydda våra celler mot ett ”rost-liknande” dödsfall
Celler i vår kropp kan dö på många sätt, och en av de nyaste och mest intressanta är kallad ferroptos — en typ av järndriven, ”rost-lik” skada på cellmembran. Denna process kopplas nu till sjukdomar från njurskador till neurodegeneration. Spårämnet selen, som många känner igen från kosttillskott, visar sig spela en avgörande roll för att stoppa denna farliga form av celldöd. Denna studie undersöker hur en vanlig seleninnehållande aminosyra, selenometionin, kan skydda celler från ferroptos genom inte bara en utan två skilda skyddsstrategier.
En ny försvarare hittad i en omfattande läkemedelssökning
För att hitta små molekyler som kan blockera ferroptos screenade forskarna tusentals föreningar från FDA-godkända läkemedel och naturprodukter. De använde en kemikalie kallad RSL3 för att utlösa ferroptos i mänskliga cancercellinjer och övervakade sedan celldöd och uppbyggnad av skadade, oxiderade fetter i cellmembranen. Bland alla kandidater framträdde selenometionin som en stark skyddare: det minskade både lipidoxidation och celldöd över olika celltyper och i två huvudsakliga ferroptosmodeller — en driven av direkt GPX4-hämning (med RSL3) och en annan genom att beröva cellerna cystin, en byggsten för antioxidanten glutathion. Dessa resultat placerade selenometionin som en bred och robust ferroptoshämmare. 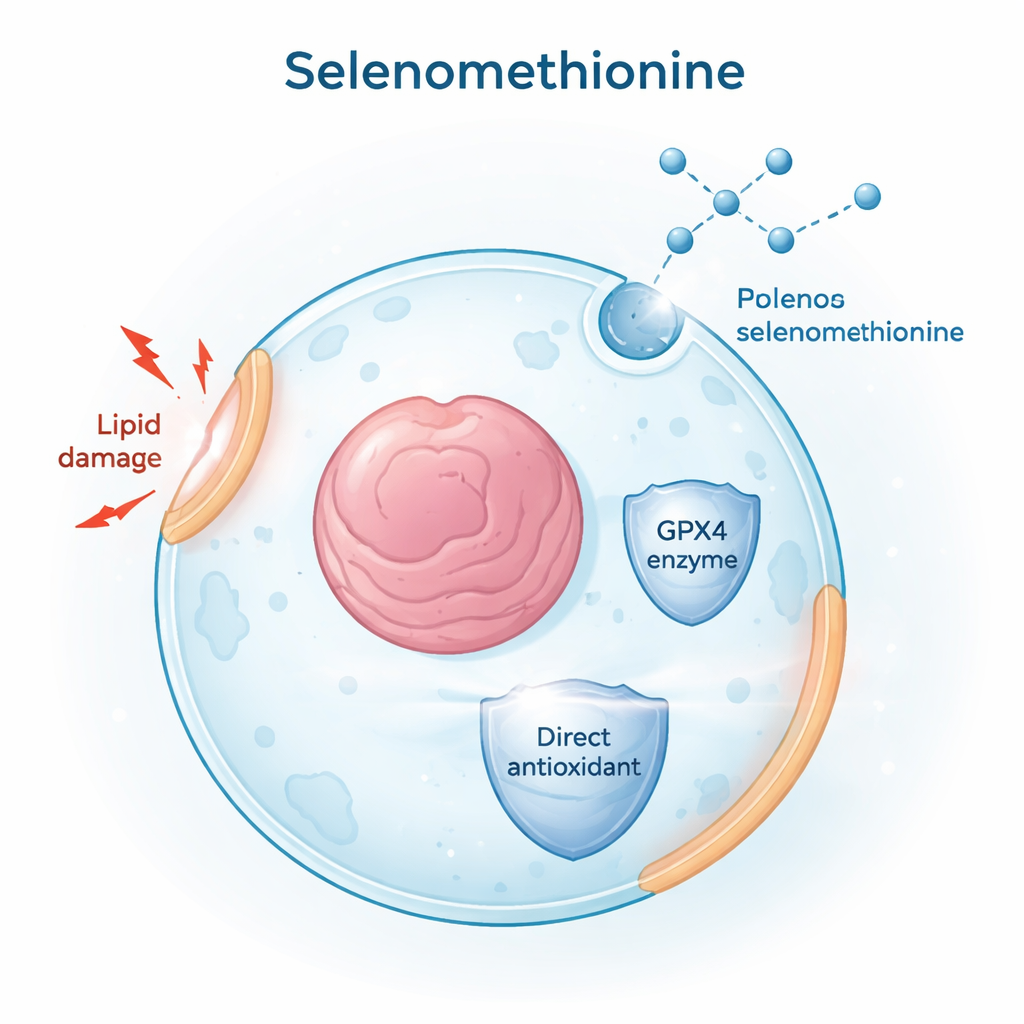
Selenleverans för ett centralt skyddande enzym
En kärna i cellernas anti-ferroptosskydd är ett enzym kallat GPX4, som är beroende av selen för att fungera. Teamet ville ta reda på om selenometionin bara matar in i denna väg eller gör mer än så. De spårade hur selen från selenometionin kan omvandlas till former lämpliga för att bygga GPX4, även när en vanlig väg, kallad transsulfationsvägen, var nedsatt eller blockerad. Genom att använda genetiska nedregleringar och kemiska hämmare av enzymer i dessa svavel–selen-vägar fann de att selenometionin ändå ökade GPX4-nivåerna och skyddade celler. Detta visade att celler kan utnyttja flera metaboliska rutter för att utvinna selen från selenometionin och upprätthålla GPX4-produktion, även i vävnader där den klassiska vägen är svag.
Skydd som inte beror på det vanliga enzymet
Överraskande nog, när forskarna helt avlägsnade GPX4 från celler med CRISPR-genredigering, fortsatte selenometionin att skydda mot ferroptos. Det minskade fortfarande membranlipidskada och celldöd, vilket tyder på att GPX4 inte är hela förklaringen. Ytterligare experiment antydde att en del av detta skydd involverar att selenometionin byggs in i nyproducerade proteiner, men att detta bara är en del av effekten. Författarna inriktade sig sedan på selenometionins kemiska reaktivitet. De fann att det kan neutralisera reaktiva syreradikaler (ROS) direkt, inklusive väteperoxid, och omvandlas till en oxiderad ”sulfoxid”-form. Masspektrometri bekräftade denna produkt, och att tillföra celler sulfoxidversionen minskade också ferroptos, vilket antyder att celler kan återcirkulera den tillbaka till aktiv selenometionin i en redoxcykel.
Från cellodling till att skydda njurar i levande djur
För att testa om dessa mekanismer spelar roll i en hel organism vände sig teamet till en musemodell för akut njurskada orsakad av cancerläkemedlet cisplatin, ett tillstånd som är känt för att involvera ferroptos. Möss som behandlades med cisplatin visade viktnedgång, svullna njurar, nedsatt njurfunktion och höga nivåer av ferroptosmarkörer. När djuren fick selenometionin förbättrades många av dessa problem: kroppsvikten återhämtade sig, njursvullnad minskade, blodvärden för njurfunktion normaliserades, inflammationssignaler sjönk och kemiska markörer för lipidoxidation minskade. Njurevävnad visade också högre GPX4-nivåer och färre strukturella skador. Dessa fördelar var jämförbara med dem som observerades med ferrostatin-1, en välkänd experimentell ferroptoshämmare. 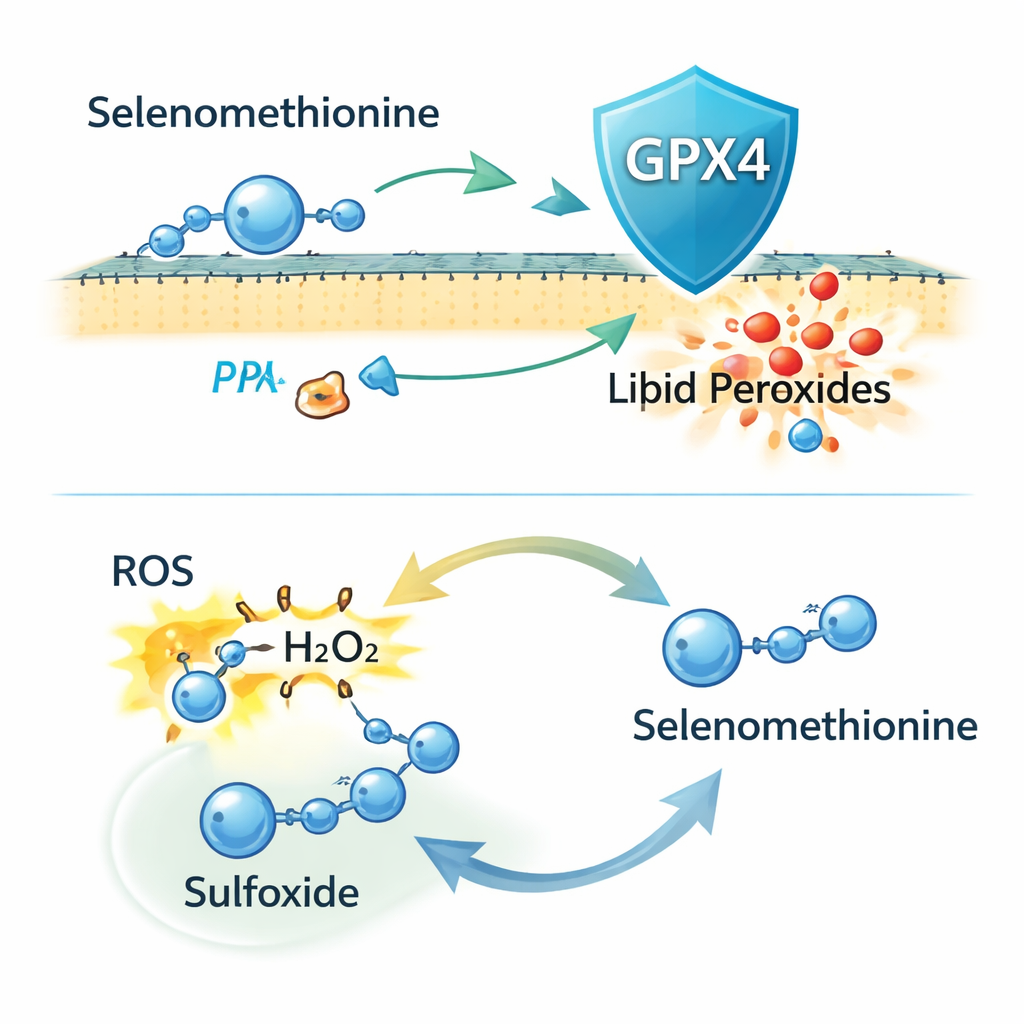
Vad detta betyder för framtida terapier
I vardagliga termer tyder detta arbete på att selenometionin fungerar som en tvåsyftig brandsläckare mot ett järndrivet ”rostande” av cellmembran. Å ena sidan tillför det selen så att celler kan bygga mer av enzymet GPX4, som agerar som ett internt städpatrull för skadade fetter. Å andra sidan kan selenometionin själv binda upp skadliga oxidanter och återcirkuleras, vilket erbjuder ett GPX4-oberoende backuppskydd. Tillsammans gör dessa egenskaper selenometionin till en lovande kandidat för att förebygga eller behandla sjukdomar där ferroptos spelar en central roll, såsom läkemedelsinducerad njurskada och potentiellt andra tillstånd som drivs av okontrollerad oxidativ stress.
Citering: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
Nyckelord: ferroptos, selen, selenomethionin, oxidativ stress, akut njurskada