Clear Sky Science · sv
Chaperonin TRiC-komponenten Cct3 krävs för axonal transport, myelinisering och förfining av neuromuskulära kopplingar
När nervkopplingar går fel
Våra hjärnor och kroppar förlitar sig på långa, kabel-liknande nervfibrer för att snabbt och pålitligt föra signaler. För att klara detta är många nerver omslutna av isolerande myelin, och deras ändar måste bilda precisa kontakter med muskler. Denna artikel utforskar vad som händer när en viktig cellulär ”hjälpare” för proteinfällning, kallad Cct3, sviktar. Med zebrafisk och mänsklig vävnad visar författarna hur just denna komponent i en stor chaperonmaskin kan rubba myelin, nerv–muskel-kontakter och det interna transportsystem som håller nervceller vid liv och fungerande.
En cellulär skräddare för nervbygge
Inuti varje cell måste nyproducerade proteiner veckas till rätt former, ungefär som att noggrant skräddarsy en kostym. TRiC-komplexet, som inkluderar subenheten Cct3, är en av de stora ”skräddarna” och hjälper omkring 10 % av alla cellulära proteiner—särskilt de strukturella proteinerna aktin och tubulin—att veckas korrekt. Dessa byggstenar utgör cellens inre skelett och de spår längs vilka viktig last förflyttas. Hos patienter med felaktiga varianter av CCT3 och närliggande gener visar hjärnavbildningar minskad vit substans (hjärnans myelinrika ledningsbanor) samt problem i perifera nerver och muskler. Författarna ville förstå hur förlust av Cct3 spårar ur nervutveckling och funktion.
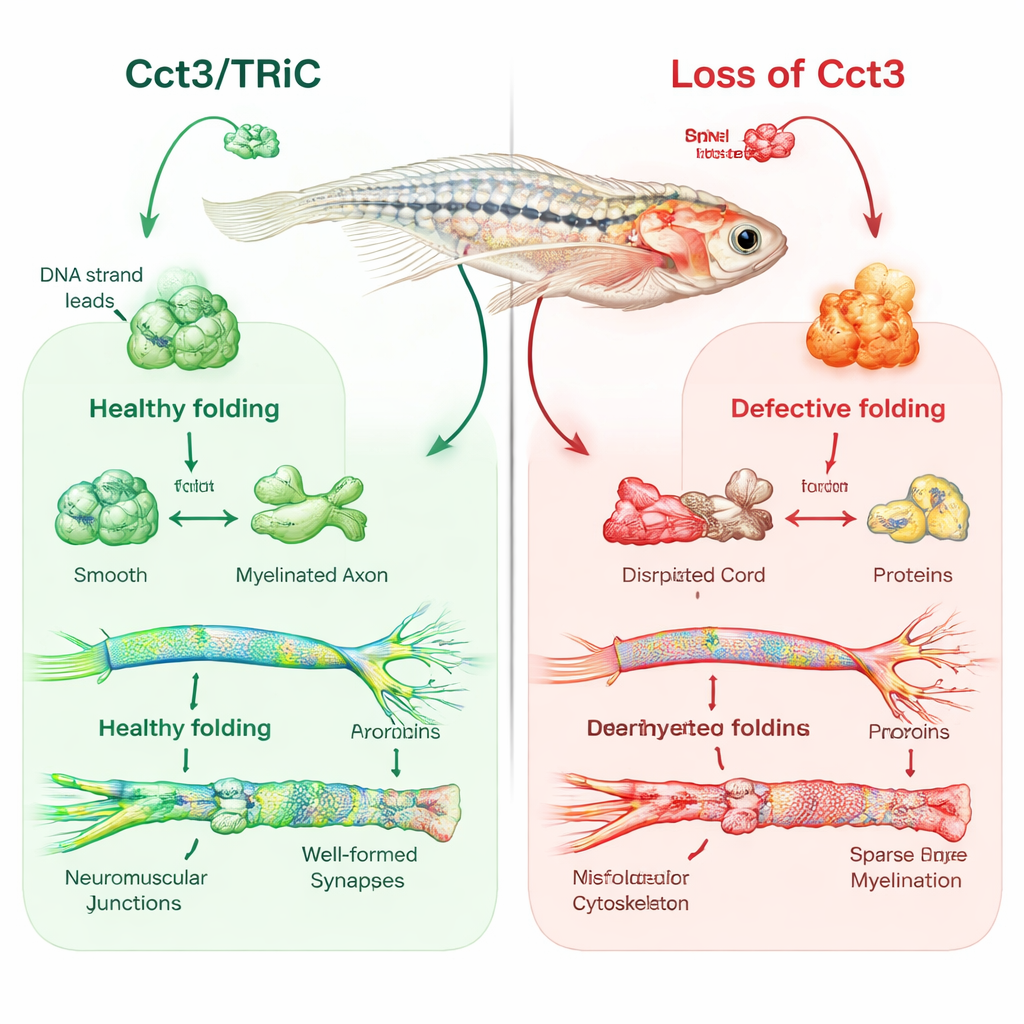
Zebrabas som fönster mot nervisolering
Forskarna använde CRISPR/Cas9-genredigering för att skapa zebrababar som saknar funktionellt cct3. Dessa små fiskar visade mindre hjärnor och ögon, vätskeansamling runt hjärtat, svaga beröringsresponser och dog inom några dagar. När forskarna återställde normalt cct3 genom att injicera dess budbärar-RNA förbättrades många av dessa defekter, vilket bekräftade att förlust av Cct3 var grundorsaken. Med fokus på myelin använde de fluorescerande markörer och elektronmikroskopi för att visualisera de isolerande lagren runt nerver. I normala fiskar omslöt myelinbildande celler i hjärnan och perifera nerver axoner med prydliga, lager på lager-höljen vid dag fyra i utvecklingen. I kontrast hade cct3-mutanter betydligt färre myelinbildande celler och i praktiken ingen korrekt myelin runt många axoner, trots att dessa axoner på ytan såg normalt formade ut.
Sköra stödjeceller och ansträngda nerv–muskel-kopplingar
För att ta reda på varför myelinet saknades undersökte författarna Schwann-celler och närliggande neural crest-celler—stödjecellerna som omsluter perifera nerver. I normala fiskar utvecklade dessa celler långa, smala utskott och förfinade sedan sin form när de bildade myelinsegment. Hos mutanter blev de rundade, förkortade sina utskott och fragmenterade. Deras cellkärnor bröts sönder i ett mönster typiskt för programmerad celldöd, och en viktig dödsmarkör (aktiverat Caspase 3) framträdde, vilket visar att många av dessa celler dog tidigt. Samtidigt vid de neuromuskulära kontaktytorna där nerver möter muskel, misslyckades mönstret av receptorchocker på musklerna att förfinas. Istället för många små, precisa kluster hade mutanterna färre, större plack av receptorer, vilket speglar de förenklade synaptiska veck som sågs hos en mänsklig patient med en CCT3-mutation.
Brutna inre spår och försenad lasttrafik
Eftersom TRiC hjälper till att veckla aktin och tubulin undersökte författarna noggrant motoraxonens inre ramverk. De fann att de totala nivåerna av tubulin var kraftigt reducerade hos mutanter, och antalet normala mikrotubuli—de ihåliga rören som fungerar som transportspår—minskade dramatiskt i både centrala och perifera nerver. Kemiska ”märken” på tubulin som är viktiga för stabila, transportredo mikrotubuli var också allvarligt förändrade. Med hjälp av liveavbildning av lysande mitokondrier och endosomer inne i motoraxonerna såg de hur dessa laster rörde sig. I friska fiskar färdades organeller snabbt och riktat längs axonet. Hos mutanter stannade många organeller upp eller vaggade fram och tillbaka, vilket stämmer överens med skadade spår och störd transport.
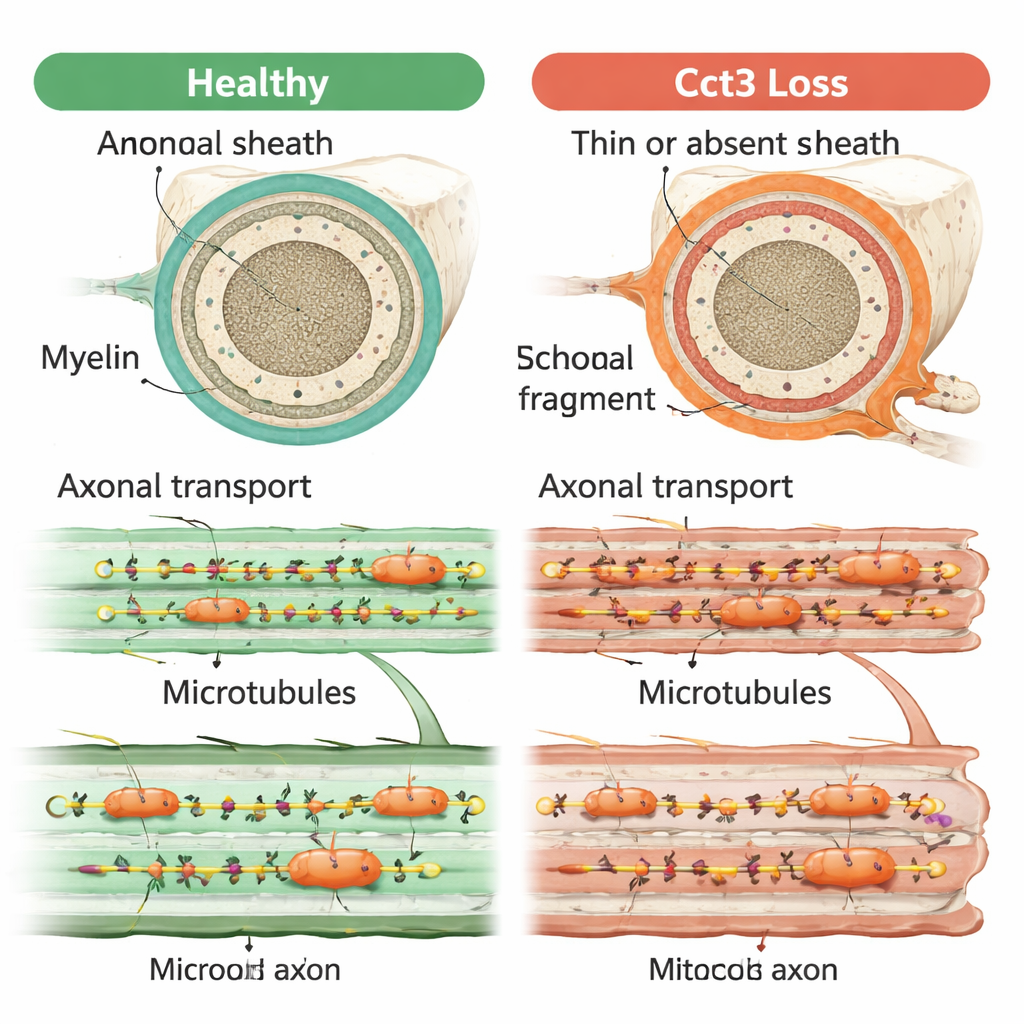
En grundläggande orsak bakom många symtom
Sammantaget visar fynden att Cct3 är avgörande för flera sammanlänkade aspekter av nervhälsa: det stöder överlevnad av myelinbildande stödjeceller, möjliggör korrekt myelinomslutning och tillåter mognande neuromuskulära kopplingar att förfinas. Alla dessa roller kan spåras tillbaka till dess uppgift i att veckla och upprätthålla de proteiner som bygger cytoskelettet och mikrotubulspåren som används för axonal transport. När dessa spår fallerar kan viktiga signaler och material inte nå rätt platser längs nerven, vilket sannolikt underminerar både kommunikationen med myelinbildande celler och formningen av nerv–muskel-kontakter. Detta arbete tyder på att försämrad axonal transport kan vara den gemensamma tråden som länkar ihop de skiftande hjärn- och nervproblemen som ses vid TRiC-relaterade sjukdomar.
Citering: Zhang, X., Zajt, K.K., Palaz, T. et al. The chaperonin TRiC component Cct3 is required for axonal transport, myelination, and neuromuscular junction refinement. Cell Death Dis 17, 221 (2026). https://doi.org/10.1038/s41419-026-08465-y
Nyckelord: myelinisering, axonal transport, neuromuskulär koppling, molekylära chaperoner, zebrabasmodell