Clear Sky Science · sv
Försämrad BDNF–TrkB‑trafik och signalering i basala framhjärnans neuroner vid Downs syndrom
Varför denna hjärnstudie är viktig
Personer med Downs syndrom lever längre än tidigare, men de har också mycket hög risk att utveckla en demens som liknar Alzheimers i medelåldern. Denna studie undersöker enskilda hjärnceller på djupet för att förstå varför vissa neuroner är särskilt sårbara. Genom att spåra hur dessa celler transporterar och svarar på en viktig ”hjärngödsel”‑molekyl avslöjar forskarna ett trafikstockningsliknande tillstånd inne i neuronerna som kan förklara minnesförlust och peka mot nya behandlingsstrategier.
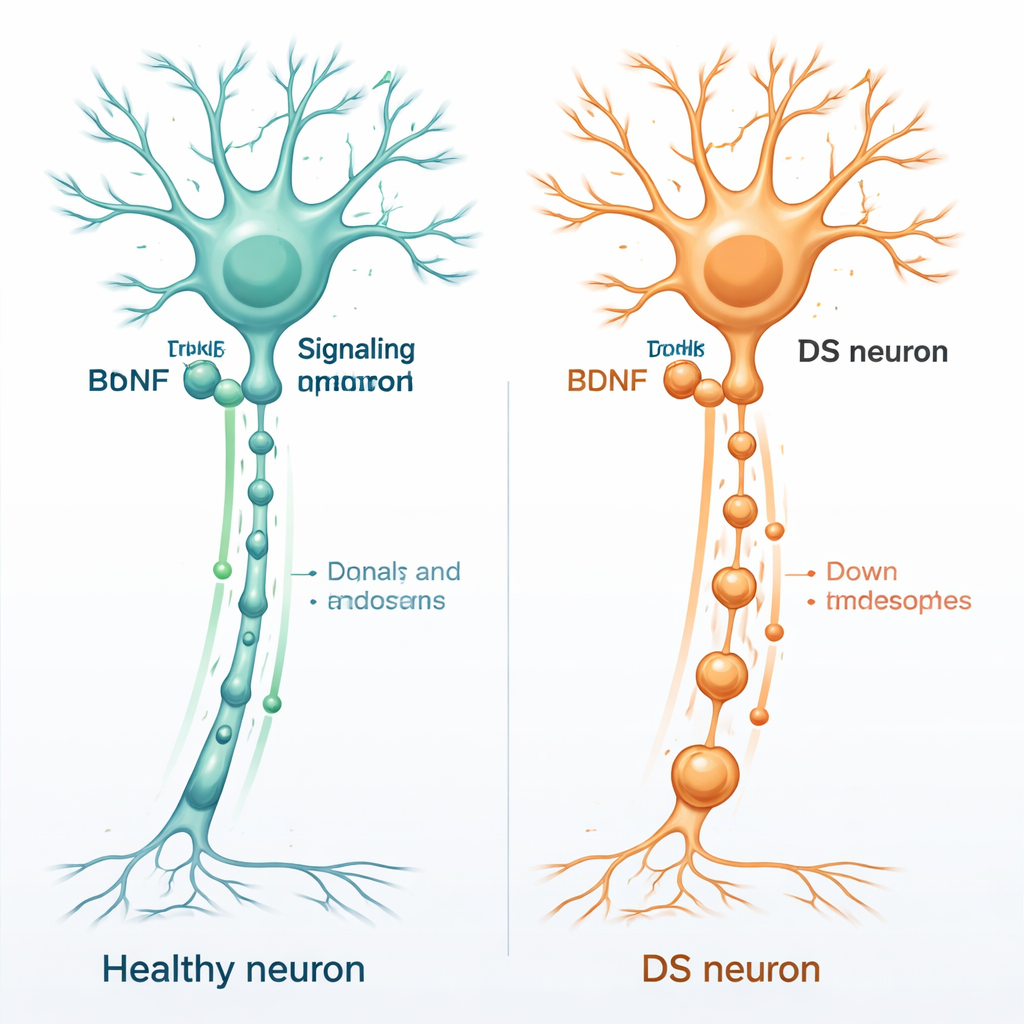
Hjärngödsel och nervcellers hälsa
Sunda hjärnceller är beroende av stödjande molekyler kallade neurotrofiner, som fungerar som gödsel för neuroner. En av de viktigaste är brain‑derived neurotrophic factor, eller BDNF. BDNF binder till ett dockningsprotein på neuroner kallat TrkB, vanligtvis i ändarna av nervfibrerna. När BDNF fäster dras hela BDNF–TrkB‑komplexet in i små membranblåsor och transporteras tillbaka längs den långa nervfibern till cellkroppen. Dessa rörliga blåsor, kända som signalendosomer, berättar för kärnan vilka gener som ska aktiveras för att hålla neuronen vid liv, ansluten och anpassningsbar.
När cellulära fraktbehållare blir för stora
Teamet fokuserade på basala framhjärnans neuroner, en cellgrupp som starkt stöder minne och uppmärksamhet och som är bland de första att försämras både vid Downs syndrom och Alzheimers sjukdom. Med en musmodell för Downs syndrom kallad Dp1Tyb färgade de neuroner för en markör för tidiga endosomer och jämförde med normala neuroner. Neuroner från Downs syndrom innehöll betydligt fler tidiga endosomer som var mer än 50 procent större än normalt. Dessa strukturer regleras av Rab5, en molekylär brytpunkt som hjälper till att bilda och sortera dessa interna ”fraktbehållare”. Forskarna fann att Rab5 satt fast i ett överaktivt tillstånd i Downs‑neuroner, redan innan BDNF‑stimulering, vilket tyder på att endosomsystemet redan kördes på högvarv.
Trafikstockningar längs nervfibern
Nästa fråga var om detta förvrängda interna landskap störde rörelsen av BDNF‑signaler. De odlade neuroner i mikrofluidiska enheter som skiljer cellkropparna från axonterminalerna, vilket gjorde det möjligt att stimulera endast axonspetsarna. Genom att följa ofarliga fluorescerande spårämnen som använder samma transportväg som BDNF–TrkB‑komplex mätte de hur snabbt signalendosomerna färdades tillbaka mot cellkropparna. I normala neuroner gjorde tillsats av BDNF att endosomerna rörde sig ungefär 30 procent snabbare och pausade mindre, vilket speglade ett robust svar på tillväxtsignaler. I neuroner från Downs syndrom lyckades däremot inte BDNF att öka hastigheten eller minska pauserna. Ett separat experiment som spårade faktiska TrkB‑receptorer bekräftade att färre av dem nådde cellkroppen framgångsrikt i Downs‑celler.
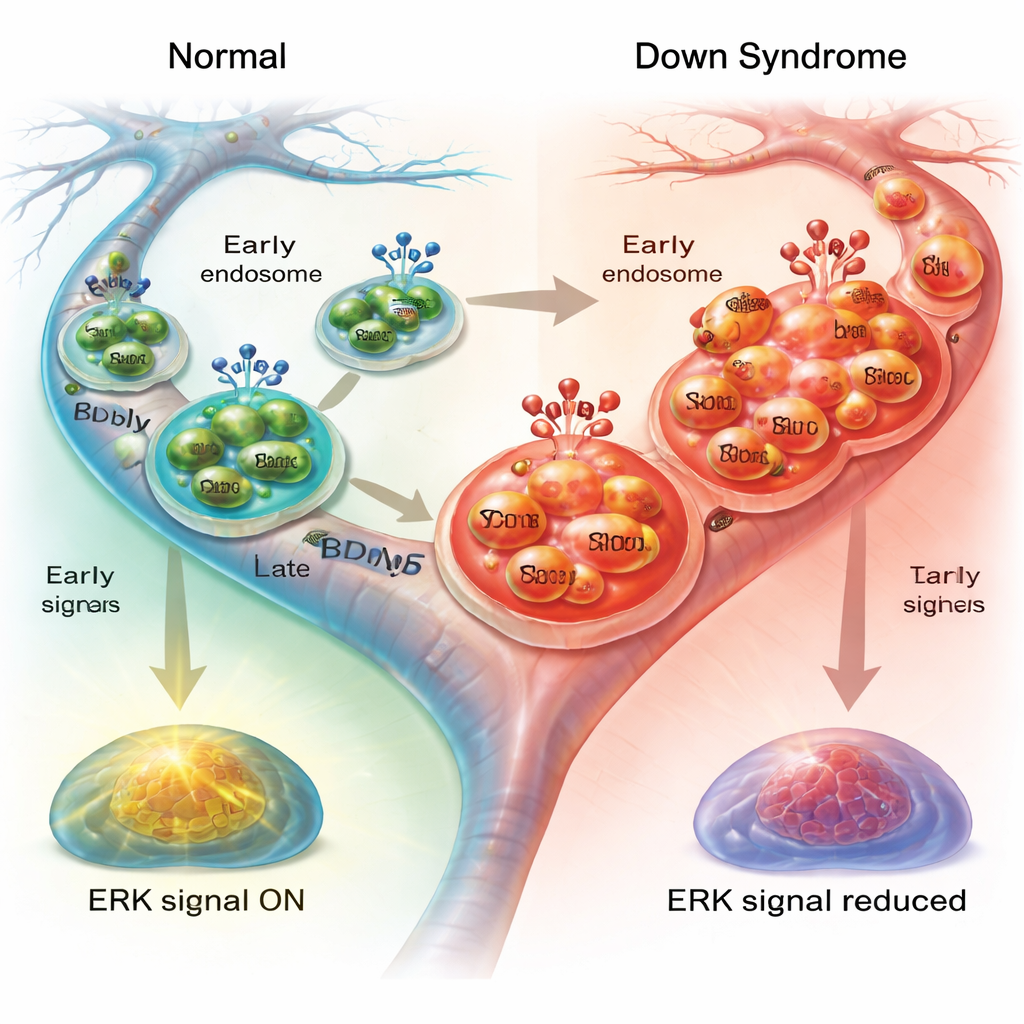
Dämpade nedströmsignaler inne i cellen
För att dessa transportblåsor ska stödja neuronens hälsa måste de aktivera interna signalvägar när de når sin destination. En nyckelväg involverar ERK1/2, ett par enzymer som för vidare BDNF:s budskap till kärnan och hjälper reglera cellens skelett och transportmaskineri. När forskarna mätte aktiverat ERK1/2 efter BDNF‑behandling såg de en tydlig ökning i normala neuroner men ett mycket svagare svar i Downs‑neuroner, särskilt i axonerna. Blockering av ERK1/2 i friska neuroner reproducerade delvis den slöa transporten som sågs i Downs‑celler, genom att sakta ner endosomerna och öka deras pauser. Däremot hade ERK1/2‑blockaden liten ytterligare effekt i Downs‑neuroner, vilket stämmer med en redan nedtonad signalering.
Vad detta betyder för hjärnans åldrande vid Downs syndrom
Tillsammans tyder fynden på ett självförstärkande problem i sårbara neuroner: Rab5 är överaktivt, tidiga endosomer sväller och BDNF–TrkB‑komplex fastnar i kompartment som inte rör sig effektivt. Som en följd når färre tillväxtsignaler cellkroppen, ERK1/2‑signalering försvagas och maskineriet som driver långtids‑transporten försämras ytterligare. Över år kan detta defekta kommunikationssystem bidra till den tidiga och allvarliga förlusten av basala framhjärnans neuroner som ses vid Downs‑relaterad Alzheimers sjukdom. Genom att belysa kopplingen mellan endosomal ”trafikstyrning” och tillväxtfaktorsignalering pekar studien mot nya terapeutiska idéer som syftar till att normalisera Rab5‑aktivitet, återställa endosomfunktion och stärka BDNF‑svar för att skydda dessa kritiska neuroner.
Citering: Blackburn, E., Birsa, N., Lopes, A.T. et al. Impaired BDNF-TrkB trafficking and signalling in Down syndrome basal forebrain neurons. Cell Death Dis 17, 214 (2026). https://doi.org/10.1038/s41419-026-08464-z
Nyckelord: Downs syndrom, Alzheimers sjukdom, BDNF, axonal transport, endosomer