Clear Sky Science · sv
PDHA1–acetyleringssignalering dämpar kuproptos för att minska anti-androgeneffekt vid prostatacancer
Varför denna forskning är viktig
Prostatacancer är en av de vanligaste cancerformerna hos män, och många avancerade fall behandlas med läkemedel som släcker manliga hormon‑signaler. Ett viktigt läkemedel, enzalutamid, fungerar ofta i början men slutar sedan vara effektivt när tumörer utvecklar resistens. Denna studie avslöjar en överraskande anledning till varför vissa prostatacancerformer undviker enzalutamids effekter och visar hur blockering av en enda metabolisk väg kan återkänsliggöra tumörer, vilket öppnar för mer varaktiga behandlingar.
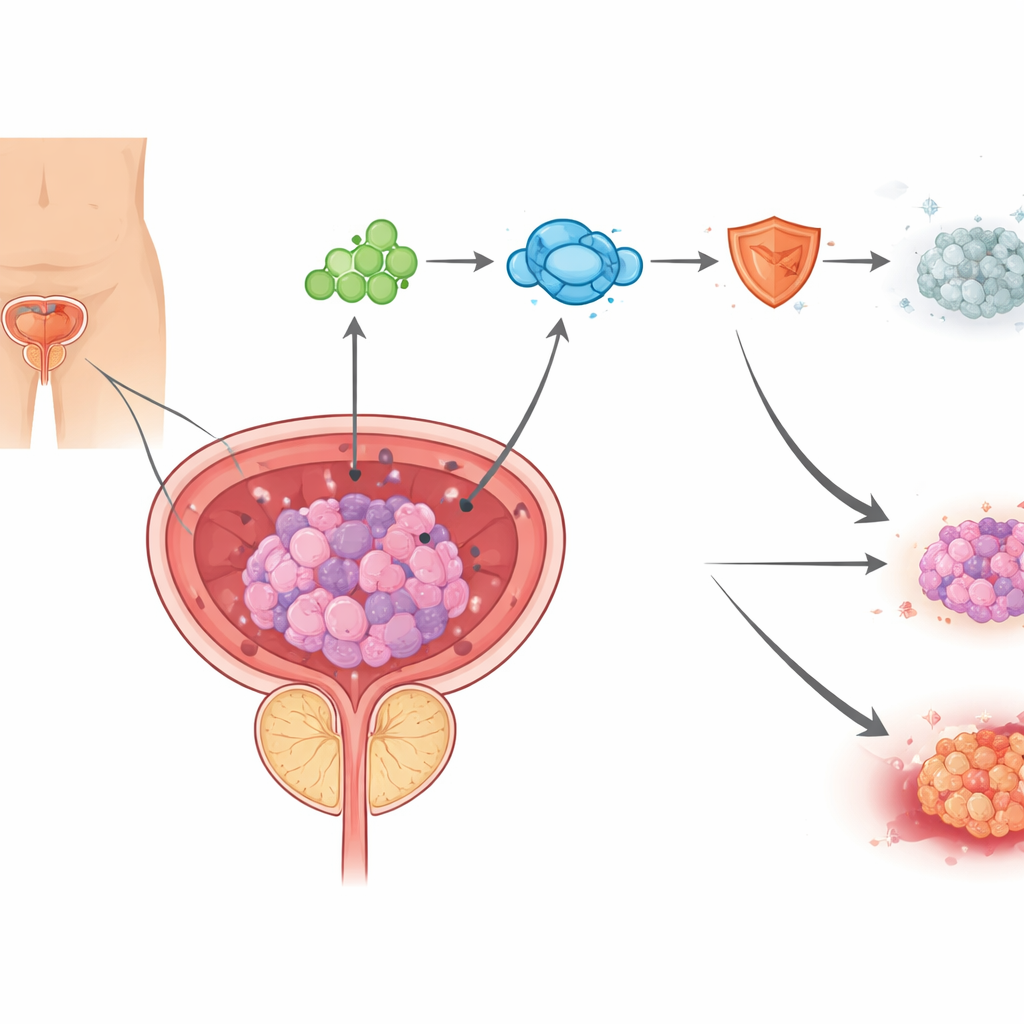
En ny form av celldöd driven av koppar
Cellers död kan ske på många olika sätt, och modern cancerforskning försöker i allt högre grad återaktivera dessa naturliga dödsprogram i tumörceller. Författarna fokuserar på en nyligen beskriven form av celldöd kallad kuproptos, som utlöses när koppar ansamlas i mitokondrierna, cellens kraftverk. I prostatacancerprover från patienter som fått androgen‑blockerande läkemedel fann teamet tecken på kopparansamling och mitokondrieskada, tillsammans med proteinförändringar som är kännetecken för kuproptos. I cellkulturer ökade enzalutamid kopparnivåerna och skadade mitokondrierna, och en kopparbindande förening kunde till stor del rädda cellerna, vilket visar att enzalutamid delvis kan döda prostatacancerceller genom att driva dem mot kopparstyrd celldöd.
Hur tumörer bedövar kopparns giftiga slag
Dock ger sig inte alla cancerceller. Genom att gräva i flera dataset av enzalutamidresistenta prostatatumörer och fokusera på gener kopplade till kuproptos identifierade forskarna ett framträdande protein: PDHA1, en central del i maskineriet som omvandlar socker‑baserat bränsle till acetyl‑CoA, en viktig byggsten i cellen. PDHA1‑nivåerna var högre i resistenta tumörer, kopplade till sämre överlevnad och mer aggressiv sjukdom, och ökade av enzalutamid självt. I labbexperiment gjorde nedreglering av PDHA1 cancerceller mycket känsligare för både enzalutamid och ett direkt kuproptos‑inducerande läkemedel, medan ökad PDHA1 gjorde dem svårare att döda. I möss krympte tumörer med reducerad PDHA1 mycket mer under enzalutamidbehandling, vilket bekräftar att detta enzym hjälper tumörer att stå emot terapi i levande organismer.
En metabolisk och epigenetisk sköld mot behandling
Teamet redde sedan ut hur PDHA1 bygger denna sköld. Eftersom PDHA1 matar in i acetyl‑CoA‑produktionen testade de om det kunde förändra hur DNA paketeras och läses. När PDHA1 var hög steg acetyl‑CoA‑nivåerna och kemiska ”acetyl”‑märken på histonproteinerna, särskilt på en markör som är associerad med aktiva gener. En viktig mottagare var SLC7A11, en transportör som för cystein in i celler för att göra glutathion, en stor antioxidant. Med mer PDHA1 producerade cellerna mer glutathion; med mindre PDHA1 sjönk cystein och glutathion. Glutathion band i sin tur koppar och neutraliserade det, vilket minskade den stress som utlöser kuproptos. Återställande av glutathion eller SLC7A11 kunde upphäva den ökade kopparstressen som sågs när PDHA1 blockerades, vilket visar att en PDHA1–acetyl‑CoA–histon–SLC7A11–glutathion‑kedja låter cancerceller rena upp koppar och undvika död.
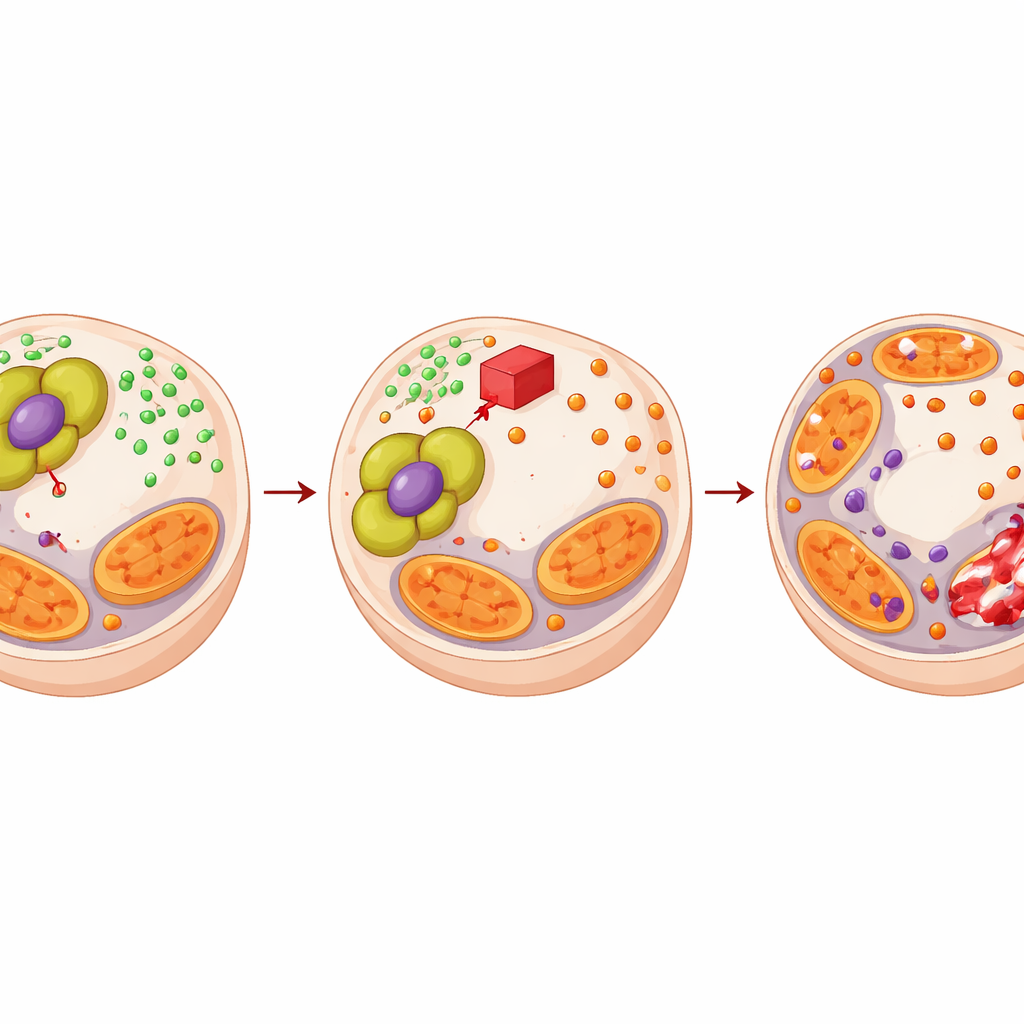
Att vända en sårbarhet till en terapeutisk strategi
Där PDHA1 hjälper tumörer att motstå enzalutamid genom att stärka detta kopparbuffrande system, frågade sig författarna om ett PDHA1‑riktat läkemedel kunde vända utvecklingen. De använde CPI‑613, en förening som stör samma metaboliska komplex. CPI‑613 ensam ökade kopparstressen och skadade mitokondriella proteiner i prostatacancerceller men skonsade normala prostataceller. I kombination med enzalutamid minskade CPI‑613 cancercellstillväxten mycket mer än någon av behandlingarna för sig, med matematisk analys som bekräftade verklig synergism. I mössmodeller och patient‑härledda tumörimplantat gav läkemedelsparet mindre tumörer, mer död vävnad, färre delande celler och starkare signaturer av koppardriven celldöd.
Vad detta betyder för patienter
Tillsammans visar dessa fynd att vissa prostatatumörer undviker enzalutamid genom att ominrikta sin metabolism för att generera mer acetyl‑CoA, skriva om genaktivitet och öka glutathion, vilket sugs upp giftigt koppar och blockerar kuproptos. Genom att hämma PDHA1 kan denna skyddscircuit demonteras, vilket tillåter koppardriven celldöd att fortgå och återställa effekten av hormonblockerande terapi. Även om kliniska prövningar fortfarande krävs, pekar arbetet på en konkret, testbar strategi: att kombinera enzalutamid med PDHA1‑inriktade läkemedel som CPI‑613 för att övervinna resistens hos män med avancerad, svårbehandlad prostatacancer.
Citering: Zhuang, R., Zhou, Q., Cheng, B. et al. PDHA1–acetylation signaling suppresses cuproptosis to attenuate anti-androgen effect in prostate cancer. Cell Death Dis 17, 243 (2026). https://doi.org/10.1038/s41419-026-08462-1
Nyckelord: prostatacancer, läkemedelsresistens, kopparinducerad celldöd, cancermetabolism, epigenetisk reglering