Clear Sky Science · sv
Endotelial IRE1‑signalering upprätthåller blod‑hjärnbarriärens integritet och begränsar neuroinflammation efter traumatisk hjärnskada
Varför det är viktigt att skydda hjärnans inre vägg
Efter ett slag mot huvudet är den omedelbara skadan bara en del av bilden. Under de följande timmarna och dagarna mobiliserar hjärnan ett kraftfullt stress‑ och immunsvar som tyst kan förlänga skadan. Denna studie undersöker hur ett litet stresskännande system inne i cellerna som klär hjärnans blodkärl hjälper till att hålla hjärnans inre vägg — blod‑hjärnbarriären — tät och lugn efter traumatisk hjärnskada. Att förstå detta dolda försvar kan peka mot nya behandlingar som minskar bestående funktionsnedsättning efter skalltrauma.
Hjärnans grindvakter under stress
Hjärnan är beroende av en specialiserad barriär som bildas av endotelceller, vilka klär insidan av blodkärlen och noggrant styr vad som får passera från blod till hjärnvävnad. Traumatisk hjärnskada (TBI) kan rubba denna blod‑hjärnbarriär, vilket tillåter inflammatoriska molekyler och immunceller att strömma in och förvärra skadan. Inuti dessa endotelceller finns ett kvalitetskontrollsystem kallat den utfällda proteinresponsen (unfolded protein response), som hjälper celler att hantera stress i ett organell som kallas endoplasmatiskt retikulum. En av dess nyckelkomponenter, känd som IRE1, fungerar som sensor och regulator när celler utsätts för påfrestning. Forskarna ställde frågan: hjälper denna endoteliala stressensor till att försvara barriären efter TBI, eller förvärrar den situationen?
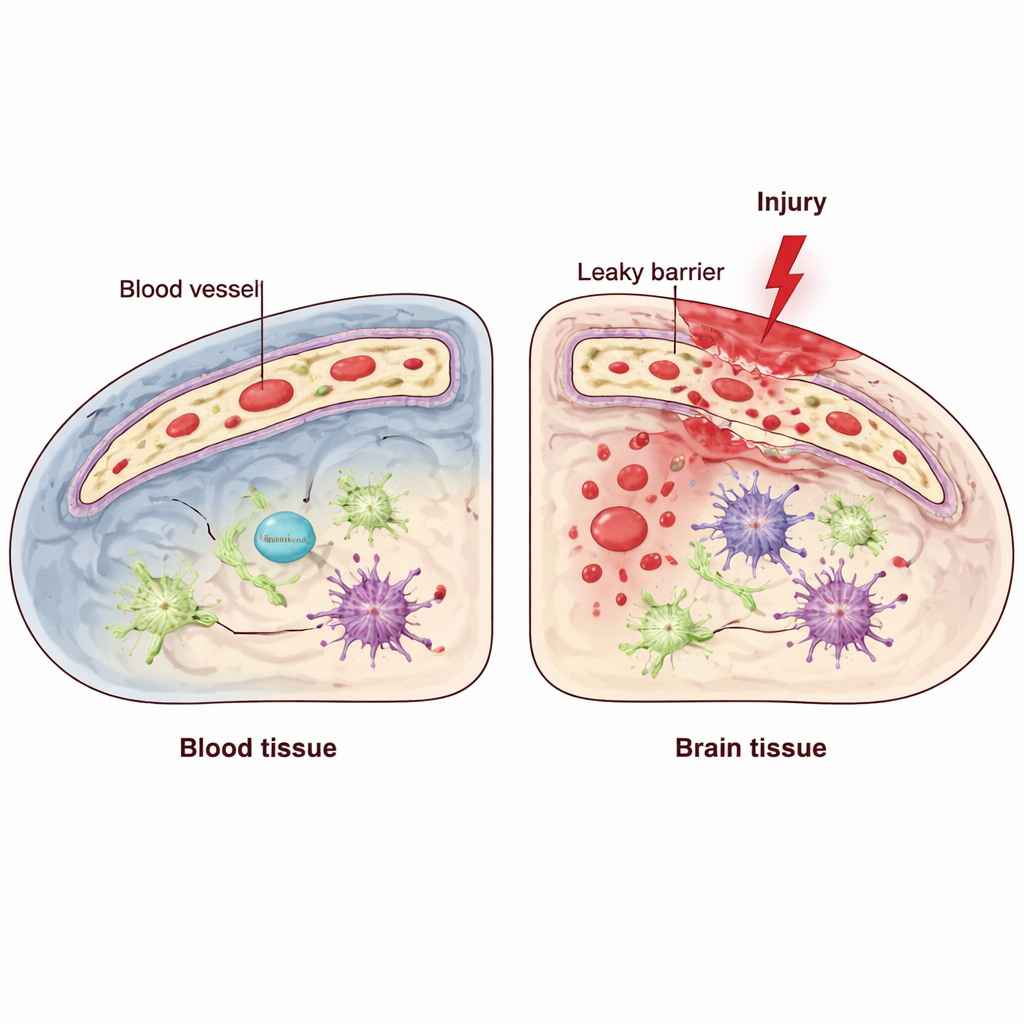
Stänger av en cellulär sensor i kärlceller
För att ta reda på det använde teamet genetiskt modifierade möss där IRE1 kunde stängas av selektivt bara i endotelceller. De skapade sedan en kontrollerad skada i motorområdet av cortex, som efterliknar delar av mänsklig TBI, och jämförde dessa möss med normala kullsyskon. De testade rörelse med uppgifter som mäter balans och precis tassplacering, och granskade hjärnvävnad med högupplöst mikroskopi och molekylära metoder. Hos normala möss ökade IRE1‑aktiviteten i kärlceller nära skadan kort efter traumat, vilket tyder på att endotelceller snabbt känner av och reagerar på stress. När IRE1 saknades specifikt i dessa celler presterade djuren sämre i motortesterna, vilket indikerar en sämre funktionell återhämtning.
Läckande kärl, fler immunceller och döende neuroner
Forskarlaget undersökte därefter hur väl blod‑hjärnbarriären höll tätt. Normalt stannar stora blodproteiner som antikroppar kvar i kärlen. Efter TBI förväntas viss läckage nära lesionen, men möss utan endotelialt IRE1 visade mycket mer utbredd genomträngning av dessa proteiner in i hjärnan. Mikroskopi visade att en viktig junction‑molekyl, VE‑cadherin, som hjälper till att täta endotelcellerna mot varandra, var reducerad i det skadade området när IRE1 saknades, även om det totala antalet kärl såg liknande ut. Detta läckage följdes av en våg av immunceller som trängde in i hjärnan runt lesionen och högre nivåer av inflammatoriska signaler. I samma områden visade neuroner i större utsträckning tecken på degeneration och programmerad celldöd, och zonen av skadad vävnad kring kärnskadan var tydligt större.
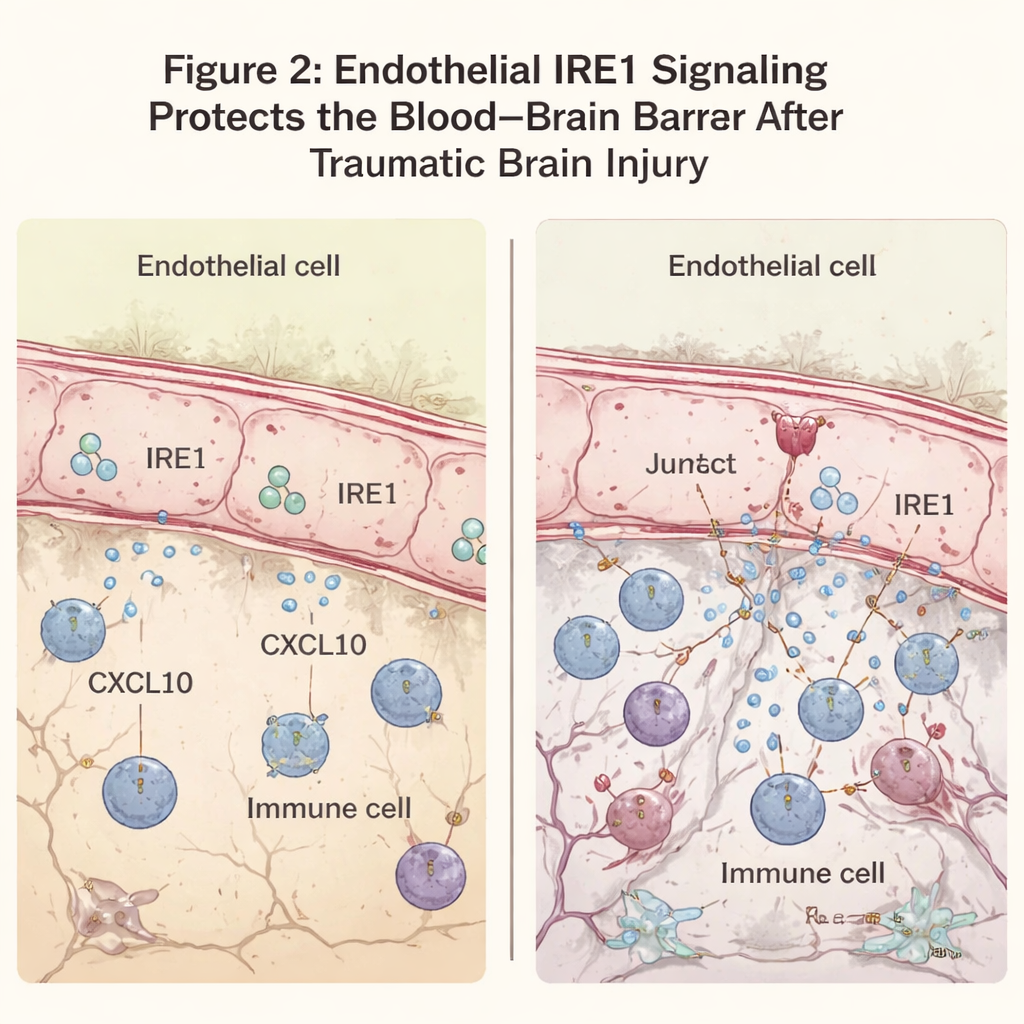
En stressdrog lugnar signalstormen
För att förstå de molekylära grunderna analyserade teamet vilka gener som aktiverades efter skadan. Hos möss utan endotelialt IRE1 ökade gener involverade i antiviral och inflammatorisk respons kraftigt. Framträdande bland dem var CXCL10, en kemokin — en slags molekylär signal — som lockar immunceller och kan försvaga barriären ytterligare. CXCL10 var särskilt förhöjd i endotelceller nära lesionen när IRE1 saknades. I odlade hjärnendotelceller som utsattes för en inflammatorisk utlösare sänkte minskad endoplasmatiskt retikulum‑stress med ett läkemedel kallat TUDCA både IRE1‑aktivitet och CXCL10‑produktion. När TUDCA gavs till skadade möss minskade CXCL10 och markörer för immunceller i den skadade cortexen och motoriken förbättrades, vilket antyder att dämpning av denna stressväg kan lindra sekundära skador.
Vad detta betyder för personer med huvudskador
Enkelt uttryckt tyder arbetet på att stressens sensor IRE1 i cellerna som klär hjärnans blodkärl fungerar som en väktare efter traumatisk hjärnskada. När den finns och fungerar hjälper den till att hålla blod‑hjärnbarriären tät, minskar utsöndringen av kemiska signaler som kallar på immunceller och begränsar spridningen av inflammation och neuronförlust runt lesionen. När den är avstängd blir barriären mer läckande, immunceller strömmar in och mer hjärnvävnad skadas. Eftersom kärlceller är relativt åtkomliga för läkemedel som cirkulerar i blodet kan riktade insatser mot deras stressresponser — med föreningar som TUDCA eller framtida mer precisa terapier — bli en praktisk strategi för att minska långsiktig skada efter skalltrauma.
Citering: Fan, Q., Takarada-Iemata, M., Tanaka, T. et al. Endothelial IRE1 signaling maintains blood–brain barrier integrity and limits neuroinflammation after traumatic brain injury. Cell Death Dis 17, 210 (2026). https://doi.org/10.1038/s41419-026-08461-2
Nyckelord: traumatisk hjärnskada, blod‑hjärnbarriär, endotelceller, neuroinflammation, cellulär stress