Clear Sky Science · sv
CD36 ökar känsligheten hos trippelnegativa bröstcancerceller för palmitatinducerad ferroptos
Varför fett runt tumörer kan vara både vän och fiende
Brösttumörer växer i vävnad som naturligt innehåller mycket fett, och cancerceller är kända för att ”äta” närliggande fettsyror. Denna studie undersöker en överraskande vändning: under rätt förhållanden kan en av de vanligaste fetterna i kroppen, palmitinsyra, faktiskt hjälpa till att döda en särskilt aggressiv form av bröstcancer genom att utlösa en specifik form av celldöd. Att förstå hur detta sker kan peka ut nya behandlingsvägar för patienter som i dag har få alternativ.
En svårbehandlad bröstcancer under mikroskopet
Trippelnegativ bröstcancer (TNBC) saknar de hormon- och tillväxtfaktorreceptorer som många moderna läkemedel riktar sig mot, vilket gör den till en av de svåraste bröstcancerformerna att behandla. Dessa tumörer lever i nära kontakt med fettceller som frisätter stora mängder fettsyror, inklusive den mättade fettsyran palmitinsyra. Forskarna ville ta reda på om palmitinsyra enbart driver tumörtillväxt eller om den också kan skapa en sårbarhet som går att utnyttja för att döda cancerceller.
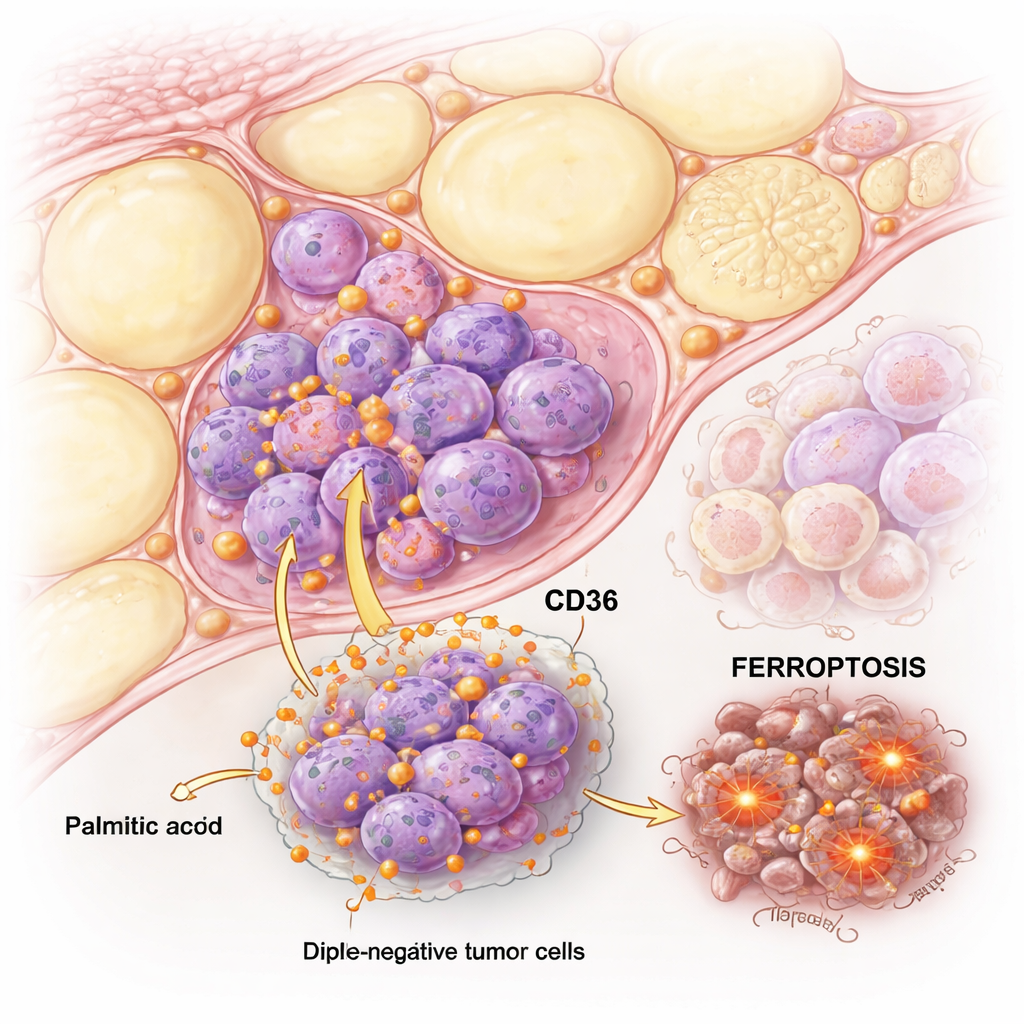
När palmitinsyra driver cancerceller över gränsen
Teamet jämförde TNBC-celler med hormonkänsliga ”luminala” bröstceller och utsatte dem för ökande mängder palmitinsyra. Båda celltyperna kunde skadas av höga doser, men TNBC-celler var betydligt mer känsliga. Detaljerade tester visade att palmitinsyra i luminala celler huvudsakligen utlöste klassisk apoptos, en ordnad form av celldöd. I TNBC-celler däremot satte palmitinsyra igång både apoptos och en annan, mindre välkänd väg kallad ferroptos, som är beroende av järn och nedbrytning av membranlipider.
En fettsyreport kallas CD36
För att förstå varför TNBC-celler reagerade så annorlunda fokuserade forskarna på CD36, ett protein på cellens yta som fungerar som en dörr för långkedjiga fettsyror. TNBC-celler bar naturligt betydligt mer CD36 än luminala celler, och exponering för palmitinsyra ökade CD36-nivåerna ytterligare. Det innebar att TNBC-celler tog upp mer palmitinsyra, ackumulerade fler skadade lipider, producerade mer reaktivt syre i sina mitokondrier och byggde upp mer fritt järn inuti cellen—alltså nyckelsignaler för ferroptos. När CD36 blockerades med ett läkemedel eller minskades med genetiska metoder sjönk palmitinsyrainducerad ferroptos kraftigt.
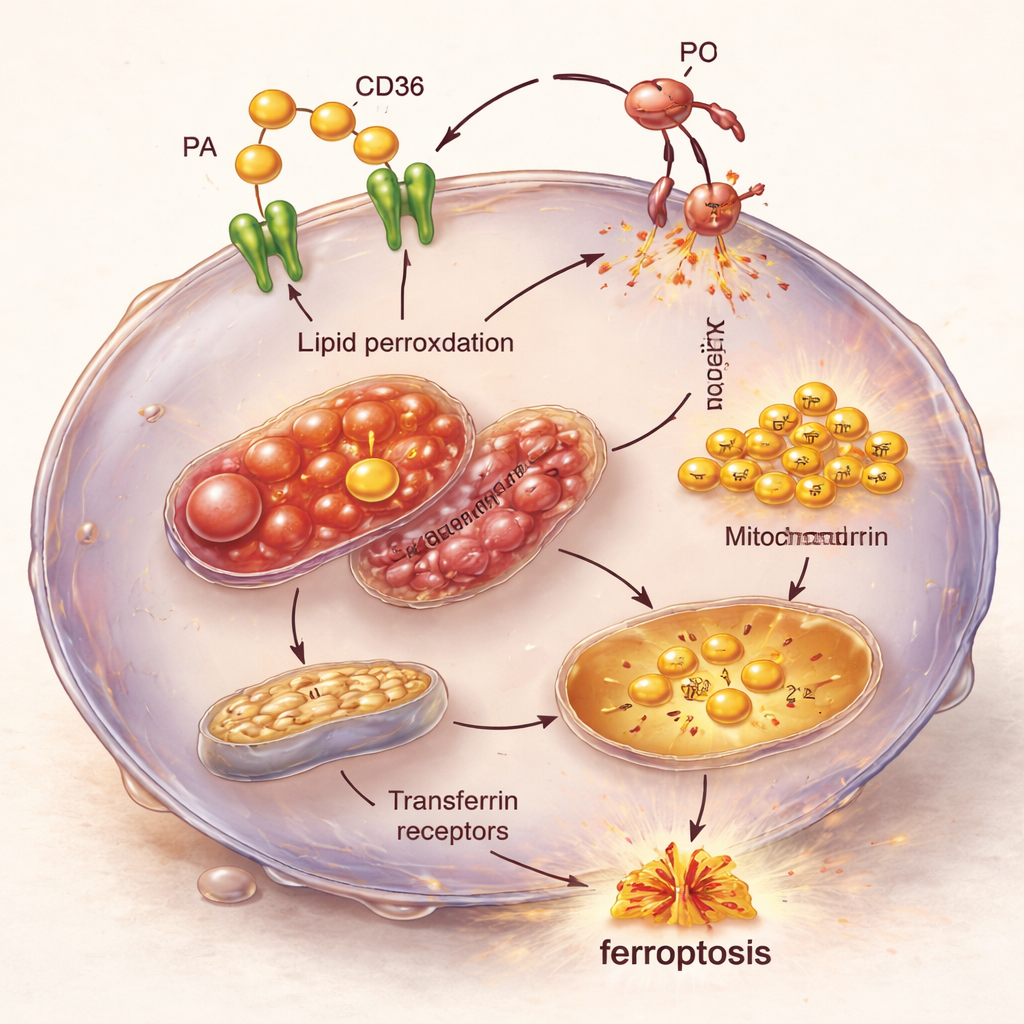
Fördjupning i kedjereaktionen inne i cellen
Mikroskopi och analyser av genaktivitet avslöjade den interna kedjereaktion som ligger bakom denna sårbarhet. TNBC-celler överlastade med palmitinsyra och CD36 visade svullna, strukturellt skadade mitokondrier och stigande järnnivåer som togs upp via transferrinreceptorer. Samtidigt aktiverades gener som främjar ferroptos, medan gener som normalt skyddar mot denna form av celldöd nedreglerades. Resultatet är en perfekt storm: överskott av fett som flödar in, mer järn tillgängligt för att driva kemiska reaktioner och försvagade försvar mot lipidoxidation—tillsammans pressar detta TNBC-celler in i ferroptos.
Vilka patienter kan ha mest nytta?
Cancer är inte enhetligt, inte ens inom TNBC. Med hjälp av tumörexemplar odlad i möss och stora patientdatabaser fann författarna att CD36 var särskilt hög i en viss TNBC-subtyp kallad luminal androgenreceptor (LAR), vilket tidigare noterats som mer känslig för ferroptos. Andra TNBC-subtyper med hög järnupptag visade också ofta högre CD36-nivåer. Detta mönster tyder på att CD36 skulle kunna fungera som en markör för att identifiera patienter vars tumörer är naturligt förberedda för ferroptosbaserade terapier.
Att vända en vanlig fettmolekyl till en terapeutisk allierad
Enkelt uttryckt visar detta arbete att en riklig kost- och kroppsfett, palmitinsyra, kan hjälpa till att döda vissa trippelnegativa bröstcancerceller när de uttrycker höga nivåer av fetttransportören CD36. Genom att driva fettöverlast, järnackumulering och skador på cellmembran gör CD36 dessa cancerceller mer benägna att genomgå ferroptos, ett förödande öde de inte kan undkomma. Om framtida behandlingar säkert kan förstärka denna väg—eller kombinera den med läkemedel som ytterligare försvagar cellernas försvar—kan kliniker kunna vända en metabol svaghet till ett nytt, mer precist sätt att angripa några av de mest aggressiva brösttumörerna.
Citering: Closset, L., Foy, JP., Louadj, L. et al. CD36 enhances sensitivity of triple negative breast cancer cells to palmitate-induced ferroptosis. Cell Death Dis 17, 219 (2026). https://doi.org/10.1038/s41419-026-08460-3
Nyckelord: trippelnegativ bröstcancer, ferroptos, CD36, palmitinsyra, tumörmetabolism