Clear Sky Science · sv
USP30-medierad deubiquitination av hexokinas 2 styr glukosens metaboliska öde och tumörprogression
Hur cancerceller omkopplar sitt sockerbruk
Cancerceller är kända för sin "söta tand": de förbränner socker på ovanliga sätt för att driva snabb tillväxt. Denna studie avslöjar en ny brytare, ett protein kallat USP30, som hjälper tumörceller att avgöra hur de ska använda glukos. Genom att finjustera ett annat protein, hexokinas 2 (HK2), kan USP30 skjuta cancerceller mot ökad sockerförbränning och snabbare tillväxt, vilket pekar ut ett nytt mål för framtida cancerläkemedel. 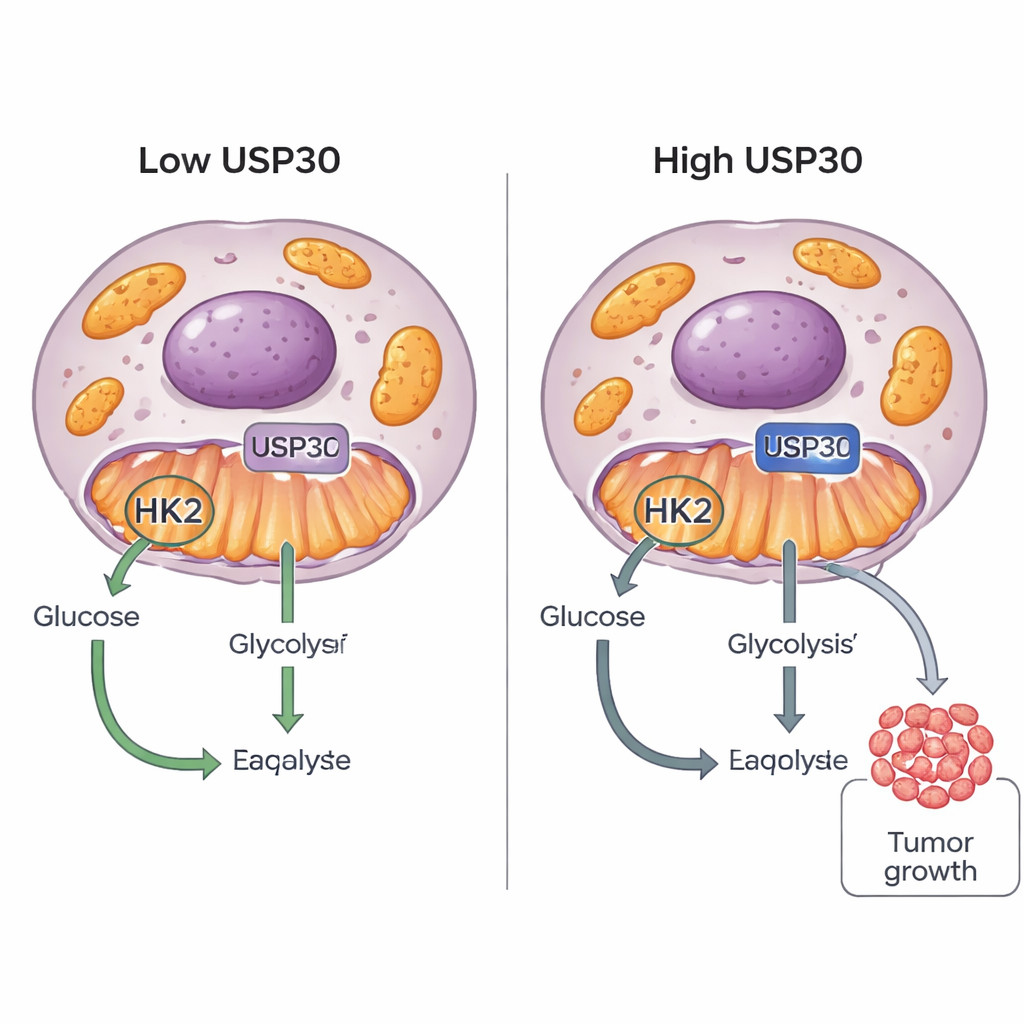
En sockerhungrig livsstil inne i tumörer
De flesta friska celler utvinner energi från näringsämnen effektivt, men många cancerceller föredrar en snabb och slarvig väg kallad aerob glykolys, även känd som Warburg-effekten. De tar upp stora mängder glukos och omvandlar det snabbt till laktat, även när syre finns tillgängligt. Denna strategi gör mer än att bara skapa energi: den förser byggstenar för DNA, fetter och proteiner, hjälper tumörer att överleva stress och kan till och med försvaga immunförsvaret. Vid ingången till denna väg sitter hexokinas, ett enzym som märker inkommande glukos med en fosfatgrupp och därmed förbinder det med vidare nedbrytning och tillväxtstödjande kemi.
Ett mitokondriellt enzym kliver in i rampljuset
USP30 är ett enzym placerat på mitokondriens yttre yta, cellens kraftverk. Det tillhör en familj av "deubiquitinaser" som tar bort små proteintaggar kallade ubiquitin från andra proteiner, ofta och därigenom ändrar deras stabilitet, lokalisering eller aktivitet. USP30 var redan känt för roller i hjärnceller och i kontrollen av mitokondriell kvalitet, men dess påverkan på cancer var oklart. Genom att gräva i stora cancergendatabaser lade forskarna märke till att tumörer med högre USP30-nivåer tenderade att visa starkare glukosförbränningssignaturer och svagare fettförbränningssignaturer, vilket antyder att USP30 kan hjälpa cancer att skifta mot en sockerdriven livsstil.
Att koppla USP30 till cellens sockerportvakter
För att undersöka denna koppling sänkte eller tog teamet bort USP30 i flera cancercellinjer och mätte hur de bearbetade energi. Med instrument som spårar syraproduktion och syreförbrukning i realtid fann de att förlust av USP30 kraftigt minskade både glykolys och mitokondriell respiration. Laktatproduktionen och glukosförbrukningen sjönk, vilket visade att cellernas sockerförbränningsmotor hade försvagats. En serie masspektrometriexperiment avslöjade sedan att USP30 fysiskt interagerar med flera enzymer kopplade till glukosmetabolism, särskilt hexokinaserna HK1 och HK2. Uppföljande tester visade att denna interaktion beror på USP30:s katalytiska aktivitet och sker direkt, inte bara genom indirekta partners.
En precis molekylär grepp om hexokinas 2
Närmare studier visade att USP30 tar bort specifika typer av ubiquitin-kedjor — så kallade atypiska kopplingar — från HK1 och HK2. För HK2 sker denna redigering vid en enda avgörande aminosyra, lysin 144 (K144). När K144 är muterad så att den inte längre kan bära ubiquitin blir HK2 mer stabilt, binder starkare till en kanalprotein kallad VDAC1 på mitokondrierna och visar högre enzymaktivitet. Celler som konstruerats för att bära denna K144‑ändring skickade mer HK2 till mitokondrier, förbrände mer glukos, släppte ut mer laktat och visade snabbare tillväxt och rörlighet i odlingsplattor. I möss växte tumörer framställda från celler med K144‑mutant HK2 större och snabbare än de med normalt HK2, vilket understryker kraften i denna lilla molekylära brytare. 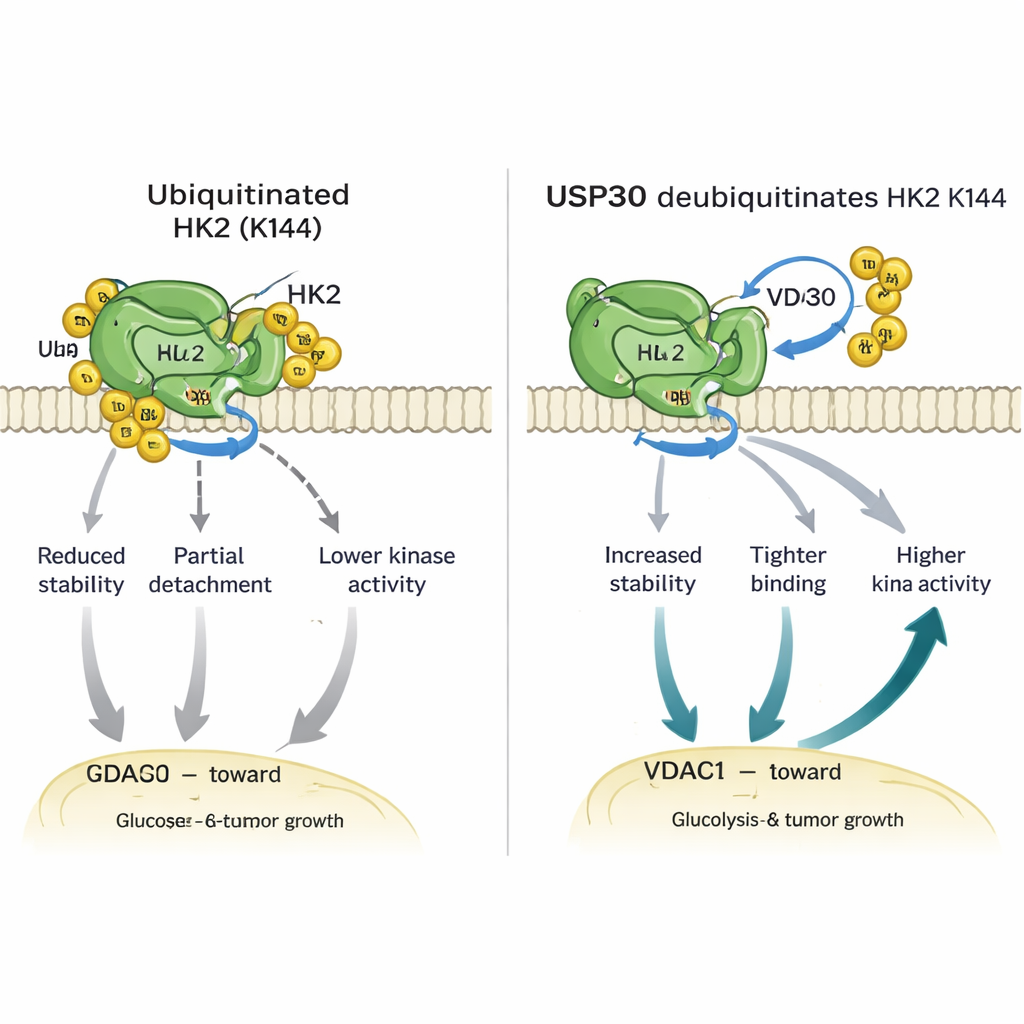
Att vända en metabolisk brytare till en tillväxtfördel
Dessa resultat kartlägger en tydlig händelsekedja: USP30 binder till HK2, tar bort ubiquitintaggar från K144, och genom det håller HK2 aktivt och förankrat vid mitokondrierna. Detta ökar glykolysen, matar tumörcellernas delning och migration, och påskyndar i slutändan tumörtillväxt. När USP30 saknas eller är inaktivt blir HK2 mindre stabilt och mindre effektivt, och cancercellerna förlorar en del av sin metaboliska fördel. För en lekmannaärende fungerar USP30 som en mekaniker som håller cancercellens sockermotor justerad och fastskruvad — ta bort mekanikern, och motorn hackar.
Vad detta betyder för framtida cancerbehandlingar
För en icke-specialist är huvudpoängen att cancerceller förlitar sig på finjusterad kontroll över hur de förbränner socker, och USP30 är en nyligen upptäckt ratt på den kontrollpanelen. Genom att stabilisera HK2 vid en specifik plats hjälper USP30 tumörer att driva sin glukos‑hungriga metabolism och växa mer aggressivt. Läkemedel som blockerar USP30, eller som stör dess grepp om HK2 vid lysin 144, skulle kunna försvaga tumörer genom att svälta deras sockermotor utan att nödvändigtvis skada normala celler i samma utsträckning. Detta arbete lägger därmed till en viktig pusselbit i förståelsen av hur cancer omskapar metabolismen och föreslår en lovande ny vinkel för riktade terapier.
Citering: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
Nyckelord: cancermetabolism, glykolys, hexokinas 2, USP30, Warburg-effekten