Clear Sky Science · sv
Oocytspecifik knockout av eIF2-subenheter orsakar apoptos hos musoocyter i tidigt växande folliklar via mitokondriella dysfunktioner och DNA-skador
Varför äggcellernas liv betyder något
Kvinnor föds med alla de äggceller de någonsin kommer att ha, lagrade i små strukturer i äggstocken som kallas folliklar. När dessa folliklar går förlorade för snabbt kan kvinnor utveckla prematur ovarialsvikt (POI), ett tillstånd som leder till tidig infertilitet och ofta klimakterieliknande symtom vid ung ålder. Denna studie i möss ställer en grundläggande men avgörande fråga: vad händer inne i äggceller när ett nyckelsteg i nyproteinsyntesen går fel, och hur kan det leda till tidig förlust av fertilitet?
Cellens startknapp för protein
För att hålla sig friska måste äggceller ständigt tillverka rätt proteiner vid rätt tidpunkt. En central del av denna process är ett trefaldigt molekylärt maskineri kallat eIF2, som hjälper till att påbörja proteinsyntesen från genetiska budskap. Forskarna stängde selektivt av två av eIF2:s delar, kallade eIF2α och eIF2β, endast i musoocyter i tidiga stadier av follikelutvecklingen. När någon av subenheterna saknades blev honorna fullständigt infertila. Deras äggstockar var mindre, och den normala övergången från tidiga folliklar till mogna, äggfrisättande folliklar stannade i stort sett av, med betydligt färre folliklar i alla senare stadier. Med tiden var i princip alla folliklar uttömda, vilket efterliknade ett allvarligt, tidigt insättande POI-liknande tillstånd.
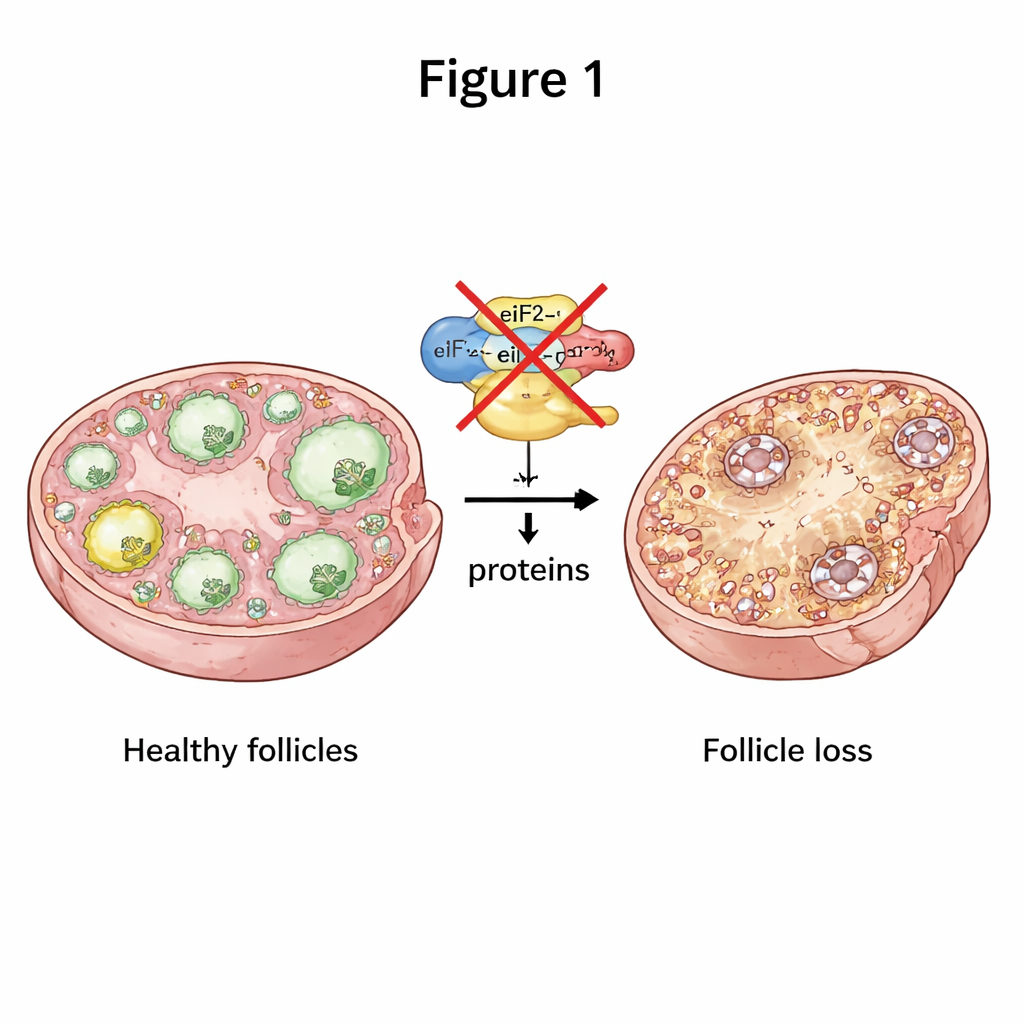
När kommunikationen i äggstocken bryts
Folliklar är inte bara äggceller som flyter ensamma; de utgör täta partnerskap mellan en äggcell och omgivande ”hjälparceller” som kallas granulosaceller. Teamet fann att utan eIF2β producerade äggceller avsevärt mindre av flera viktiga signalproteiner som normalt stödjer granulosacellernas tillväxt och näringstillförsel. De fysiska broarna mellan ägg- och granulosaceller var oorganiserade och förkortade, och äggets ytmikrovilli såg förkrympta och skadade ut under elektronmikroskopet. Granulosaceller i dessa folliklar delade sig mindre och dog oftare. Denna sammanbrottna tvåvägskommunikation innebar att folliklarna inte kunde växa ordentligt, vilket drev äggstocken mot follikelförlust.
Strömavbrott i äggcellens batterier
Mitokondrier, ofta kallade cellens kraftverk, är särskilt viktiga i äggceller eftersom de förser den energi som krävs för tillväxt och senare embryoutveckling. I eIF2β-bristande oocyter sjönk den övergripande hastigheten för nyproteinsyntes, och många mitokondrierelaterade proteiner minskade. Mitokondrierna blev abnormt långa, klumpade sig nära cellens yta och visade svagare membranpotential, lägre energinivåer (ATP) och färre kopior av mitokondrie-DNA. Samtidigt ackumulerade cellerna höga nivåer av reaktiva syreradikaler (ROS), aggressiva syrebaserade molekyler som kan skada cellulära komponenter. Tillsammans avslöjade dessa förändringar en djup kollaps i mitokondriell dynamik och funktion.
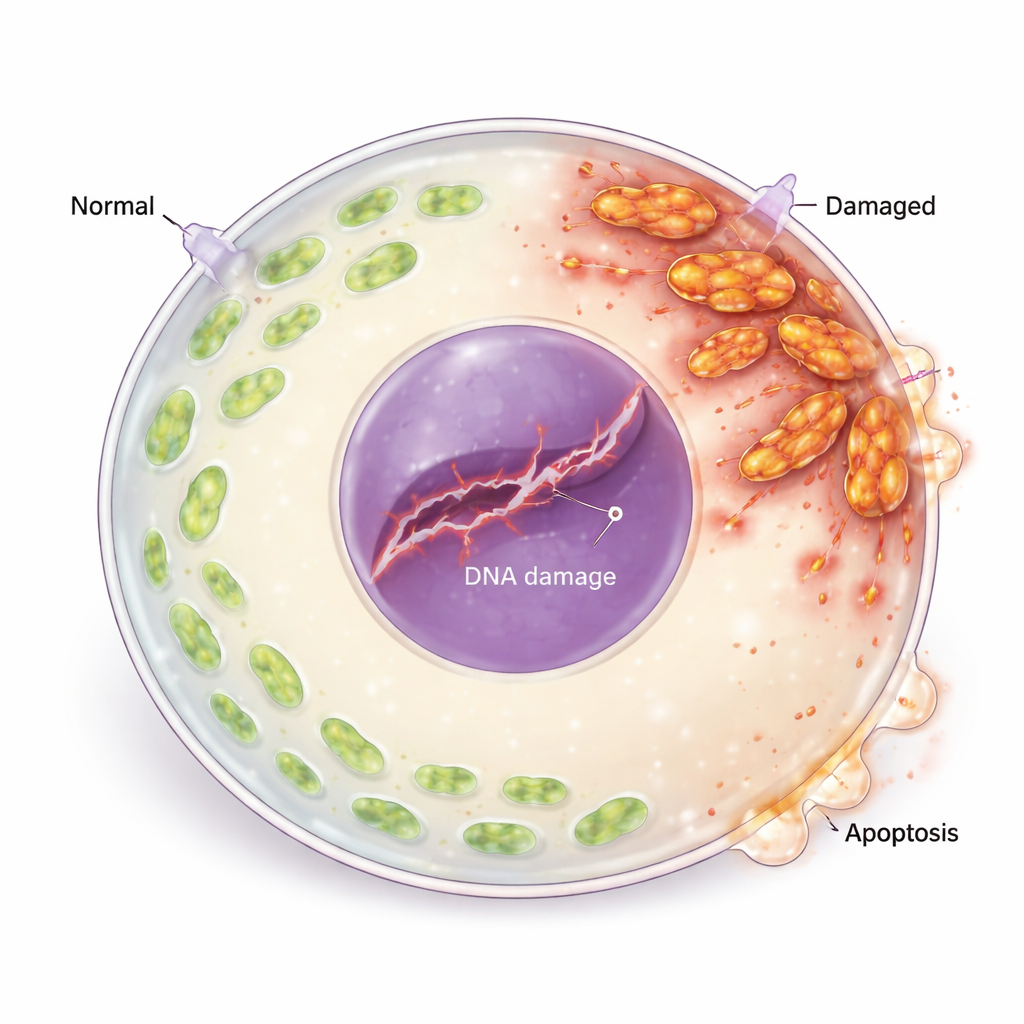
Från oxidativ stress till DNA-skada och celldöd
Överskott av ROS skadade inte bara mitokondrierna; det skadade också äggcellens genetiska material. Forskarna såg ökade markörer för brutna DNA-strängar och aktivering av cellens DNA-skaderespons, inklusive proteiner som känner av och signalerar genetiska skador. Ett centralt reparationsprotein var reducerat, vilket tyder på att skadorna inte reparerades effektivt. Nedströms skiftade balansen mellan livs- och dödsregulatorer: pro-dödsproteiner ökade medan skyddande anti-dödsproteiner minskade, och äggcellerna visade tydliga tecken på programmerad celldöd (apoptos). När teamet behandlade oocyterna med en antioxidant (N-acetylcystein) sjönk ROS-nivåerna, DNA-skador och apoptosmarkörer minskade och äggmognaden förbättrades, vilket direkt kopplar oxidativ stress till förlust av äggceller.
Vad detta betyder för tidigt ovarieinsufficiens
Genom att följa händelseförloppet från ett enda molekylärt komplex (eIF2) till felaktig proteinsyntes, mitokondriellt sammanbrott, oxidativ stress, DNA-skador och slutligen äggcellsdöd, beskriver detta arbete en detaljerad kedja av händelser som kan förgöra äggstocksreserven. Studien stärker idén att mutationer i faktorer som initierar translation, redan påvisade hos vissa kvinnor med POI, kan skada äggceller direkt genom denna bana. Den pekar också ut potentiella sätt att hjälpa: antioxidanter, modulatorer av stressresponser eller behandlingar som skyddar tidiga folliklar (till exempel anti-Müllerskt hormon, som delvis bevarade vilande folliklar i dessa möss) kan en dag stödja fertilitet hos patienter vars äggstockar är känsliga för liknande påfrestningar.
Citering: Liu, H., Wang, W., Li, B. et al. Oocyte-specific knockout of eIF2 subunits causes apoptosis of mouse oocytes within the early growing follicles via mitochondrial dysfunctions and DNA damage. Cell Death Dis 17, 196 (2026). https://doi.org/10.1038/s41419-026-08449-y
Nyckelord: prematur ovarialsvikt, oocytapoptos, mitokondriell dysfunktion, proteinsyntes, reaktiva syreradikaler