Clear Sky Science · sv
Transglutaminas 2 förvärrar överlevnaden vid ovarialcancer genom att direkt inaktivera GSK3β
Varför denna forskning är viktig för kvinnors hälsa
Ovarialcancer är en av de dödligaste cancerformerna hos kvinnor eftersom den ofta upptäcks sent och ofta återkommer trots kraftfull cytostatikabehandling. Denna studie avslöjar hur ett relativt okänt protein, transglutaminas 2 (TGase 2), hjälper ovarialcancerceller att överleva behandling och sprida sig i kroppen. Genom att blottlägga denna dolda hjälpare pekar arbetet på nya sätt att göra befintliga läkemedel mer effektiva och att bromsa eller stoppa dödlig metastasering.
En dold drivkraft i aggressiva tumörer
Läkare har länge observerat att många ovarialcancerformer blir resistenta mot kemoterapi och sprider sig vida i buken. En viktig orsak är en process kallad epitelial–mesenkymal omvandling (EMT), där cancerceller lossnar från varandra, blir mer rörliga och beter sig mer som invasiva ”vandrare” än som organiserade vävnadsceller. Författarna visar att TGase 2, som finns i mycket låga nivåer i normal äggstock men i mycket högre nivåer i ovariala tumörer, är starkt knutet till denna förskjutning. I ett stort panelmaterial av mänskliga vävnadsprover steg TGase 2-nivåerna stadigt från tidiga tumörer till avancerad och metastaserande sjukdom, och dess förekomst matchade väl aktiviteten hos många EMT-relaterade gener som styr cellrörelse, tillväxt och blodkärlsbildning. 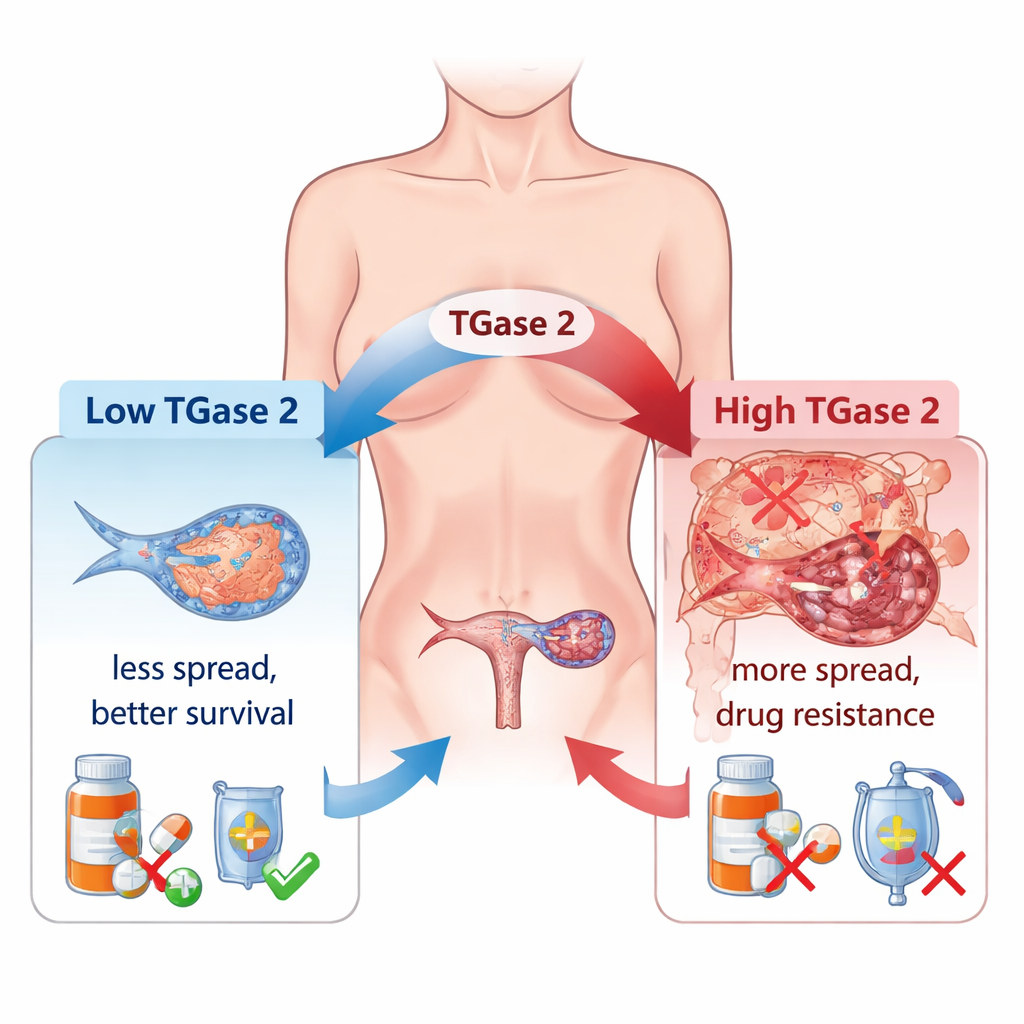
Hur TGase 2 stänger av en viktig säkerhetsbroms
För att förstå vad TGase 2 faktiskt gör inne i cancercellerna fokuserade forskarna på dess relation med ett annat protein, GSK3β. Under friska förhållanden fungerar GSK3β som en broms mot invasion: det håller nivåerna av signalmolekylen β‑catenin låga, vilket i sin tur dämpar gener som driver EMT. Teamet upptäckte att TGase 2 fysiskt binder till GSK3β och både försvagar dess aktivitet och underlättar dess nedbrytning via cellens återvinningssystem, en väg kallad autofagi. När TGase 2 var rikligt förekommande migrerade ovarialcancerceller lättare och visade högre nivåer av klassiska EMT-markörer som fibronectin, vimentin och β‑catenin. När forskarna minskade TGase 2 med genetiska verktyg sjönk dessa invasiva egenskaper och β‑catenin‑signaleringen dämpades, vilket visar att TGase 2 inaktiverar en avgörande säkerhetsbroms mot metastasering.
Från cancerceller till levande djur
Gruppen undersökte sedan om blockering av TGase 2 faktiskt kunde bromsa cancer i djurmodeller. De konstruerade ovariala cancerceller utan TGase 2‑genen och implantatde dem i möss. Jämfört med möss som fått normala cancerceller utvecklade djur som fått TGase 2‑defekta celler mindre tumörbörda och levde längre. I en separat modell som efterliknar cancerspridning via blodbanan utvecklade möss som injicerats med TGase 2‑defekta celler betydligt färre och mindre lungmetastaser. Viktigt var att dessa metastatiska insättningar visade högre nivåer av GSK3β, vilket stämmer med idén att borttagande av TGase 2 återställer den naturliga bromsen mot invasion och hjälper till att begränsa sjukdomen.
Att översätta ett laboratorieledtråd till en läkemedelsstrategi
Eftersom att ta bort en gen inte är praktiskt hos patienter testade författarna en liten molekyl kallad streptonigrin, tidigare känd för att binda samma ände av TGase 2 som används för att greppa andra proteiner. De fann att streptonigrin kunde störa interaktionen mellan TGase 2 och GSK3β i celler, minska deras samlokalisering och begränsa cancercellernas migration. I musmodeller av ovarialcancer saktade oral behandling med streptonigrin tumörtillväxten, krympte metastatiska lesioner och förlängde överlevnaden. Mest anmärkningsvärt var att när streptonigrin kombinerades med standardkemoterapier som cisplatin eller paklitaxel levde mössen veckor längre än med bara kemoterapi. Kemoterapi ensam tenderade att öka TGase 2‑nivåerna och sänka GSK3β, vilket indirekt pushade cellerna mot EMT, men tillsats av TGase 2‑hämmaren vände denna trend och dämpade cellernas nyvunna rörlighet. 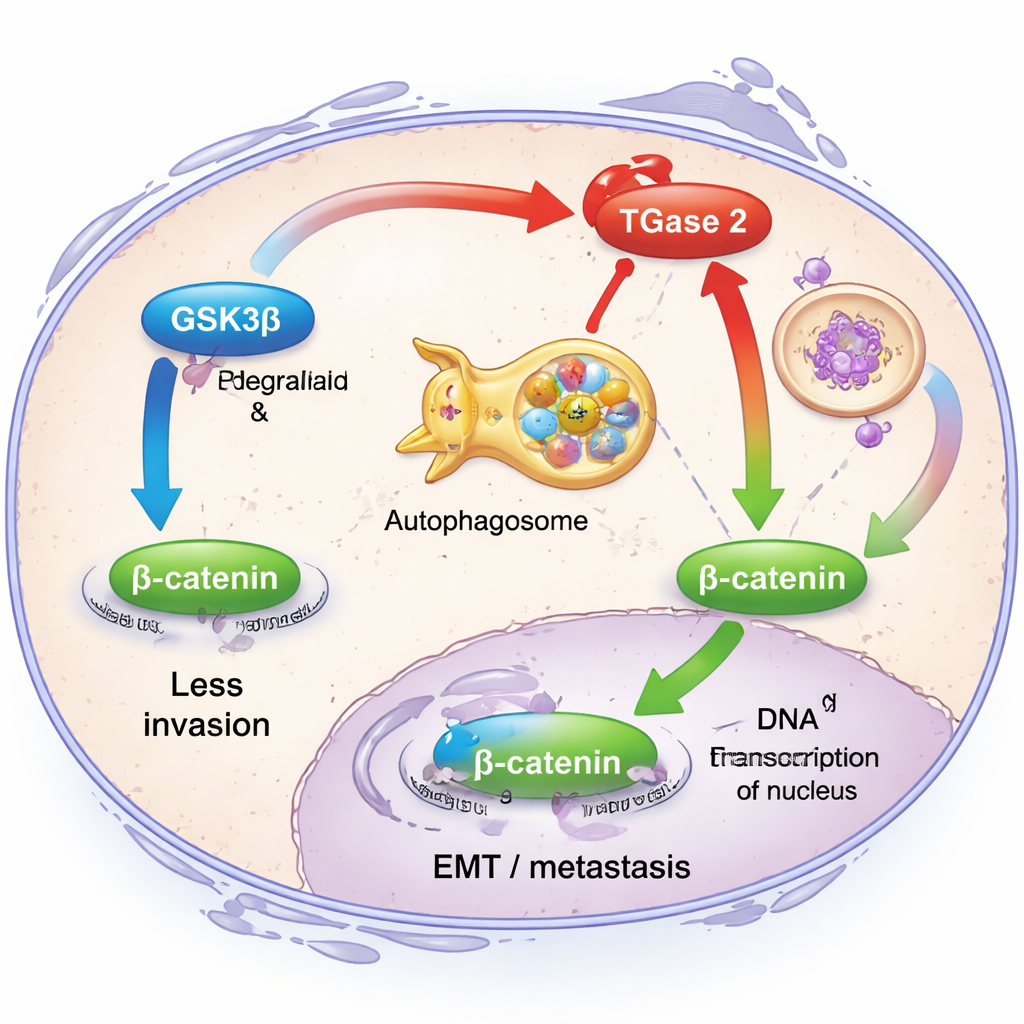
Vad detta kan innebära för framtida behandling
För en icke‑specialist är huvudbudskapet att ovarialcancerceller utnyttjar TGase 2 för att stänga av en inbyggd broms mot metastasering och för att klara av trycket från kemoterapi. Genom att direkt inaktivera GSK3β och stabilisera β‑catenin hjälper TGase 2 tumörer att bli mer invasiva och läkemedelsresistenta. Detta arbete antyder att läkemedel riktade mot TGase 2:s N‑terminala region—som streptonigrin eller framtida, säkrare föreningar modellerade efter den—kan göra befintlig kemoterapi mer effektiv, minska risken för återfall och förbättra överlevnaden. I enkla termer kan riktad behandling mot TGase 2 stänga av en cancer "flyktrutt", vilket håller ovarialtumörer mer känsliga för behandling och mindre benägna att sprida sig.
Citering: Lee, H., Kang, J.H., Kim, H.J. et al. Transglutaminase 2 exacerbates ovarian cancer survival by directly inactivating GSK3β. Cell Death Dis 17, 199 (2026). https://doi.org/10.1038/s41419-026-08447-0
Nyckelord: ovarialcancer, läkemedelsresistens, metastasering, epitelial-mesenkymal omvandling, riktad terapi