Clear Sky Science · sv
Hämning av autoantigen‑inducerad internalisering av B‑cellens receptor (BCR) som en terapeutisk strategi i diffust storcelligt B‑cellslymfom (DLBCL)
Varför detta är viktigt för patienter
Diffust storcelligt B‑cellslymfom (DLBCL) är den vanligaste snabbväxande blodcancerformen hos vuxna, och många patienter får fortfarande återfall efter standard kemoterapi‑immunterapi. Denna studie undersöker en oväntad svag punkt i en stor delmängd av dessa tumörer: deras beroende av en yt‑antenn kallad B‑cellsreceptorn (BCR). Genom att visa att blockering av hur denna antenn dras in i cellen kan försvaga cancercellers överlevnad öppnar arbetet för att återanvända långvarigt använda läkemedel mot illamående och antipsykotika som riktade hjälpmedel mot lymfom.
Cancercellens antenn
B‑celler, en typ av vita blodkroppar, använder B‑cellsreceptorn på ytan för att känna igen hot. I många DLBCL, särskilt den hög‑riskabla "aktiverade B‑cell" (ABC)‑subtypen, kapras samma receptor för att sända kontinuerliga "behåll dig vid liv och väx"‑signaler. Ofta känner dessa BCR igen kroppens egna molekyler (autoantigener), som fungerar som en fastnat dörrklocka. När autoantigener binder gör BCR mer än att bara signalera vid ytan: den dras in i cellen och går med i en intern proteinkluster med sensorer som kallas TLR9 och MYD88. Detta superkomplex aktiverar sedan NFκB, en kraftfull tillväxt‑främjande signalväg. Fram till nu var det oklart om denna inre resa av receptorn verkligen krävdes för de cancerdrivande signalerna.
Omkoppling av antennen för att testa dess gränser
För att besvara den frågan använde forskarna CRISPR‑genredigering för att precist förändra "topparna" av BCR i lymfomcellinjer. De ersatte de naturliga, självreaktiva igenkänningsregionerna med varianter som känner igen ovalbumin, ett ofarligt äggprotein som används som laboratorieverktyg. Dessa modifierade receptorer grep inte längre sina vanliga autoantigener, men kunde fortfarande aktiveras på ett kontrollerat sätt med tillfört ovalbumin. I ABC‑typens lymfomceller som normalt beror på självantigenbindning minskade denna omkoppling kraftigt aktiviteten hos många viktiga signaleringsenzym och dämpade NFκB‑responsiva gener. Cellerna växte långsammare, trots att de faktiskt hade fler BCR på ytan, vilket visar att fortlöpande engagemang av autoantigener och efterföljande intern signalering är avgörande för deras överlevnad.
Att dra in receptorer: ett avgörande steg
Teamet undersökte sedan direkt vad som händer med BCR efter att den möter sitt antigen. I deras konstruerade modeller fick både antikroppsbaserade trigger och ovalbumin receptorn att försvinna från cellytan inom minuter, vilket bekräftar snabb internalisering. Detta skedde inte bara när antigenet flöt utanför cellen, utan även när det konstgjort visades på samma cells membran, vilket efterliknar vissa verkliga tumörsituationer. Att blockera denna inre trafik genetiskt, med en dominant‑negativ form av ett protein kallat dynamin‑2 som är nödvändigt för klatrin‑medierad endocytos, höll BCR kvar på ytan, krympte de interna BCR–TLR9–NFκB‑komplexen, minskade NFκB‑målgener och saktade ned celltillväxten. Intressant nog, när endocytosen blockerades ökade vissa "bakgrunds"‑BCR‑signaler vid ytan, vilket tyder på att cancerceller kan försöka kompensera genom att höja en svagare, tonisk signaleringsläge.
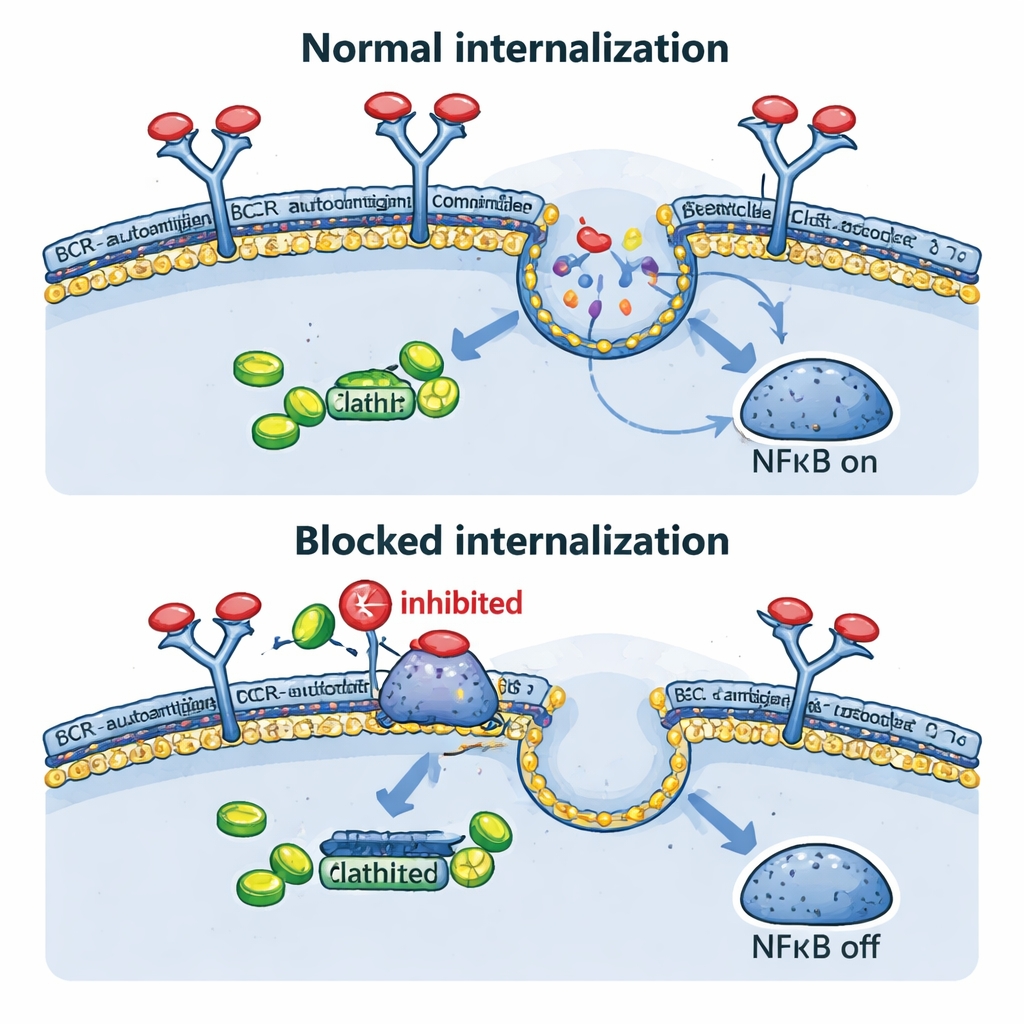
Gammal medicin, nya knep
Eftersom utveckling av nya läkemedel är långsamt och kostsamt undrade författarna om befintliga läkemedel som blockerar endocytos kunde efterlikna de genetiska experimenten. Fenotiaziner, en familj av antipsykotiska och anti‑illamående läkemedel, är kända för att hämma dynamin‑2 och klatrinberoende upptag av receptorer. I lymfomceller ökade föreningar som proklorperazin och klorpromazin BCR‑nivåerna på ytan och minskade starkt antigen‑driven internalisering. Detta ledde till lägre NFκB‑driven genaktivitet och minskad livskraft hos ABC‑typens DLBCL‑celler, särskilt de med intakta BCR‑komponenter. I möss med mänskliga lymfomtransplantat saktade proklorperazin vid kliniskt uppnåeliga doser tumorväxten avsevärt. Dessutom gav kombinationer av fenotiaziner med läkemedel som blockerar andra BCR‑kopplade enzymer, såsom SYK och PI3Kδ, kraftfullare cancer‑dödande effekter än någon av behandlingarna ensam.
Vad detta kan innebära för behandling
Sammanfattningsvis visar studien att för en betydande undergrupp av DLBCL är de cancerdrivande signalerna inte bara ett resultat av receptorer vid cellytan; de är beroende av att BCR–antigen‑komplexet dras in genom en specifik endocytosväg. Att avbryta detta steg — antingen med genetiska knep eller med fenotiaziner — försvagar NFκB‑signaleringen och försämrar tumörcellernas överlevnad, samtidigt som det potentiellt gör cellerna känsligare för befintliga BCR‑vägsinhibitorer. Eftersom fenotiaziner redan har välkända doserings‑ och säkerhetsprofil som anti‑illamående läkemedel ger detta arbete en realistisk plan för kliniska prövningar som testar dem, ensamma eller i kombination, hos patienter vars lymfom visar autoantigen‑beroende BCR‑aktivitet.
Citering: Górniak, P., Polak, A., Rams, A. et al. Inhibition of autoantigen-induced B-cell receptor (BCR) internalization as a therapeutic strategy in diffuse large B cell lymphoma (DLBCL). Cell Death Dis 17, 216 (2026). https://doi.org/10.1038/s41419-026-08446-1
Nyckelord: diffust storcelligt B‑cellslymfom, B‑cellsreceptor, endocytos, fenotiaziner, NFkB‑signalering