Clear Sky Science · sv
Tidsupplöst multiomisk analys av exponering för paclitaxel i mänskliga iPSC‑avledda sensoriska neuroner avslöjar mekanismer för kemoterapiinducerad perifer neuropati
Varför vissa cancerläkemedel skadar nerver
Kemoterapi har hjälpt miljontals människor att överleva cancer, men många patienter betalar ett dolt pris: månader eller år av brännande smärta, pirrningar och domningar i händer och fötter. Denna studie ställer en enkel men viktig fråga: vad gör det välanvända cancerläkemedlet paclitaxel exakt mot mänskliga sensoriska nervceller, och kan förståelsen av dessa förändringar peka ut vägar till bättre förebyggande och behandling av denna nervskada?
Från patienters celler till laboratorieodlade smärtkänsliga nerver
I stället för att förlita sig på djurförsök började forskarna med celler från fem mänskliga donatorer, inklusive bröstcancerpatienter som hade fått paclitaxel. De omprogrammerade dessa celler till inducerade pluripotenta stamceller och styrde dem sedan att bli sensoriska neuroner—samma typ av nervcell som för känsel och smärtsignaler från huden till ryggmärgen. Dessa laboratorieodlade neuroner bildade långa, sköra fibrer och uppvisade elektrisk aktivitet mycket lik verkliga smärtkännande nerver i kroppen. Teamet utsatte dem sedan för ökande doser paclitaxel, som efterliknade läkemedelsnivåer som ses hos patienter, och följde cellernas hälsa över flera dagar. Vid låga koncentrationer klarade neuronerna sig väl, men vid en kliniskt relevant dos (100 nM) började deras överlevnad sjunka efter ungefär två dagar, vilket markerar början på toxisk nervskada.
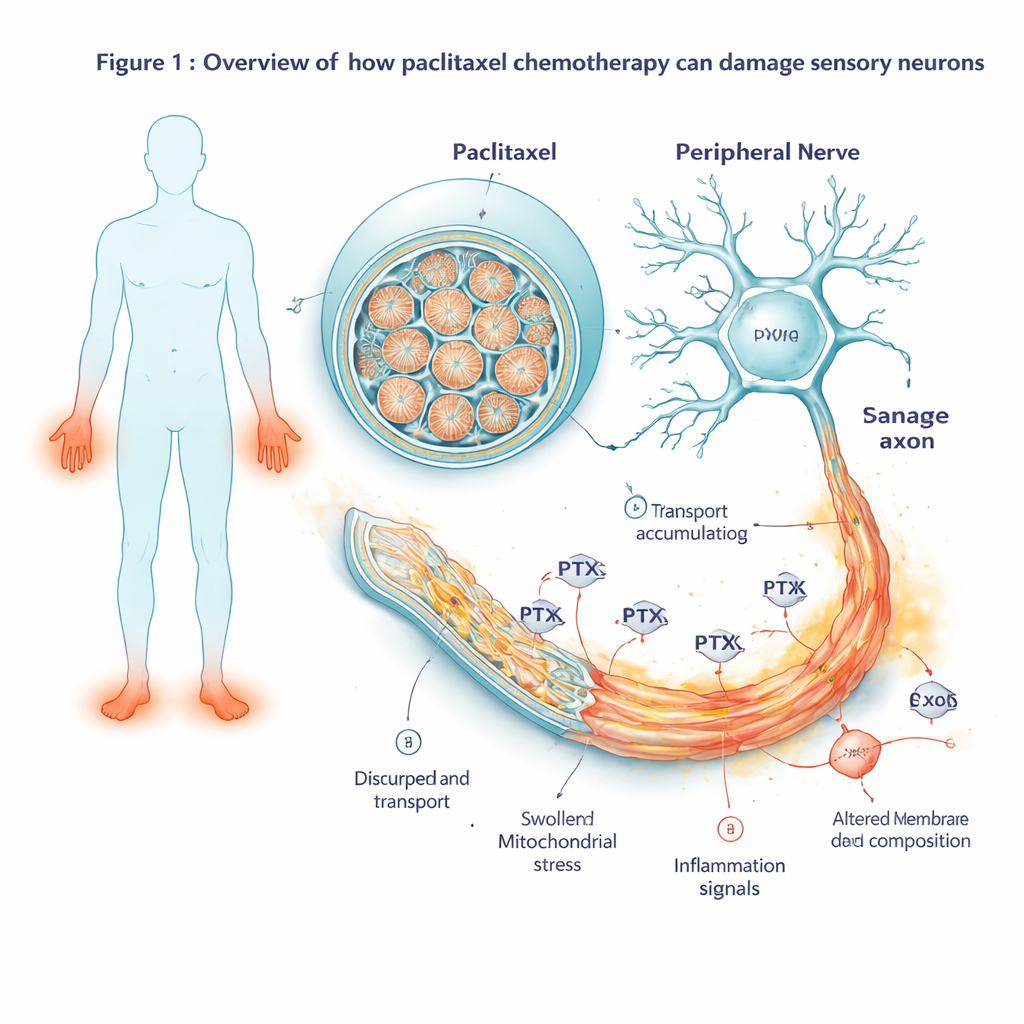
Att följa genaktivitet över tid
För att se hur cellerna reagerade innan de synligt försämrades mätte forskarna vilka gener som slog på eller av vid flera tidpunkter från två timmar efter läkemedelsexponering till flera dagar efter att läkemedlet sköljts bort. Tidigt såg de aktivering av ett klassiskt cellulärt stressprogram centrerat kring en gen kallad JUN. När exponeringen fortsatte bredde denna stressignal ut sig till en fullskalig självdestruktionskascade: gener som driver celler mot programmerad celldöd blev starkt påslagna, medan skyddande partners överväldigades. Samtidigt blev gener kopplade till inflammation och smärtsignalering mer aktiva. Neuronerna började producera fler inflammatoriska budbärare, smärtrelaterade peptider och receptorer som gör celler mer känsliga för skadliga stimuli—förändringar som speglar det som ses i smärtsamma nervsjukdomar.
Djupdykning i proteiner och fetter inne i neuronerna
Eftersom gener bara är ritningar undersökte teamet också de proteiner som faktiskt fanns i neuronerna samt deras lipid (fett) sammansättning. Efter 48 timmar av paclitaxelexponering uppträdde många av samma stress- och inflammationssignaler som upptäckts på RNA‑nivå även som ökade proteinnivåer, vilket bekräftar att neuronerna verkställde dessa skadliga program. Slående var att proteiner som behövs för axonal transport—de molekylära motorerna och stommen som flyttar last längs de långa nervfibrerna—var kraftigt reducerade. Detta inkluderade kinesiner och regulatoriska proteiner som håller mikroTubuli-spåren stabila. På lipidnivå visade neuronerna ett fall i viktiga byggstenar för kolesterol och membranlipider, samtidigt som lagrade fetter kallade triacylglyceroler ökade. Tillsammans tyder dessa skiften på att paclitaxel inte bara utlöser celldödssignalvägar utan också försvagar den fysiska strukturen och energibalansen i nervfibrerna.
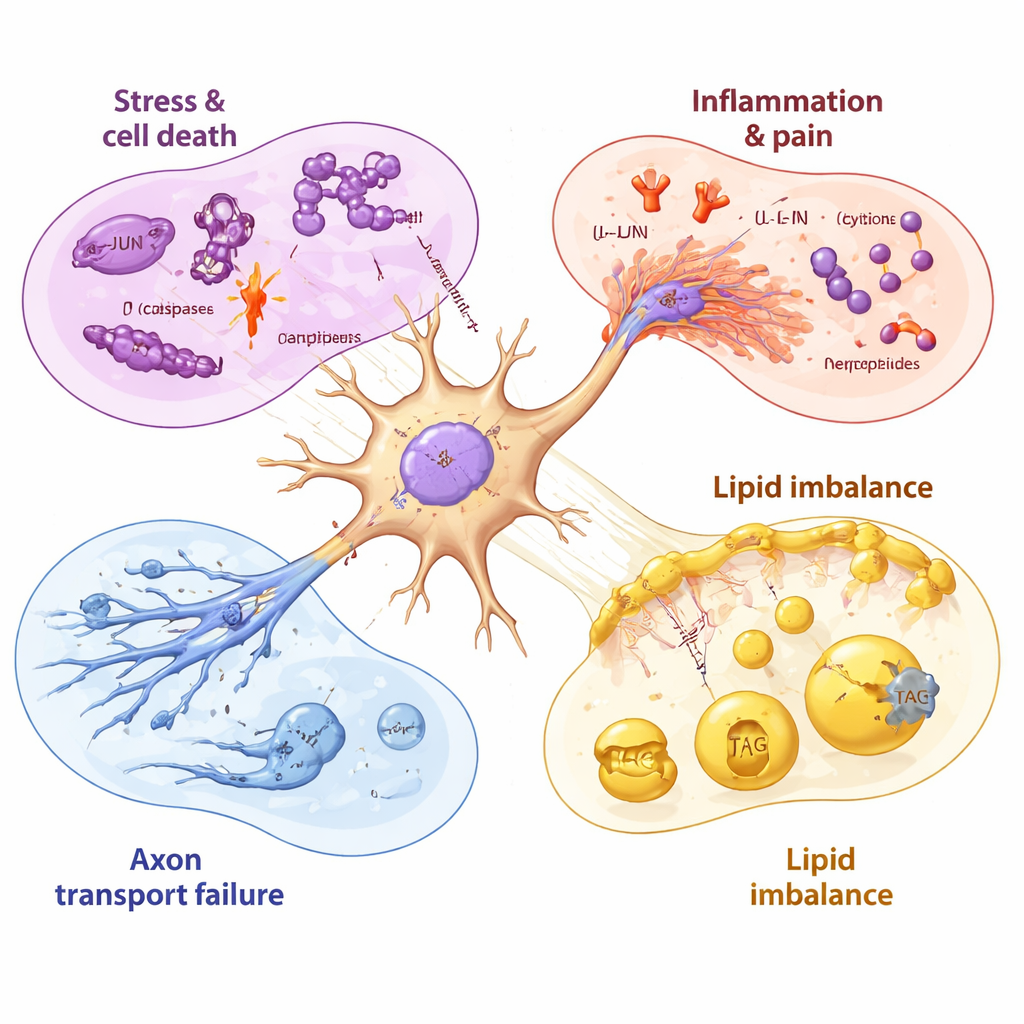
En tidslinje för nervskada och ofullständig återhämtning
Genom att provta neuronerna före, under och efter läkemedelsexponering kunde forskarna ordna dessa händelser i tid. Mitokondriella (energirrelaterade) gener stördes inom timmar, följt av stressgenen JUN, och sedan en starkare aktivering av celldöds- och inflammationsprogram när livskraften började falla. Även efter att paclitaxel tagits bort förblev många skadliga signaler förhöjda i flera dagar, medan generna som behövs för att tillverka friska membranlipider fortsatte att sjunka. Några sent uppkommande molekyler, såsom en läkemedels-effluxpump som kan föra ut paclitaxel och vissa tillväxtfaktorer, antydde att neuronerna försökte skydda och reparera sig—men dessa svar verkade relativt långsamma och ofullständiga jämfört med den snabba, tidiga drivningen mot skada.
Vad detta betyder för patienter som lever med nervsmärta
För en lekman är budskapet att paclitaxel skadar sensoriska nerver genom en samordnad serie av slag: det stressar deras energisystem, växlar genetiska brytare mot celldöd, rör upp inflammation och smärtsignalering, stör de interna ”transportmotorvägarna” inne i nervfibrerna och förändrar fetterna som håller nervmembran stabila. Genom att kartlägga dessa förändringar i människoderiverade neuroner med hög detaljrikedom lyfter studien fram konkreta, läkbara mål—såsom specifika stressregulatorer, inflammatoriska receptorer och lipid‑producerande enzymer—som skulle kunna blockeras eller stödjas för att skydda nerver utan att försvaga cancerbehandlingen. Medan nya terapier kräver vidare prövning erbjuder detta arbete en tydligare färdplan för att förebygga eller lindra kemoterapiinducerad nervskada och förbättra livskvaliteten för canceröverlevare.
Citering: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
Nyckelord: kemoterapiinducerad perifer neuropati, paclitaxel, sensoriska neuroner, neuroinflammation, axondegeneration