Clear Sky Science · sv
Reversibel argininmetylering reglerar mitokondriell IDH2-aktivitet: samordnad kontroll av CARM1 och KDM3A/4A
Finjustering av cellens kraftverk
Mitokondrier, ofta kallade cellernas kraftverk, gör långt mer än att bara producera energi. De justerar ständigt hur de förbränner bränsle för att möta kroppens behov, och när detta går fel kan det bidra till sjukdomar som diabetes, hjärtsvikt och cancer. Denna studie avslöjar en dold ”dimratt” inne i mitokondrierna: en liten kemisk markör på en enda byggsten i ett nyckelenzym, IDH2, som hjälper avgöra om mitokondrierna går på låg växel eller skruvar upp sin energiproduktion.
En liten tagg med stora konsekvenser
Proteiner i våra celler är inte statiska; de modifieras ofta med små kemiska grupper som ändrar hur de beter sig. Medan många sådana modifieringar i cellkärnan och cytosolen är väl kända, är de inne i mitokondrierna mindre utforskade. Författarna fokuserade på en särskild typ av märkning som kallas argininmetylering och frågade om den kan styra hur mitokondriella enzymer fungerar. De inriktade sig på ett enzym kallat IDH2, en arbetsmyra i trikarboxylsyracykeln (TCA), som hjälper till att omvandla näringsämnen till både energi och viktiga metaboliska byggstenar. Med biokemiska verktyg och masspektrometri fann de att IDH2 bär en specifik metylmärka på en aminosyra, arginin 188, och att denna märkning sätts dit av ett enzym kallat CARM1 som oväntat fungerar inne i mitokondrierna.
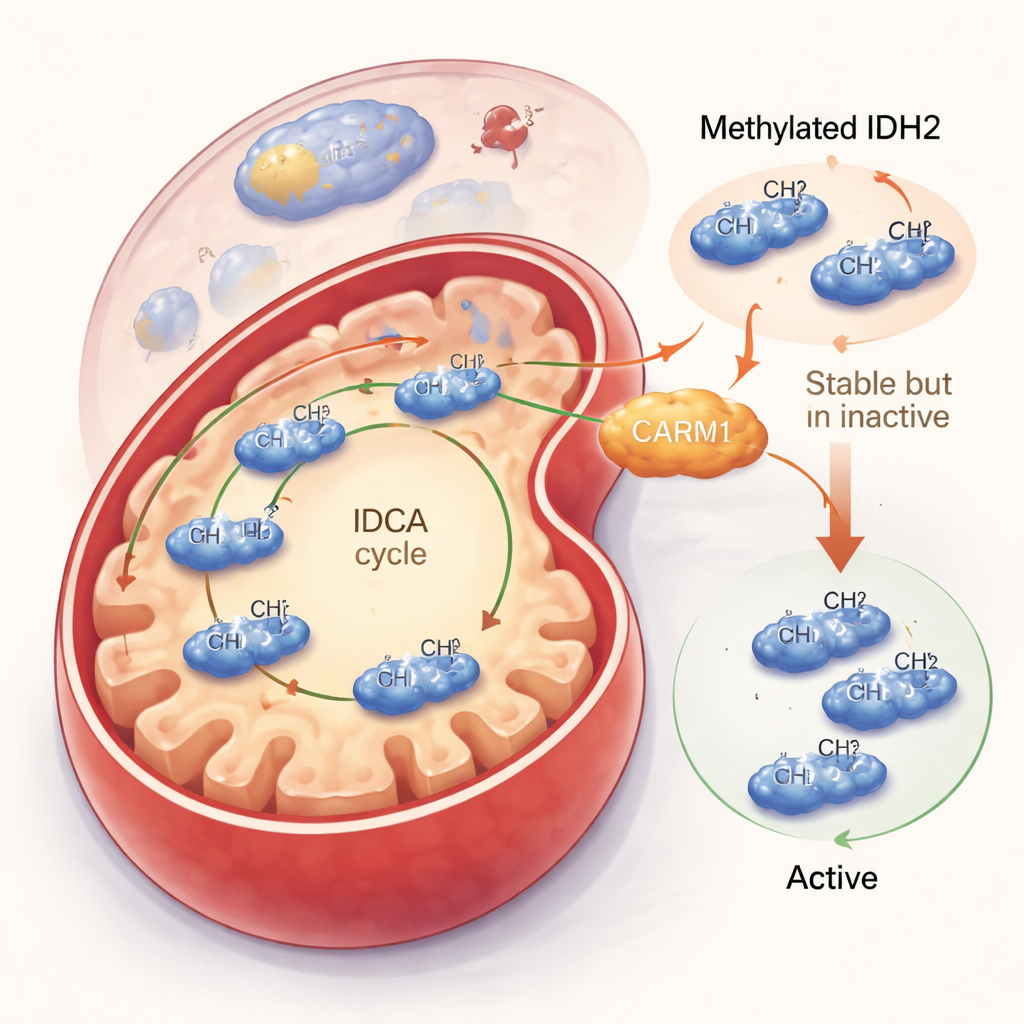
Stänger ner IDH2 men gör det mer beständigt
Teamet undersökte sedan vad denna metylmarkering faktiskt gör. När CARM1 var aktivt och kunde metylera IDH2 blev IDH2-proteinet mer stabilt och fanns kvar längre i cellen. Men denna till synes positiva effekt kom med en kompromiss: metylerat IDH2 var mindre aktivt. I cellförsök och rena proteinanalyser producerade metylerat IDH2 mindre av sin huvudsakliga produkt, alfa-ketoglutarat, och genererade mindre av den skyddande molekylen NADPH. I kontrast bildade en version av IDH2 som inte kunde metyleras vid arginin 188 fler av den aktiva dimerformen, fungerade snabbare och ökade både alfa-ketoglutarat- och NADPH-nivåerna. Även om mängden av detta ometylerade IDH2 totalt var lägre gjorde varje molekyl mer arbete, vilket ledde till en nettouppgång i mitokondriell aktivitet.
En reversibel strömbrytare med två sudd
Avgörande är att denna metylmärkning inte är permanent. Forskarna visade att två enzymer som normalt är kända för att ta bort en annan sorts märkning, lysindemetyleraserna KDM3A och KDM4A, också kan radera argininmetylmärket från IDH2. När dessa demetyleraser fanns närvarande förlorade argininen vid position 188 sina extra kemiska grupper, IDH2 blev mindre stabilt men mer aktivt, och andelen dimerform ökade. Celler med mer aktiv KDM3A eller KDM4A visade högre mitokondriemembranpotential och förbrukade mer syre, tecken på att deras mitokondrier gick varmare på oxidativ metabolism. När dessa enzymer minskades skedde motsatsen: IDH2-aktiviteten sjönk och mitokondriernas prestanda försvagades, vilket understryker att detta är ett reversibelt kontrollsystem snarare än en envägsförändring.
Kopplingen mellan metabolism och sjukdom
Eftersom IDH2 har kopplats till cancer och andra sjukdomar undersökte författarna hur denna metyleringsomkopplare kan spela roll i sjukdomsliknande miljöer. I olika normala och cancercellinjer observerade de att högre IDH2-proteinnivåer ofta gick hand i hand med mer metylering och förvånansvärt lägre enzymaktivitet, vilket tyder på att ”mer protein” inte alltid betyder ”mer funktion”. I bröstcancer-dataset tenderade patienter med högre IDH2-proteinnivåer att ha sämre överlevnad, även om IDH2-genaktivitet inte korrelerade med utfall. Resultaten stöder en modell där CARM1-driven metylering bromsar TCA-cykeln och skjuter celler mot alternativa, cancerfavoriserade sätt att använda näringsämnen, medan demetyleraser som KDM3A och KDM4A kan föra tillbaka cellerna mot effektivare energiproduktion.
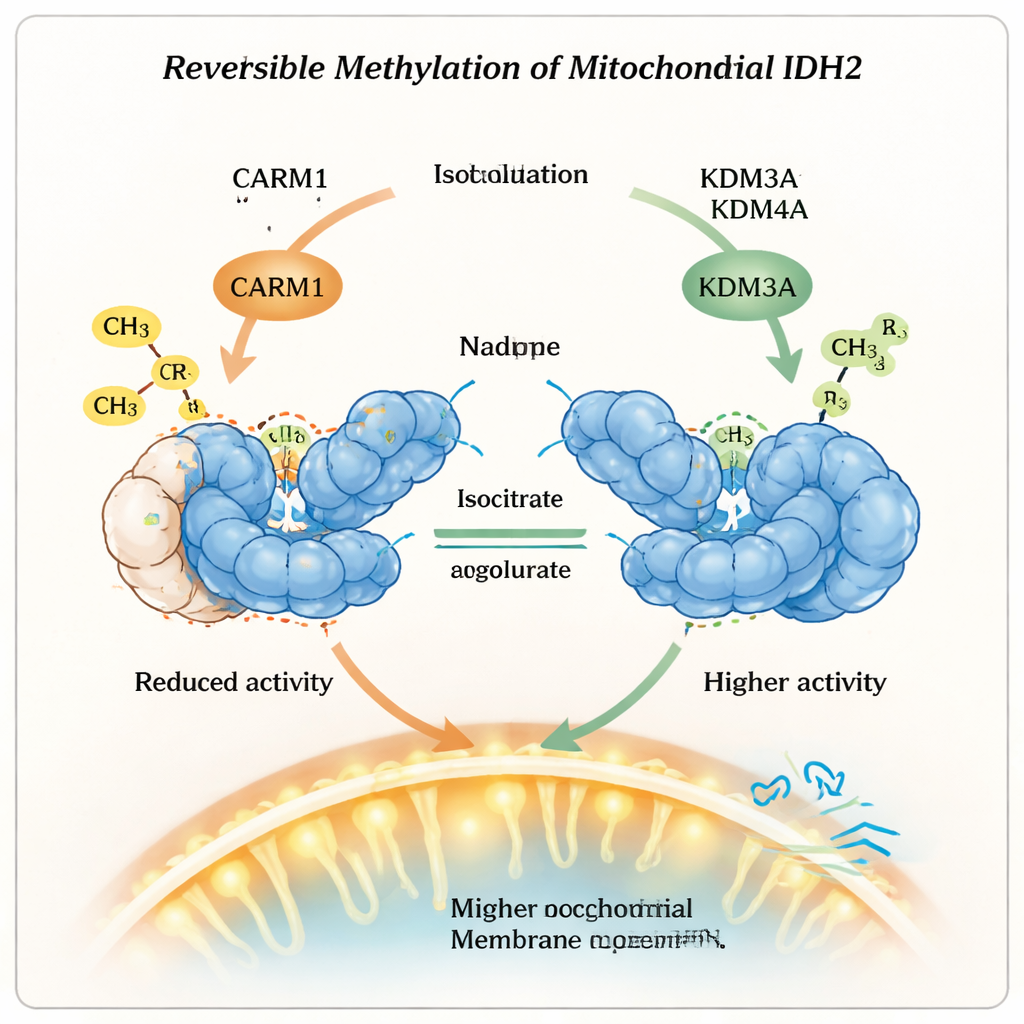
Vad detta betyder för hälsa och terapi
I enkla termer visar detta arbete att mitokondrier inte bara slår enzymer av eller på, utan använder reversibla kemiska märkningar som finjusterade rattar. Genom att lägga till en metylgrupp förvandlar CARM1 IDH2 till en längre levande men mindre aktiv form; genom att ta bort den märkningen offrar KDM3A och KDM4A viss stabilitet för att vinna mer kraft. Denna balans påverkar hur celler väljer mellan snabb men ineffektiv sockerförbränning och långsammare, mer effektiv energiproduktion. Att förstå denna metylerings-”dimratt” på IDH2 öppnar nya möjligheter för terapier som syftar till att korrigera felaktig mitokondriell metabolism vid tillstånd som cancer och metabola sjukdomar, genom att rikta in sig på enzymerna som skriver och raderar dessa små men kraftfulla kemiska märken.
Citering: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
Nyckelord: mitokondrier, IDH2, argininmetylering, cellmetabolism, CARM1