Clear Sky Science · sv
Honokiol blockerar tumörutveckling och metastas genom mitokondrieinriktade effekter
Att förvandla en trädsläkts förening till ett cancerbekämpningsmedel
Många cancerläkemedel kommer från växtriket, och forskare upptäcker fortfarande hur några av dessa naturliga molekyler verkar inne i våra celler. Denna studie fokuserar på honokiol, ett ämne som finns i magnoliabark och som länge använts i traditionell medicin, och visar hur det kan rikta in sig direkt mot de små kraftverk som finns i cancerceller för att bromsa tumörtillväxt och blockera spridning, samtidigt som normala celler i huvudsak skonas.
Cellernas kraftstationer
Varje cell är beroende av mitokondrier, ofta kallade cellens ”kraftstationer”, för att generera energimolekylen ATP. I cancer gör mitokondrier mer än att bara producera bränsle — de hjälper till att avgöra om en cell överlever eller dör. En stor molekylmaskin, ATP-syntas, sitter i mitokondriens inre membran och tillverkar ATP. Cancerceller överproducerar ofta ett medhjälparprotein som kallas IF1 och som hakar fast vid ATP-syntas och fungerar som ett slags säkerhetslås, vilket hjälper tumörer att motstå en form av självförstöring känd som mitokondriell permeabilitetstransition och efterföljande celldöd.
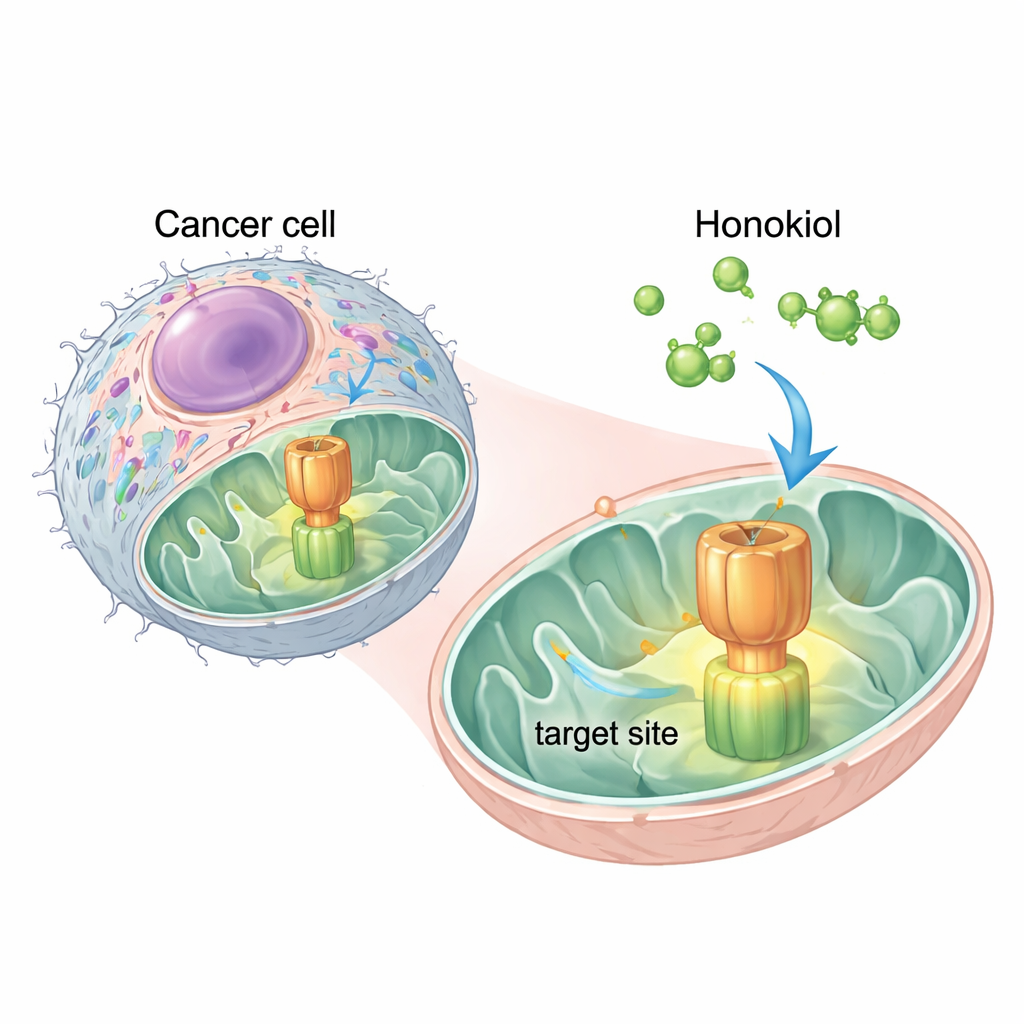
En naturlig molekyl hittar en kritisk brytare
Forskarna använde datorbaserade simuleringar för att se var honokiol skulle kunna binda på ATP-syntas. De fann två lovande ”docknings”ställen på en av dess komponenter, ett område som kallas OSCP. Det starkaste stället överlappade med samma yta som IF1 använder för att hålla sig fast vid ATP-syntas. Detta antydde att honokiol skulle kunna fungera som ett molekylärt kil, slinka in i OSCP och tränga undan IF1. Experiment med mänskliga livmoderhalscancerceller (HeLa) bekräftade denna idé: tillsats av honokiol minskade den fysiska kontakten mellan IF1 och OSCP, utan att störa andra delar av enzymet, vilket visar att effekten var specifik.
Från celler till levande djur: mindre tumör, mindre spridning
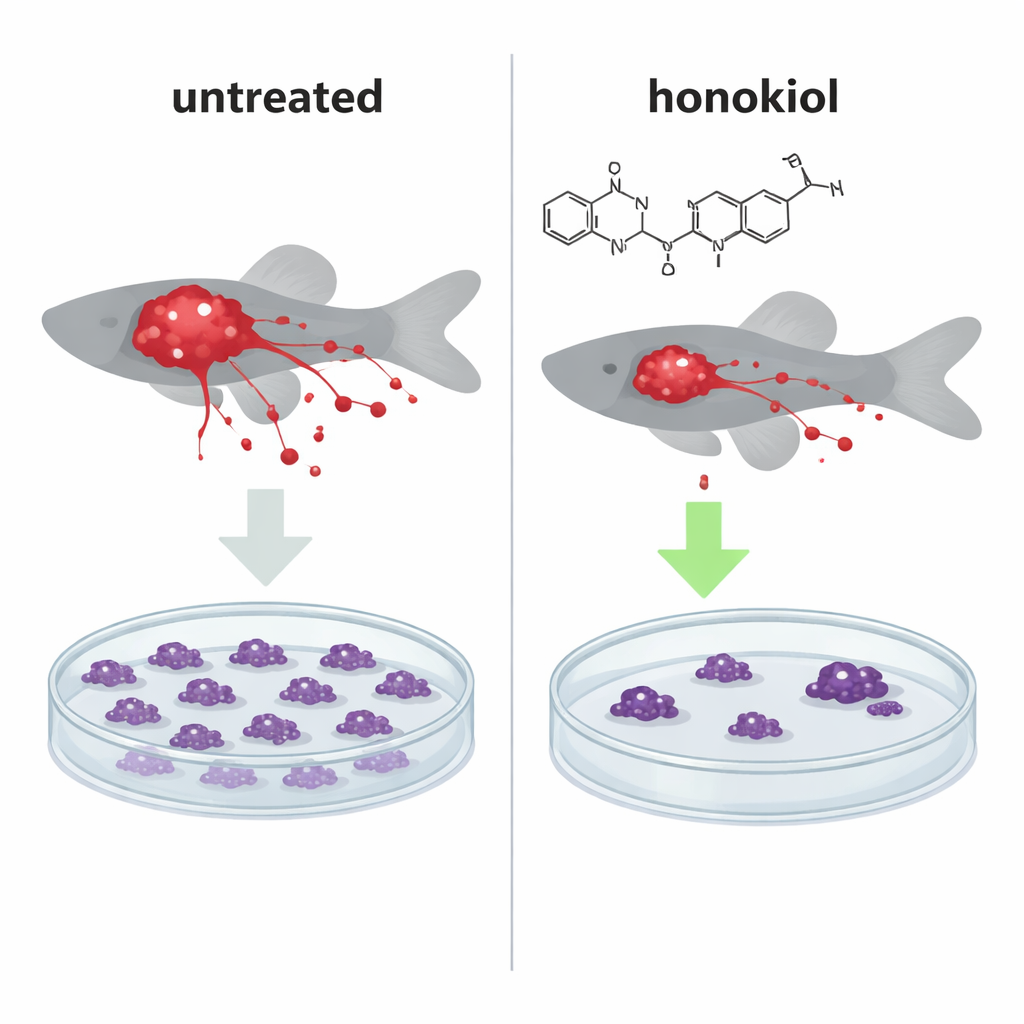
För att se om detta molekylära knuffande hade verklig effekt implanterade teamet lysande mänskliga cancerceller i små zebrafisksembryon, en väletablerad heldjursmodell för att följa tumörtillväxt och metastasering. I fisk som injicerats med normala, IF1-rika HeLa-celler krympte tumörmassorna avsevärt vid behandling med honokiol och antalet cancerceller som spreds till avlägsna områden minskade, vilket gav ett mönster som liknade fisk som injicerats med IF1-knockout-celler som saknar det skyddande proteinet. Intressant nog minskade honokiol även antalet metastatiska celler när IF1 var frånvarande, vilket tyder på en andra, IF1-oberoende mekanism för att begränsa cancerspridning.
Att tvinga defekta kraftverk att utlösa självförstörelse
Tillbaka i odlingsskålen minskade honokiol cancercellernas förmåga att bilda stora kolonier i mjuk agar, ett test som efterliknar de stressiga, lågsyremiljöerna inne i solida tumörer. Detta skedde utan en stor broms i vanlig celldelning eller i grundläggande mitokondriell respiration, vilket istället pekar mot en förändring i hur mitokondrier avgör mellan liv och död. Mätningar av kalciumhantering visade att honokiol gjorde att mitokondrier öppnade permeabilitetstransitionsporen vid lägre kalciumnivåer, en känd utlösare för svullnad och frisättning av dödsfrämjande faktorer. Vid måttliga doser berodde denna effekt på förskjutning av IF1; vid högre doser agerade honokiol via sin andra OSCP-bindningsplats och genom ökad bildning av reaktiva syreföreningar, vilket gjorde även IF1‑defekta celler känsligare för programmerad celldöd.
Att stoppa cancerceller från att förflytta sig
Cancer blir som farligast när celler lossnar och migrerar till nya organ. I sår‑lika ”scratch”-tester bromsade honokiol starkt den kollektiva migrationen av cancercellskikt och minskade markörer för epitelial-mesenkymal omvandling, en process som utrustar tumörceller för rörelse och inväxt. Detaljerade elektronmikroskopbilder visade att migrerande celler normalt förstorar och omformar sina mitokondrier, lägger till interna veck för att möta höga energibehov vid framkanten. Med honokiol blev dessa frontlinjemitokondrier istället svullna och strukturellt skadade — kännetecken för öppnande av permeabilitetstransitionsporen — medan mitokondrier i icke-rörliga regioner påverkades mindre eller till och med ökade i antal, beroende på IF1.
Vad detta betyder för framtida cancerbehandlingar
Enkelt uttryckt visar detta arbete att honokiol kan rikta sig mot en liten regulatorisk region av mitokondriernas ATP‑tillverkande maskineri och slå om en inbyggd säkerhetsfunktion som cancerceller ofta håller låst. Genom att avlägsna IF1 och direkt putta poren mot öppning uppmuntrar honokiol tumörceller att självförstöra och försvårar deras förmåga att migrera och så frön till metastaser. Eftersom dessa effekter härrör från egenskaper som många cancerformer delar — snarare än från en enda yta-markör — kan inriktning på OSCP‑regionen i ATP‑syntas inspirera en ny klass av terapier som utnyttjar sårbarheterna i cancercellernas kraftverk samtidigt som skadan på frisk vävnad begränsas.
Citering: Grandi, M., Boldrin, F., Risato, G. et al. Honokiol blocks tumor development and metastasis through mitochondrion-targeted effects. Cell Death Dis 17, 186 (2026). https://doi.org/10.1038/s41419-026-08441-6
Nyckelord: honokiol, mitokondrier, ATP-syntas, apoptos, metastas