Clear Sky Science · sv
Immune checkpoint inhibitor-relaterad pneumonit: aktuella framsteg och den hypotetiska rollen för terapi med mesenkymala stamceller
När cancerbehandling slår tillbaka mot lungorna
Läkemedel som släpper loss immunsystemet mot cancer har förändrat vården vid sjukdomar som lungcancer och melanom. Men denna nya kraft har en baksida: hos vissa patienter riktar samma immunsvar som attackerar tumörer också in sig mot lungorna och orsakar ett tillstånd som kallas immune checkpoint inhibitor-relaterad pneumonit (ICIP). Denna översikt förklarar vad ICIP är, varför det uppstår, hur läkare i dag behandlar det, och varför en särskild typ av stamcell — mesenkymala stamceller (MSC) — en dag skulle kunna erbjuda ett säkrare, mer precist sätt att dämpa inflammationen utan att offra cancerkontrollen. 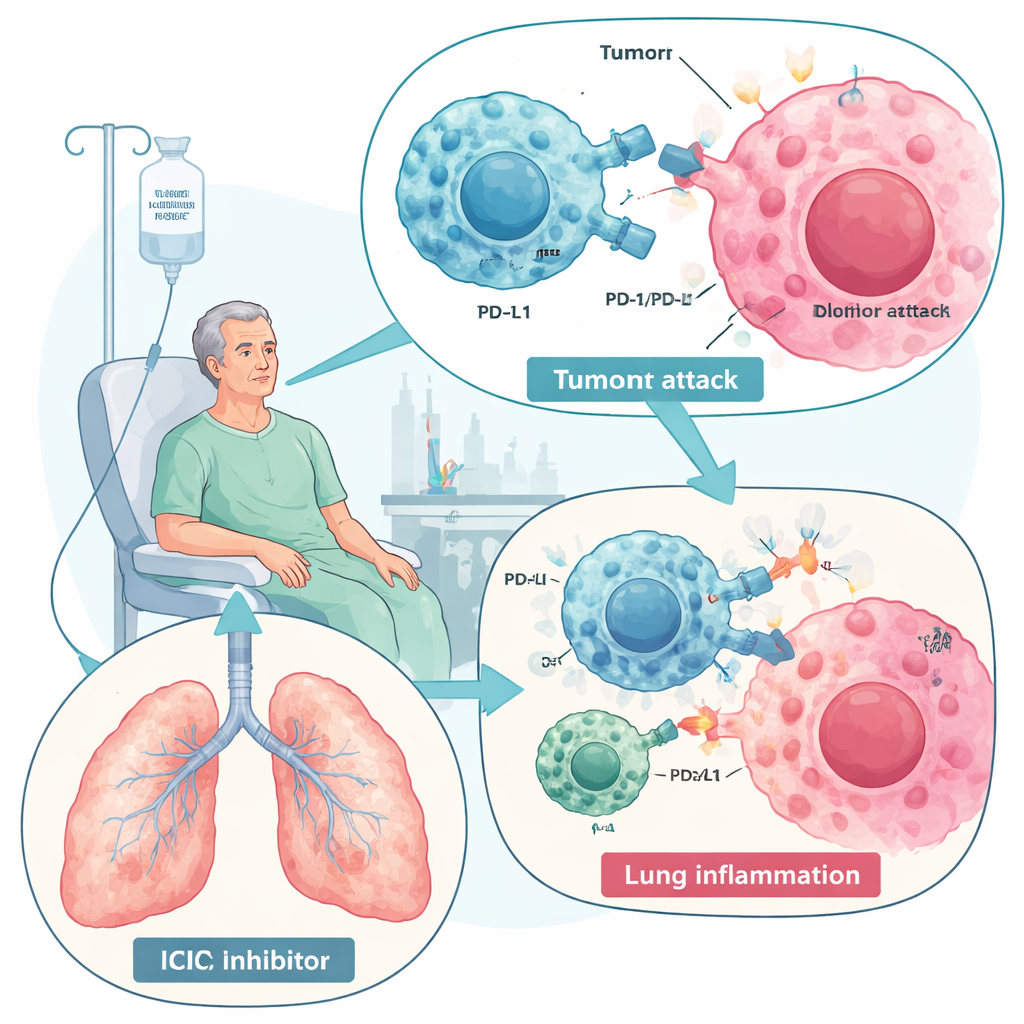
Kraftfulla cancerläkemedel med en dold lungrisk
Immune checkpoint-hämmare, särskilt de som blockerar PD-1 och PD-L1, fungerar genom att ta bort molekylära ”bromsar” som normalt håller immunsvaret i schack. När bromsarna släppts kan T‑celler bättre känna igen och förstöra cancerceller, vilket förbättrar överlevnaden vid många tumörtyper. Men samma förstärkning kan rubba normal tolerans och utlösa immunrelaterade biverkningar i flera organ. ICIP är den allvarligaste lungkomplikationen av dessa läkemedel och en av de ledande immunrelaterade orsakerna till behandlingsrelaterad död. Förekomsten varierar från några procent till nästan en tredjedel av patienterna i vissa realvärdsstudier, särskilt hos dem med lungcancer eller tidigare lungsjukdom som KOL eller interstitiell lungsjukdom. Symtomen sträcker sig från mild hosta och andfåddhet till livshotande andningssvikt.
Hur immunsystemet skadar lungan
Översikten beskriver ICIP som resultatet av en rubbad immunbalans i lungorna. Överaktiva ”strids”-celler — CD8 T‑celler, vissa hjälpar-T‑celler, inflammatoriska makrofager, neutrofiler och natural killer‑celler — översvämmer lungvävnaden och släpper ut aggressiva signalsubstanser, inklusive interferon‑gamma, TNF‑alfa och interleukiner som IL‑6 och IL‑17. Samtidigt minskar normalt skyddande celler som dämpar inflammation, såsom regulatoriska T‑celler och reparationsinriktade makrofager. Vissa patienter visar också ökande nivåer av självreaktiva antikroppar före eller under behandling, vilket tyder på att ICIP delvis kan likna en autoimmun sjukdom. I bronkoalveolärt spolningsvätska finner läkare ett T‑cellsrikt inflammatoriskt mönster och en cytokinprofil som skiljer sig från infektion eller tumörprogression, vilket kan hjälpa vid diagnostik.
Att se, gradera och behandla skadan
På CT‑skanningar syns ICIP oftast som disiga ”ground‑glass”-områden eller fläckiga konsolideringar spridda genom båda lungorna, mönster som skiljer sig från strålskada som förblir begränsad till det bestrålade fältet. Läkare ställer diagnosen ICIP genom att kombinera röntgenfynd, symtom och en noggrann uteslutning av infektion och andra orsaker. Internationella riktlinjer graderar sedan svårighetsgraden från 1 (lindrig, ofta endast radiologisk) till 4 (livshotande andningssvikt). Dagens hörnsten i behandlingen är glukokortikoider — starka antiinflammatoriska steroider — ibland i kombination med andra immunhämmande läkemedel som tocilizumab (som blockerar IL‑6) eller infliximab (som blockerar TNF‑alfa) vid svåra eller steroidresistenta fall. Dessa tillvägagångssätt kan rädda liv, men de är grova verktyg: steroider ger många biverkningar, vissa patienter svarar inte, och bred immunosuppression kan försvaga just det antitumörsvar som läkemedlen var avsedda att förstärka.
Varför stamceller kommer in i diskussionen
Mesenkymala stamceller, som kan utvinnas från benmärg, fett eller navelsträngsvävnad, har framträtt som lovande ”immunsmodulerare” snarare än enbart vävnadsbyggare. När de ges i blodbanan fastnar många av dessa celler temporärt i lungornas fina blodkärl — en så kallad first‑pass‑effekt — vilket är en nackdel för behandling av avlägsna organ men en potentiell fördel för lungsjukdomar. I djurmodeller och tidiga kliniska prövningar vid tillstånd som svår pneumoni, akut respiratoriskt distressyndrom, inflammatorisk tarmsjukdom och graft‑versus‑host‑sjukdom dämpar MSCs överaktiva immunsvar, förskjuter immunceller mot ett mer balanserat tillstånd och utsöndrar tillväxtfaktorer som främjar vävnadsreparation samtidigt som ärrbildning begränsas. Viktigt är att deras fördelar ofta uppstår inte genom att de själva blir lungceller utan via blandningen av signalsubstanser och små vesiklar de frigör. 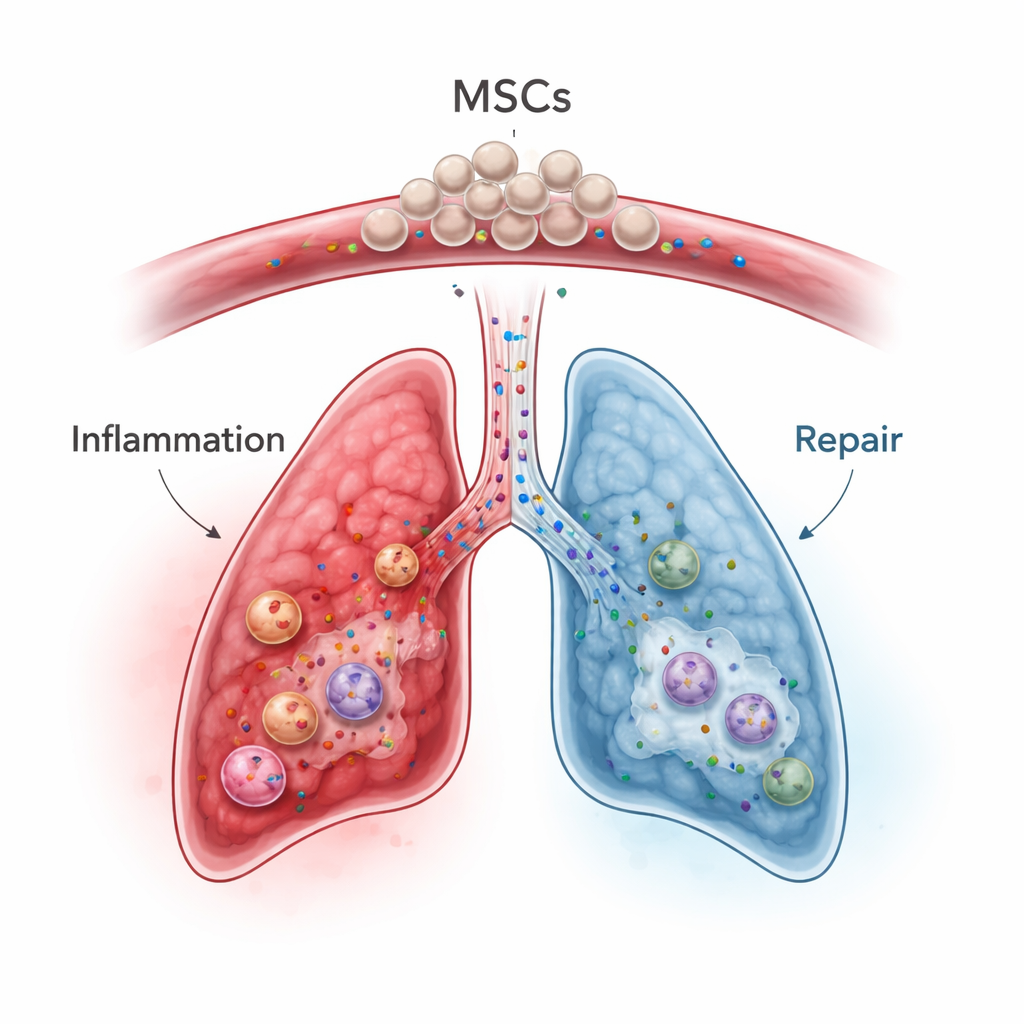
Hur MSCs kan dämpa ICIP utan att förstöra behandlingen
I sammanhanget av ICIP skulle MSCs i teorin kunna tackla flera problem samtidigt. De kan direkt hämma aktiverade T‑celler, främja tillväxt och funktion hos regulatoriska T‑celler och styra makrofager bort från ett aggressivt, vävnadsskadande läge mot ett läkningsinriktat. De sänker också viktiga inflammatoriska budbärare som IL‑6, IL‑1β och TNF‑alfa, och ökar antiinflammatoriska faktorer och skyddande proteiner som TSG‑6 som hjälper till att begränsa lungskada och fibros. Prekliniska studier tyder på att MSCs eller ingenjörsproducerade MSC‑deriverade exosomer kan minska cytokinstormar och organskador inducerade av checkpoint‑hämmare eller strålning, samtidigt som de i vissa situationer bevarar antitumoraktivitet bättre än standardimmunosuppressiva medel. Författarna varnar dock för att MSCs också kan interagera med tumörer och blodkoagulation på komplexa sätt, och att deras effekter starkt beror på den omgivande inflammatoriska miljön och till och med på MSC‑källan (benmärg, fett eller navelsträng).
Framtiden: löfte med noggrann prövning
För patienter vars cancerbehandling avbryts eller hotas av svår lungtoxicitet kan MSC‑baserade terapier så småningom erbjuda ett mer riktat sätt att kyla ner inflammation, reparera lungvävnad och förebygga långsiktig ärrbildning — helst utan att urholka de livräddande effekterna av immune checkpoint‑inhibitorer. Hittills har dock inga ICIP‑specifika MSC‑prövningar slutförts. Författarna argumenterar för att väl utformade djurstudier och kliniska prövningar behövs skyndsamt för att definiera vilken typ av MSC eller exosomprodukt som fungerar bäst, hur mycket som ska ges, när den bör ges i förhållande till steroider och immunterapi, och hur man övervakar risker som tumörtillväxt eller koagulationsstörningar. Fram till dess förblir MSCs ett hoppfullt men fortfarande experimentellt alternativ i horisonten för att hantera denna allvarliga biverkan av modern cancerbehandling.
Citering: Li, Z., Zheng, X., Xia, H. et al. Immune checkpoint inhibitor-related pneumonitis: current advances and the putative role of mesenchymal stem cell therapy. Cell Death Dis 17, 200 (2026). https://doi.org/10.1038/s41419-026-08440-7
Nyckelord: immunoterapins biverkningar, pneumonit, checkpoint-hämmare, mesenkymala stamceller, lunginflammation